Aktiva ingredienser: Candesartan
Atacand 4 mg tabletter
Atacand 8 mg tabletter
Atacand 16 mg tabletter
Atacand 32 mg tabletter
Varför används Atacand? Vad är det för?
Läkemedlets namn är Atacand. Den aktiva ingrediensen är candesartan cilexetil. Det tillhör en grupp läkemedel som kallas angiotensin II -receptorantagonister. Det fungerar genom att få blodkärlen att slappna av och vidgas. Detta hjälper till att sänka blodtrycket. Det får också hjärtat att pumpa blod lättare runt om i världen. Kroppen.
Atacand kan användas för:
- behandla högt blodtryck (hypertoni) hos vuxna patienter och hos barn och ungdomar i åldern 6 till 18 år.
- behandla hjärtsvikt hos vuxna patienter med nedsatt hjärtmuskelfunktion när Angiotensin Converting Enzyme (ACE) -hämmare inte kan användas eller förutom ACE -hämmare när symtomen kvarstår trots behandling och antagonister mineralocorticoid receptor (MRA) inte kan användas (ACE -hämmare och MRA är läkemedel används för att behandla hjärtsvikt).
Kontraindikationer När Atacand inte ska användas
Ta inte Atacand:
- om du är allergisk mot candesartan cilexetil eller något annat innehållsämne i detta läkemedel (anges i avsnitt 6).
- om du är mer än tre månader gravid (det är också bättre att undvika Atacand under tidig graviditet - se avsnittet om graviditet)
- om du har allvarlig leversjukdom eller gallvägsobstruktion (problem med dränering av gallan från gallblåsan)
- om patienten är ett barn under 1 år. om han har diabetes eller nedsatt njurfunktion och behandlas med ett blodtryckssänkande läkemedel som innehåller aliskiren.
Om du inte är säker på om något av detta gäller dig, rådfråga din läkare eller apotekspersonal innan du tar Atacand.
Försiktighetsåtgärder vid användning Vad du behöver veta innan du tar Atacand
Tala med din läkare innan du tar Atacand:
- om du har hjärt-, lever- eller njurproblem eller är i dialys.
- om du nyligen har genomgått en njurtransplantation.
- om du kräks, nyligen har haft kraftiga kräkningar eller har diarré.
- om du har en binjurssjukdom som kallas Conn's syndrom (kallas även primär aldosteronism).
- om du har lågt blodtryck.
- om du någonsin har haft stroke.
- tala om för din läkare om du tror att du är gravid (eller om det finns möjlighet att bli gravid). Atacand rekommenderas inte under tidig graviditet och får inte tas om du är mer än tre månader gravid, eftersom det kan orsaka allvarlig skada på ditt barn om det används i det skedet (se avsnittet om graviditet).
- om du tar något av följande läkemedel som används för att behandla högt blodtryck:
- en "ACE-hämmare" (t.ex. enalapril, lisinopril, ramipril), särskilt om du har diabetesrelaterade njurproblem.
- aliskiren.
- Om du tar en ACE -hämmare tillsammans med ett läkemedel som tillhör klassen läkemedel som kallas mineralokortikoidreceptorantagonister (MRA). Dessa läkemedel används för att behandla hjärtsvikt (se "Ta andra läkemedel")
Din läkare kan kontrollera din njurfunktion, blodtryck och mängden elektrolyter (till exempel kalium) i ditt blod med jämna mellanrum.
Se även information under rubriken "Ta inte Atacand om".
Din läkare kan behöva träffa dig oftare och bli testad om du har något av dessa tillstånd.
Om du ska opereras ska du tala om för din läkare eller tandläkare att du tar Atacand, eftersom Atacand i kombination med bedövning kan orsaka blodtrycksfall.
Barn och ungdomar
Atacand har studerats hos barn. Fråga din läkare för mer information. Atacand ska inte ges till barn under 1 år på grund av den potentiella risken för att utveckla njurar.
Interaktioner Vilka läkemedel eller livsmedel kan ändra effekten av Atacand
Tala om för din läkare eller apotekspersonal om du tar, nyligen har tagit eller kan tänkas ta andra läkemedel. Atacand kan påverka hur vissa andra läkemedel fungerar, och vissa läkemedel kan påverka Atacand. Om du tar vissa läkemedel kan din läkare behöva ta blodprov då och då.
Tala särskilt om för din läkare om du tar något av följande läkemedel eftersom din läkare kan behöva ändra din dos och / eller vidta andra försiktighetsåtgärder:
- andra läkemedel som hjälper till att sänka blodtrycket, inklusive betablockerare, diazoxid och ACE -hämmare som enalapril, captopril, lisinopril eller ramipril
- icke-steroida antiinflammatoriska läkemedel (NSAID) som ibuprofen, naproxen, diklofenak, celecoxib eller etoricoxib (läkemedel för att lindra smärta och inflammation)
- acetylsalicylsyra (om du tar mer än 3 g per dag) (läkemedel för att lindra smärta och inflammation)
- kaliumtillskott eller kaliuminnehållande saltsubstitut (läkemedel som ökar kaliumnivån i blodet)
- heparin (ett läkemedel för att tunna blodet)
- cotrimoxazol (ett antibiotikum), även känt som trimetoprim / sulfametoxazol.
- tabletter som hjälper dig att kissa (diuretika)
- litium (ett läkemedel mot psykiska problem)
- om du tar en ACE -hämmare eller aliskiren (se även information under rubrikerna: "Ta inte Atacand om" och "Var särskilt försiktig med Atacand")
- om du behandlas med en ACE -hämmare tillsammans med andra läkemedel som används för hjärtsvikt, kända som mineralokortikoidreceptorantagonister (MRA) (t.ex. spironolakton, eplerenon).
Atacand med mat, dryck och alkohol
- Du kan ta Atacand med eller utan mat.
- Tala med din läkare när du förskrivit Atacand innan du dricker alkohol. Alkohol kan få dig att känna dig svag eller yr.
Varningar Det är viktigt att veta att:
Graviditet och amning
Graviditet
Du bör tala om för din läkare om du tror att du är gravid (eller om det finns risk för att du blir gravid). Din läkare kommer vanligtvis att råda dig att sluta ta Atacand innan du blir gravid eller så snart du vet att du är gravid och kommer att råda dig att ta ett annat läkemedel istället för Atacand. Tidig graviditet och får inte tas om du är mer än tre månader gravid eftersom det kan orsaka allvarlig skada på ditt barn om det tas efter den tredje graviditetsmånaden.
Matdags
Tala om för din läkare om du ammar eller ska börja amma. Atacand rekommenderas inte för kvinnor som ammar och din läkare kan välja en annan behandling för dig om du vill amma, särskilt om din baby är nyfödd eller född för tidigt.
Köra och använda maskiner
Vissa människor kan känna sig trötta eller yr när de tar Atacand. Om detta händer dig ska du inte köra bil eller använda några verktyg eller maskiner.
Atacand innehåller laktos. Laktos är en typ av socker. Om din läkare har fått veta att du inte tål vissa sockerarter, kontakta din läkare innan du tar detta läkemedel.
Dos, metod och administreringstid Hur man använder Atacand: Dosering
Ta alltid detta läkemedel enligt läkarens anvisningar. Kontakta din läkare eller apotekspersonal om du är osäker. Det är viktigt att fortsätta ta Atacand varje dag. Atacand kan tas med eller utan mat.
Svälj tabletten med en drink vatten.
Försök att ta tabletten vid samma tidpunkt varje dag. Detta hjälper dig att komma ihåg att ta det.
Högt blodtryck:
- Den vanliga dosen Atacand är 8 mg en gång om dagen. Din läkare kan öka denna dos upp till 16 mg en gång om dagen och ytterligare upp till 32 mg en gång om dagen beroende på ditt blodtryckssvar.
- Hos vissa patienter, till exempel de med leverproblem, njurproblem eller som nyligen tappat vätska på grund av till exempel: kräkningar, diarré eller att ta tabletter som hjälper till att kissa, kan läkaren ordinera en lägre startdos.
- Vissa svarta patienter kan reagera dåligt på detta läkemedel när de ges som den enda behandlingen och kan behöva en högre dos.
Användning till barn och ungdomar med högt blodtryck
Barn mellan 6 och 18 år:
Den rekommenderade startdosen är 4 mg en gång om dagen.
För patienter som väger mindre än 50 kg: Hos vissa patienter vars blodtryck inte är tillräckligt kontrollerat kan läkaren besluta om dosen ska ökas till högst 8 mg en gång om dagen.
För patienter som väger 50 kg eller mer: Hos vissa patienter vars blodtryck inte är tillräckligt kontrollerat kan läkaren besluta om dosen ska ökas till 8 mg en gång dagligen och 16 mg en gång dagligen.
Hjärtsvikt hos vuxna:
- den rekommenderade startdosen av Atacand är 4 mg en gång om dagen. Din läkare kan öka denna dos genom att fördubbla dosen med minst 2 veckors intervall till 32 mg en gång om dagen. Atacand kan tas tillsammans med andra läkemedel mot hjärtsvikt, och din läkare avgör vilken behandling som är bäst för dig.
Om du har glömt att ta Atacand
Ta inte en dubbel dos för att kompensera för en glömd tablett. Ta bara nästa dos som vanligt.
Om du slutar ta Atacand
Om du slutar ta Atacand kan ditt blodtryck stiga igen.
Sluta därför inte ta Atacand utan att först tala med din läkare.
Fråga din läkare eller apotekspersonal om du har ytterligare frågor om användningen av detta läkemedel.
Överdosering Vad du ska göra om du har tagit för mycket Atacand
Om du tar mer Atacand än vad din läkare har ordinerat, kontakta genast läkare eller apotekspersonal för råd.
Biverkningar Vilka är biverkningarna av Atacand
Liksom alla läkemedel kan detta läkemedel orsaka biverkningar men alla användare behöver inte få dem. Det är viktigt att du är medveten om vad dessa biverkningar kan vara.
Sluta ta Atacand och sök genast medicinsk hjälp om du upplever någon av följande allergiska reaktioner:
- andningssvårigheter, med eller utan svullnad i ansikte, läppar, tunga och / eller hals
- svullnad i ansikte, läppar, tunga och / eller hals, vilket kan orsaka svårigheter att svälja
- svår kliande hud (med upphöjda blåsor)
Atacand kan orsaka en minskning av antalet vita blodkroppar. Ditt motstånd mot infektion kan minska och du kan märka trötthet, infektion eller feber. Kontakta din läkare om detta händer. Din läkare kan ibland utföra blodprov för att kontrollera om Atacand har haft några effekter på ditt blod (agranulocytos).
Möjliga biverkningar inkluderar:
Vanliga (drabbar 1 till 10 användare av 100)
- Yrsel / yrsel
- Huvudvärk
- Luftvägsinfektion
- Lågt blodtryck. Detta kan få dig att känna dig svag eller yr.
- Förändringar i blodprovsresultat:
- En ökad mängd kalium i blodet, särskilt om du redan har njurproblem eller hjärtsvikt. Om detta är allvarligt kan du också märka trötthet, svaghet, oregelbunden hjärtslag eller stickningar.
- Effekter på hur dina njurar fungerar, särskilt om du redan har njurproblem eller hjärtsvikt. I mycket sällsynta fall kan njursvikt uppstå.
Mycket sällsynta (drabbar färre än 1 användare av 10 000)
- Svullnad i ansikte, läppar, tunga och / eller hals.
- En minskning av röda eller vita blodkroppar. Du kan märka trötthet, infektion eller feber.
- Hudutslag, svullna utslag (nässelfeber).
- Klåda.
- Ryggont, smärta i leder och muskler.
- Förändringar i leverns sätt, inklusive inflammation i levern (hepatit). Du kan märka trötthet, gulning av huden och ögonvita och influensaliknande symptom.
- Illamående.
- Förändringar i blodprovsresultat:
- En låg mängd natrium i blodet. Om detta är allvarligt kan du också märka svaghet, brist på energi eller muskelkramper.
- Hosta.
Hos barn som behandlas för högt blodtryck verkar biverkningar likna dem som ses hos vuxna, men de förekommer oftare. Halsont hos barn är en mycket vanlig men inte rapporterad biverkning hos vuxna och rinorré (rinnande näsa), feber och ökad hjärtfrekvens är vanliga hos barn men rapporteras inte hos vuxna.
Rapportering av biverkningar
Om du får några biverkningar, tala med din läkare, apotekspersonal eller sjuksköterska. Detta inkluderar eventuella biverkningar som inte nämns i denna bipacksedel. Du kan också rapportera biverkningar direkt via det nationella rapporteringssystemet på www.agenziafarmaco.gov. It / it / ansvarig. Genom att rapportera biverkningar kan du hjälpa till att ge mer information om läkemedlets säkerhet.
Giltighetstid och lagring
- Förvara detta läkemedel utom syn- och räckhåll för barn
- Använd inte detta läkemedel efter utgångsdatum som anges på kartongen eller blistret. Utgångsdatumet avser den sista dagen i månaden.
- Detta läkemedel kräver inga lagringstemperaturer.
- Kasta inga läkemedel i avloppsvatten eller hushållsavfall. Fråga din apotekare om hur du ska kasta läkemedel som du inte använder längre. Detta skyddar miljön.
Deadline "> Annan information
Vad Atacand innehåller
Den aktiva ingrediensen är candesartan cilexetil. Tabletterna innehåller 4 mg, 8 mg, 16 mg eller 32 mg kandesartancilexetil.
Övriga innehållsämnen är kalciumkarmellos, hydroxipropylcellulosa, laktosmonohydrat, magnesiumstearat, majsstärkelse, makrogol. 8 mg, 16 mg och 32 mg tabletterna innehåller också järnoxid (E172).
Beskrivning av hur Atacand ser ut och förpackningens innehåll
- Tabletterna på 4 mg är vita, runda med en mållinje och präglade med A / CF på ena sidan och 004 på den andra.
- 8 mg tabletterna är blekrosa, runda med en mållinje och präglade med A / CG på ena sidan och 008 på den andra.
- 16 mg tabletterna är rosa, runda med en mållinje och präglade med A / CH på ena sidan och 016 på den andra.
- 32 mg tabletterna är rosa, runda med en mållinje och präglade med A / CL på ena sidan och 032 på den andra.
Tabletten kan delas upp i lika stora halvor genom att klippa längs mållinjen.
Tabletterna finns i plastflaskor innehållande 100 eller 250 tabletter eller i blister med 7, 14, 15, 15x1, 20, 28, 30, 30x1, 50, 50x1, 56, 90, 98, 98x1, 100 eller 300 tabletter.
Alla förpackningsstorlekar kanske inte marknadsförs i alla länder.
Bipacksedel: AIFA (Italian Medicines Agency). Innehåll publicerat i januari 2016. Den information som finns finns kanske inte uppdaterad.
För att få tillgång till den senaste versionen är det lämpligt att gå till AIFA (Italian Medicines Agency) webbplats. Ansvarsfriskrivning och användbar information.
01.0 LÄKEMEDLETS NAMN -
RATACAND -TABLETTER
02.0 KVALITATIV OCH KVANTITATIV SAMMANSÄTTNING -
4 mg: varje tablett innehåller 4 mg candesartan cilexetil.
8 mg: varje tablett innehåller 8 mg candesartan cilexetil.
16 mg: varje tablett innehåller 16 mg candesartan cilexetil.
32 mg: varje tablett innehåller 32 mg candesartan cilexetil.
Hjälpämnen:
4 mg: varje tablett innehåller 93,4 mg laktosmonohydrat.
8 mg: varje tablett innehåller 89,4 mg laktosmonohydrat.
16 mg: varje tablett innehåller 81,4 mg laktosmonohydrat.
32 mg: varje tablett innehåller 163 mg laktosmonohydrat.
För fullständig förteckning över hjälpämnen, se avsnitt 6.1.
03.0 LÄKEMEDELSFORM -
Läsplatta.
4 mg: vita, runda tabletter (diameter 7 mm) med en strecklinje och präglade med A / CF på ena sidan och 004 på den andra.
8 mg: ljusrosa, runda tabletter (diameter 7 mm) med en strecklinje och präglade med A / CG på ena sidan och 008 på den andra.
16 mg: rosa, runda tabletter (diameter 7 mm) med en strecklinje och präglad med A / CH på ena sidan och 016 på den andra.
32 mg: rosa, runda tabletter (9,5 mm diameter) med en strecklinje och präglad med A / CL på ena sidan och 032 på den andra.
Tabletten kan delas i lika stora halvor.
04.0 KLINISK INFORMATION -
04.1 Terapeutiska indikationer -
Atacand är indicerat för:
Behandling av essentiell hypertoni hos vuxna.
Behandling av vuxna patienter med hjärtsvikt och nedsatt systolisk funktion i vänster kammare (fraktion av vänster kammare ≤ 40%) utöver behandling med Angiotensin Converting Enzyme (ACE) -hämmare eller när ACE -hämmare inte tolereras (se avsnitt 5.1).
04.2 Dosering och administreringssätt -
Dosering vid högt blodtryck
Den rekommenderade startdosen och den vanliga underhållsdosen av Atacand är 8 mg en gång om dagen. Det mesta av den blodtryckssänkande effekten uppnås inom 4 veckor. Hos vissa patienter vars blodtryck inte är tillräckligt kontrollerat kan dosen ökas upp till 16 mg en gång dagligen och upp till högst 32 mg en gång dagligen. Behandlingen bör anpassas enligt blodtryckssvar.Atacand kan också administreras med andra antihypertensiva medel.Tillsatsen av hydroklortiazid har visat en ytterligare antihypertensiv effekt med olika doser av Atacand.
Äldre befolkning
Ingen initial dosjustering är nödvändig hos äldre patienter.
Patienter med intravaskulär volymutarmning
Hos patienter med risk för hypotoni, till exempel patienter med eventuell intravaskulär volymutarmning, kan en startdos på 4 mg övervägas (se avsnitt 4.4).
Patienter med nedsatt njurfunktion
Hos patienter med nedsatt njurfunktion är startdosen 4 mg, inklusive patienter i hemodialys. Dosen ska titreras baserat på svaret. Erfarenhet hos patienter med mycket allvarlig njurinsufficiens eller slutskede (Clcreatinine
Patienter med nedsatt leverfunktion
En startdos på 4 mg en gång dagligen rekommenderas till patienter med lätt till måttligt nedsatt leverfunktion. Dosen kan justeras baserat på svaret. Atacand är kontraindicerat hos patienter med allvarligt nedsatt leverfunktion och / eller kolestas (se avsnitt 4.3 och 5.2).
Svarta patienter
Den antihypertensiva effekten av candesartan är mindre uttalad hos svarta patienter än hos icke-svarta patienter. Därför kan ökade doser av Atacand och tillägg av samtidig behandling behövas oftare för blodtryckskontroll hos patienter. Svart jämfört med icke-svarta (se avsnitt 5.1).
Dosering vid hjärtsvikt
Den vanliga rekommenderade startdosen av Atacand är 4 mg en gång dagligen. Titrering till måldosen 32 mg en gång dagligen (maximal dos) eller till den högsta tolererade dosen görs genom att fördubbla dosen med minst 2 veckors intervall (se avsnitt 4.4). Utvärdering av patienter med hjärtsvikt bör alltid inkludera övervakning av njurfunktionen, inklusive serumkreatinin och kalium.
Atacand kan ges tillsammans med andra behandlingar för hjärtsvikt, inklusive ACE-hämmare, betablockerare, diuretika och digitalis eller en kombination av dessa läkemedel. Kombinationen av en ACE-hämmare, ett kaliumsparande diuretikum (t.ex.
Särskilda patientpopulationer
Ingen initial dosjustering är nödvändig hos äldre patienter eller hos patienter med intravaskulär volymutarmning, nedsatt njurfunktion eller lätt till måttligt nedsatt leverfunktion.
Pediatrisk population
Atacands säkerhet och effekt hos barn från födsel till 18 år har inte fastställts vid behandling av högt blodtryck och hjärtsvikt. Inga data finns tillgängliga.
Administreringssätt
Oral användning
Atacand ska administreras en gång dagligen med eller utan mat.
Biotillgängligheten för candesartan påverkas inte av mat.
04.3 Kontraindikationer -
Överkänslighet mot candesartan cilexetil eller mot något hjälpämne.
Andra och tredje trimestern av graviditeten (se avsnitt 4.4 och 4.6).
Allvarlig leverinsufficiens och / eller kolestas.
04.4 Varningar och lämpliga försiktighetsåtgärder vid användning -
Förändrad njurfunktion
Liksom med andra medel som hämmar renin-angiotensin-aldosteronsystemet kan förändringar i njurfunktionen förväntas hos mottagliga patienter som behandlas med Atacand.
Periodisk övervakning av serumkalium- och kreatininnivåer rekommenderas när Atacand används hos hypertensiva patienter med nedsatt njurfunktion. Erfarenheten är begränsad hos patienter med mycket allvarligt eller nedsatt njurfunktion (Clcreatinine-blodtrycksövervakning.
Utvärdering av patienter med hjärtsvikt bör inkludera periodiska bedömningar av njurfunktionen, särskilt hos äldre patienter 75 år eller äldre, och hos patienter med nedsatt njurfunktion. Under dostitrering av Atacand rekommenderas serumkreatinin- och kaliumkoncentrationer i serum. Kliniska prövningar av hjärtsvikt inkluderade inte patienter med serumkreatinin> 265 μmol / L (> 3 mg / dL).
Samtidig behandling med ACE -hämmare vid hjärtsvikt
Risken för biverkningar, särskilt nedsatt njurfunktion och hyperkalemi, kan öka när Atacand ges i kombination med en ACE -hämmare (se avsnitt 4.8). Patienter som genomgår denna behandling bör övervakas regelbundet och noggrant.
Hemodialys
Under dialys kan blodtrycket vara särskilt känsligt för AT1-receptorblockad till följd av minskad plasmavolym och aktivering av renin-angiotensin-aldosteronsystemet. Därför bör Atacand doseras noggrant genom att övervaka blodtrycket hos hemodialyspatienter.
Njurartärstenos
Läkemedel som påverkar renin-angiotensin-aldosteronsystemet, inklusive angiotensin II-receptorantagonister (AIIRA), kan öka ureakväve och kreatinin i blodet hos patienter med bilateral njurartärstenos eller renal artärstenos i närvaro av en enda njure.
Njurtransplantation
Det finns ingen erfarenhet av användning av Atacand hos patienter som nyligen har genomgått njurtransplantation.
Hypotoni
Hypotoni kan uppstå under behandling med Atacand hos patienter med hjärtsvikt. Detta kan också inträffa hos hypertensiva patienter med intravaskulär volymutarmning, såsom de som tar högdosdiuretika. Försiktighet bör iakttas när behandling påbörjas och försök bör göras för att korrigera hypovolemi.
Bedövning och operation
Hypotoni på grund av blockad av renin-angiotensinsystemet kan uppstå under anestesi och kirurgi hos patienter som behandlas med angiotensin II-antagonister. Mycket sällan kan hypotoni vara så allvarlig att det motiverar användning av intravenösa vätskor och / eller vasopressorsubstanser.
Aorta- och mitralstenos (obstruktiv hypertrofisk kardiomyopati)
Precis som med andra vasodilatatorer rekommenderas särskild försiktighet hos patienter med hemodynamiskt relevant aorta- eller mitralstenos eller hypertrofisk obstruktiv kardiomyopati.
Primär hyperaldosteronism
Patienter med primär aldosteronism svarar i allmänhet inte på antihypertensiva läkemedel som verkar genom att hämma renin-angiotensin-aldosteronsystemet. Därför rekommenderas inte användning av Atacand i denna population.
Hyperkalemi
Samtidig användning av Atacand med kaliumsparande diuretika, kaliumtillskott, kaliuminnehållande saltsubstitut eller andra läkemedel som kan öka kalium (t.ex. heparin) kan orsaka serumkaliumhöjningar hos hypertensiva patienter. Serumkaliumnivåer bör utföras vid behov.
Hos patienter med hjärtsvikt som behandlas med Atacand kan hyperkalemi uppstå. Periodisk övervakning av serumkaliumnivåer rekommenderas. Kombinationen av en ACE-hämmare, ett kaliumbesparande diuretikum (t.ex.
Allmänna aspekter
Hos patienter vars kärlton och njurfunktion huvudsakligen är beroende av aktiviteten hos renin-angiotensin-aldosteronsystemet (t.ex. patienter med allvarlig hjärtsvikt eller med underliggande njursjukdom inklusive njurartärstenos), har behandlingen associerats med akut hypotoni, azotaemi, oliguri eller sällan akut njursvikt med andra läkemedel som påverkar detta system. Möjligheten till liknande effekter kan inte uteslutas med användning av AIIRA. Liksom med andra antihypertensiva läkemedel kan överdriven blodtryckssänkning hos patienter med ischemisk hjärtsjukdom eller ischemisk cerebrovaskulär sjukdom leda till hjärtinfarkt eller stroke.
Den antihypertensiva effekten av candesartan kan förstärkas av andra läkemedel med hypotensiva egenskaper, antingen förskrivna som antihypertensiva eller för andra indikationer.
Atacand innehåller laktos. Patienter med sällsynta ärftliga problem med galaktosintolerans, Lapp-laktasbrist eller glukos-galaktosmalabsorptionssyndrom bör inte ta detta läkemedel.
Graviditet
Angiotensin II -receptorantagonistbehandling (AIIRA) ska inte påbörjas under graviditet.
För patienter som planerar graviditet bör alternativa blodtryckssänkande behandlingar med en beprövad säkerhetsprofil för graviditet användas, såvida inte fortsatt behandling med AIIRA anses vara nödvändig. behandlingen bör startas (se avsnitt 4.3 och 4.6).
04.5 Interaktioner med andra läkemedel och andra former av interaktion -
Föreningar som har testats i kliniska farmakokinetiska studier inkluderar hydroklortiazid, warfarin, digoxin, orala preventivmedel (etinylestradiol / levonorgestrel), glibenklamid, nifedipin och enalapril. Inga kliniskt relevanta farmakokinetiska interaktioner med andra läkemedel har identifierats.
Samtidig användning av kaliumsparande diuretika, kaliumtillskott, kaliuminnehållande saltsubstitut eller andra läkemedel (t.ex. heparin) kan öka kalium. Om så är lämpligt kan övervakning av kalium övervägas (se avsnitt 4.4).
Reversibla ökningar i serum litiumkoncentrationer och toxiska reaktioner har rapporterats vid samtidig administrering av litium med ACE -hämmare. En liknande effekt kan uppstå med AIIRA. Användning av candesartan med litium rekommenderas inte. Om kombinationen visar sig nödvändig rekommenderas noggrann övervakning av serum litiumhalter.
När AIIRA administreras samtidigt med icke-steroida antiinflammatoriska läkemedel (NSAID) (t.ex. selektiva COX-2-hämmare, acetylsalicylsyra (> 3 g / dag) och icke-selektiva NSAID) kan "dämpning av den antihypertensiva effekten" uppstå.
Liksom med ACE-hämmare kan samtidig användning av AIIRA och NSAID leda till en ökad risk för försämrad njurfunktion inklusive eventuellt akut njursvikt och ökade serumkaliumnivåer, särskilt hos patienter med redan nedsatt njurfunktion. Kombinationen ska administreras med försiktighet, särskilt hos äldre. Patienterna bör hydratiseras tillräckligt och övervakning av njurfunktionen bör övervägas vid samtidig behandling och därefter regelbundet.
04.6 Graviditet och amning -
Graviditet
Användning av Angiotensin II -receptorantagonister (AIIRA) rekommenderas inte under graviditetens första trimester (se avsnitt 4.4). Användning av AIIRA är kontraindicerat under andra och tredje trimestern av graviditeten (se avsnitt 4.3 och 4.4).
Epidemiologiska bevis på risken för teratogenicitet efter exponering för ACE -hämmare under graviditetens första trimester har inte varit avgörande. en liten riskökning kan dock inte uteslutas. Även om kontrollerade epidemiologiska data om risken för Angiotensin II -receptorantagonister (AIIRA) inte finns tillgängliga, kan en liknande risk också finnas för denna klass av läkemedel. Beprövad säkerhetsprofil för användning under graviditet om inte fortsatt behandling med AIIRA anses vara avgörande.När graviditet diagnostiserats ska behandlingen med AIIRA avbrytas omedelbart och, om lämpligt, alternativ behandling påbörjas.
Exponering för AIIRA under andra och tredje trimestern är känd för att orsaka fostertoxicitet (nedsatt njurfunktion, oligohydramnios, retardation av skalleförbening) och neonatal toxicitet (njursvikt, hypotoni, hyperkalemi) hos kvinnor (se avsnitt 5.3).
Om exponering för AIIRA har inträffat från graviditetens andra trimester rekommenderas ultraljudskontroll av njurfunktion och skalle.
Nyfödda vars mödrar har tagit AIIRA bör övervakas noga med avseende på hypotoni (se avsnitt 4.3 och 4.4).
Matdags
Eftersom inga data finns tillgängliga om användning av Atacand under amning, rekommenderas inte Atacand och alternativa behandlingar med en beprövad säkerhetsprofil för användning under amning föredras, särskilt när man ammar ett nyfött eller prematur barn.
04.7 Effekter på förmågan att framföra fordon och använda maskiner -
Inga studier har gjorts om kandesartans effekter på förmågan att framföra fordon och använda maskiner. Det bör dock beaktas att yrsel eller trötthet ibland kan uppstå under behandling med Atacand.
04.8 Biverkningar -
Behandling av högt blodtryck
I kontrollerade kliniska prövningar var biverkningarna milda och övergående. Den totala förekomsten av biverkningar visade ingen korrelation med dos eller ålder. Avbrytande av behandlingen på grund av biverkningar var liknande med candesartan cilexetil (3,1%) och placebo (3,2%).
Från en samlad analys av data från kliniska prövningar med hypertensiva patienter definierades biverkningar med candesartancilexetil baserat på förekomsten av biverkningar med candesartancilexetil minst 1% högre än incidensen som observerades med placebo. Baserat på denna definition var de vanligaste rapporterade biverkningarna yrsel / yrsel, huvudvärk och luftvägsinfektioner.
Tabellen nedan visar biverkningar som rapporterats från kliniska studier och erfarenheter efter marknadsföring.
Frekvenserna i tabellerna i avsnitt 4.8 är: mycket vanliga (≥ 1/10), vanliga (≥1 / 100a
Laboratorietester
Det fanns i allmänhet inga kliniskt relevanta effekter av Atacand på rutinmässiga laboratorieparametrar. Liksom med andra hämmare av renin-angiotensin-aldosteronsystemet har en liten minskning av hemoglobin observerats. Ingen rutinmässig laboratorieövervakning krävs vanligtvis hos patienter som behandlas med Atacand, men för patienter med nedsatt njurfunktion rekommenderas det att regelbundet kontrollera serumkalium och kreatininnivåer.
Behandling av hjärtsvikt
Atacands toleransprofil observerad hos patienter med hjärtsvikt överensstämde med läkemedelsfarmakologi och patienternas hälsotillstånd. I det kliniska CHARM -programmet, som jämförde Atacand vid doser upp till 32 mg (n = 3 803) med placebo (n = 3 766), avbröt 21,0% av kandesartancilexetilgruppen och 16,1% av placebogruppen behandlingen på grund av biverkningar. De vanligaste rapporterade biverkningarna var hyperkalemi, hypotoni, nedsatt njurfunktion.
Dessa händelser var vanligare hos patienter över 70 år, diabetiker eller de som hade fått andra läkemedel som påverkar renin-angiotensin-aldosteronsystemet, särskilt en ACE-hämmare och / eller spironolakton.
Tabellen nedan visar biverkningar som rapporterats från kliniska studier och erfarenheter efter marknadsföring.
Laboratorietester
Hyperkalemi och nedsatt njurfunktion är vanliga hos patienter som behandlas med Atacand för indikation på hjärtsvikt. Periodisk övervakning av serumkreatinin- och kaliumkoncentrationer rekommenderas (se avsnitt 4.4).
04.9 Överdosering -
Symtom
Baserat på farmakologiska överväganden bör överdosens huvudsakliga manifestation vara symtomatisk hypotoni och yrsel. I enskilda rapporter om överdosering (upp till 672 mg kandesartancilexetil) återhämtade sig patienten utan konsekvenser.
Metoder för intervention vid överdosering
Om symtomatisk hypotoni inträffar, bör symptomatisk behandling sättas in och vitala funktioner övervakas. Patienten ska placeras i ryggläge med benen upphöjda. Om detta inte är tillräckligt bör plasmavolymen ökas genom infusion, till exempel av isoton saltlösning. Sympatomimetiska läkemedel kan administreras om åtgärderna ovan är otillräckliga.
Candesartan avlägsnas inte genom hemodialys.
05.0 FARMAKOLOGISKA EGENSKAPER -
05.1 "Farmakodynamiska egenskaper -
Farmakoterapeutisk kategori: angiotensin II-antagonister, oberoende.
ATC -kod: C09CA06.
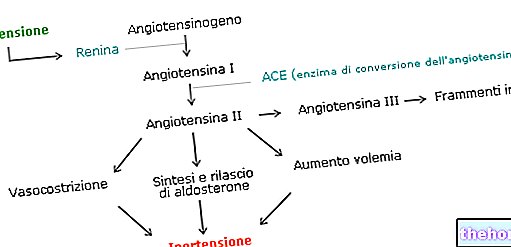
Angiotensin II är det huvudsakliga vasoaktiva hormonet i renin-angiotensin-aldosteronsystemet och spelar en roll i patofysiologin för högt blodtryck, hjärtsvikt och andra kardiovaskulära sjukdomar. Det spelar också en roll vid patogenesen av "hypertrofi och skada" Den stora fysiologiska effekter av angiotensin II, såsom vasokonstriktion, stimulering av aldosteron, reglering av salt- och vattenbalans och stimulering av celltillväxt, medieras genom typ 1 -receptorn (AT1).
Candesartan cilexetil är ett pro-läkemedel för oral användning. Det omvandlas snabbt till den aktiva substansen, candesartan, genom esterhydrolys under absorption från mag -tarmkanalen. Candesartan är en AIIRA -selektiv för AT1 -receptorer, med nära bindningsaffinitet och långsam dissociation från receptorn. Han har ingen tävlingsverksamhet.
Candesartan hämmar inte ACE, som omvandlar angiotensin I till angiotensin II och bryter ned bradykinin. Det finns ingen effekt på ACE och ingen förstärkning av bradykinin eller substans P. I kontrollerade kliniska prövningar där candesartan jämfördes med ACE -hämmare var förekomsten av hosta lägre hos patienter som behandlades med candesartancilexetil. Candesartan binder inte eller blockerar andra hormonreceptorer eller jonkanaler som är viktiga för att reglera det kardiovaskulära systemet. Angiotensin II-receptor (AT1) -antagonism resulterar i dosrelaterade ökningar i plasmareninnivåer, angiotensin I-nivåer och angiotensin II, och med en minskning av plasmakoncentrationer av aldosteron.
Hypertoni
Vid högt blodtryck orsakar candesartan en dosberoende, långvarig sänkning av blodtrycket.Den antihypertensiva effekten beror på minskningen av perifert systemiskt motstånd, utan reflexhöjningar i hjärtfrekvensen. Inga allvarliga eller överdrivna effekter av första dosens hypotoni eller effekt observerades "studs" efter avslutad behandling.
Efter administrering av en engångsdos candesartancilexetil inträffar vanligtvis antihypertensiv effekt inom 2 timmar. Efter kontinuerlig behandling uppnås i allmänhet maximal sänkning av blodtrycket med vilken dos som helst inom 4 veckor och bibehålls under långtidsbehandling.
Enligt en metaanalys hade en ökning av dosen från 16 mg till 32 mg en gång dagligen i genomsnitt en liten ytterligare effekt, med hänsyn tagen till den individuella variationen kan en större effekt av dosen förväntas hos vissa patienter. genomsnitt.
Candesartan cilexetil administrerat en gång dagligen orsakar en effektiv och homogen minskning av blodtrycket under 24 timmar med en liten skillnad i förhållandet mellan dal och topp under intervallet mellan doserna. Den antihypertensiva effekten och toleransen för candesartan och losartan jämfördes i två randomiserade dubbelblinda kliniska prövningar med totalt 1 268 patienter med lätt till måttlig högt blodtryck. 32 mg administrerat en gång dagligen och 10,0 / 8,7 mmHg med losartankalium 100 mg administrerat en gång dagligen (skillnad i blodtrycksreduktion 3,1 / 1,8 mmHg, p
När candesartan cilexetil kombineras med hydroklortiazid sker en additiv sänkning av blodtrycket.En ökning av den antihypertensiva effekten observeras också när candesartan cilexetil används i kombination med amlodipin eller felodipin.
Läkemedel som blockerar renin-angiotensin-aldosteronsystemet har en mindre uttalad antihypertensiv effekt hos svarta patienter (vanligtvis låg-reninpopulation) än hos icke-svarta patienter. Detta inträffar också när det gäller candesartan. I en öppen klinisk studie av 5 156 patienter med diastolisk hypertoni var minskningen av blodtrycket under behandling med candesartan signifikant mindre hos svarta patienter än hos icke-svarta (14,4 / 10,3 mmHg vs 19,0 / 12,7 mmHg, p
Candesartan ökar njurflödet och har ingen effekt eller ökar glomerulär filtrationshastighet, samtidigt som det reducerar njurkärlsmotståndet och filtreringsfraktionen. I en 3-månaders klinisk studie på hypertensiva patienter med typ 2-diabetes mellitus och mikroalbuminuri reducerade antihypertensiv behandling med candesartancilexetil urinalbuminutsöndring (genomsnittlig minskning av albumin / kreatininförhållande med 30%, 95%KI 15-42%). Det finns för närvarande inga data om effekten av candesartan på progression till diabetisk nefropati.
Effekterna av kandesartancilexetil 8-16 mg (genomsnittlig dos 12 mg), en gång dagligen, på kardiovaskulär sjuklighet och dödlighet utvärderades i en randomiserad klinisk prövning på 4 937 äldre patienter (70-89 år, varav 21% i åldern 80 år eller äldre) med mild till måttlig högt blodtryck följt i genomsnitt 3,7 år (studie om COgnition and Prognosis hos äldre). Patienterna fick candesartan cilexetil eller placebo med andra ytterligare blodtryckssänkande behandlingar efter behov. Blodtrycket sänktes från 166/90 till 145/80 mmHg i candesartangruppen och från 167/90 till 149/82 mmHg i kontrollgruppen. Det fanns ingen statistiskt signifikant skillnad i den primära slutpunkten, större kardiovaskulära händelser (kardiovaskulär dödlighet, icke-dödlig stroke och icke-dödligt hjärtinfarkt). Det fanns 26,7 händelser per 1000 patientår i candesartangruppen mot 30,0 händelser per 1000 patientår i kontrollgruppen (relativ risk 0,89, 95% KI 0,75 till 1,06, p = 0,19).
Hjärtsvikt
Behandling med candesartancilexetil minskar dödligheten, minskar sjukhusvistelse på grund av hjärtsvikt och förbättrar symtom hos patienter med systolisk dysfunktion i vänster kammare, vilket visas i Candesartan vid hjärtsvikt - utvärdering av minskning av dödlighet och morbiditet (CHARM).
Detta dubbelblinda, placebokontrollerade studieprogram hos patienter med kronisk hjärtsvikt (CHF) NYHA funktionell klass II till IV bestod av tre separata studier:
CHARM-alternativ (n = 2.028) hos patienter med fraktion av vänster kammare (LVEF) ≤ 40% som inte behandlas med ACE-hämmare på grund av intolerans (främst på grund av hosta, 72%), CHARM-tillförd (n = 2548) hos patienter med LVEF ≤ 40% och behandlas med en ACE-hämmare och CHARM-bevarad (n = 3023) hos patienter med LVEF> 40%. Patienter på optimal bakgrundsterapi för hjärtsvikt (CHF) randomiserades till placebo eller candesartan cilexetil (titrerades från 4 mg eller 8 mg en gång dagligen upp till 32 mg en gång dagligen eller den högsta tolererade dosen., Genomsnittlig dos 24 mg) och följdes efter en median på 37,7 månader. Efter 6 månaders behandling hade 63% av patienterna som fortfarande tog candesartan cilexetil (89%) nått måldosen 32 mg.
I den CHARM-alternativa studien minskade den kombinerade slutpunkten för kardiovaskulär dödlighet eller första sjukhusvistelse för CHF signifikant med candesartan jämfört med placebo, riskförhållande (HR) 0,77 (95% KI: 0,67 till 0, 89, kardiovaskulär eller sjukhusvistelse för behandlingen av hjärtsvikt.
Den kombinerade slutpunkten för dödlighet av alla orsaker eller första sjukhusvistelse för CHF minskade också signifikant med candesartan HR 0,80 (95% KI: 0,70 till 0,92, p = 0,001). Av patienter behandlade med candesartan var 36,6% (95% KI: 33,7 till 39,7) och för patienter som behandlades med placebo, hade 42,7% (95% KI: 39,6 till 45,8) nått denna slutpunkt, absolut skillnad 6,0% (95% KI: 10,3 till 1,8).
Både dödlighet och sjuklighet (sjukhusvistelse för CHF), båda komponenterna i dessa kombinerade slutpunkter, bidrog till de gynnsamma effekterna av candesartan. Behandling med candesartan cilexetil resulterade i en förbättring av funktionsklassen NYHA (p = 0,008).
I den CHARM-tillagda studien minskade den kombinerade slutpunkten för kardiovaskulär dödlighet eller första sjukhusvistelse för CHF signifikant med candesartan jämfört med placebo HR 0,85 (95% KI: 0,75 till 0,96, p = 0,011) Detta motsvarar en relativ riskreduktion på 15 Av candesartanbehandlade patienter uppfyllde 37,9% (95% KI: 35,2 till 40,6) och av placebobehandlade patienter 42,3% (95% KI: 39,6 till 45,1) detta slutpunkt, absolut skillnad 4,4% (95% KI: 8,2 till 0,6). 23 patienter måste behandlas under studiens varaktighet för att förhindra dödsfall från kardiovaskulära händelser eller sjukhusvistelse för behandling av hjärtsvikt hos en patient. Den kombinerade slutpunkten för dödlighet av alla orsaker eller första sjukhusvistelse för CHF minskade också signifikant med candesartan HR 0,87 (95% KI: 0,78 till 0,98, p = 0,021). Candesartanbehandlade patienter, 42,2% (95% KI: 39,5 till 45,0) och för placebobehandlade patienter, 46,1% (95% KI: 43,4 till 48,9) uppnådde detta slutpunkt, absolut skillnad 3,9% (95% KI: 7,8 till 0,1) Både dödlighet och sjuklighet, båda komponenterna i dessa kombinerade slutpunkter, bidrog till candesartans gynnsamma effekter.Behandling med candesartan cilexetil resulterade i en förbättring av funktionsklassen NYHA (p = 0,020).
I den CHARM-bevarade studien erhölls ingen statistiskt signifikant minskning av den kombinerade slutpunkten för kardiovaskulär dödlighet eller första sjukhusvistelse för CHF, HR 0,89, (95% CI: 0,77 till 1,03, p = 0,118).
Alla dödsorsaker var inte statistiskt signifikanta när de undersöktes separat för var och en av de tre CHARM -studierna. Dödligheten av alla orsaker bedömdes dock också i poolade populationer, i CHARM-alternativa och CHARM-tillagda studier, HR 0,88, (95% KI: 0,79 till 0,98, p = 0,018) och i alla tre studierna, HR 0,91 (95% CI: 0,83 till 1,00, p = 0,55).
De fördelaktiga effekterna av candesartan var konsekventa oavsett ålder, kön och samtidig medicinering. Candesartan var också effektivt hos patienter som tog både betablockerare och ACE-hämmare samtidigt, och fördelen uppnåddes om patienterna tog ACE-hämmare i den dos som rekommenderas av behandlingsriktlinjerna.
Hos patienter med CHF och nedsatt systolisk funktion i vänster kammare (utkastningsfraktion vänster kammare, LVEF ≤40%) minskar candesartan systemiskt kärlresistens och pulmonalt kapillärt kiltryck, ökar plasma reninaktivitet och blodkoncentration. Angiotensin II och sänker aldosteronnivåerna.
05.2 "Farmakokinetiska egenskaper -
Absorption och distribution
Efter oral administrering omvandlas candesartan cilexetil till den aktiva substansen candesartan. Den absoluta biotillgängligheten för candesartan är cirka 40% efter administrering av en oral lösning av candesartan cilexetil. Den relativa biotillgängligheten för tablettformuleringen jämfört med samma orala lösning är cirka 34% med mycket liten variation. Den beräknade absoluta biotillgängligheten för tabletten är därför 14%. Medelvärden för maximal koncentration (Cmax) uppnås inom 3-4 timmar efter dosering. Serumkoncentrationerna av kandesartan ökar linjärt med ökande doser inom det terapeutiska området. Inga skillnader i kandesartans farmakokinetik observerades för båda könen. Området under kurvan (AUC) påverkas inte signifikant av mat.
Candesartan är starkt bundet till plasmaproteiner (mer än 99%). Den uppenbara distributionsvolymen för candesartan är 0,1 L / kg.
Biotillgängligheten för candesartan påverkas inte av mat.
Biotransformation och eliminering
Candesartan elimineras nästan helt oförändrat via urin- och gallvägarna och endast i mindre utsträckning via levermetabolism (CYP2C9). Tillgängliga interaktionsstudier indikerar ingen effekt på CYP2C9 och CYP3A4. Baserat på data in vitro, förväntas ingen interaktion inträffa in vivo med läkemedel vars metabolism beror på cytokrom P450, CYP1A2, CYP2A6, CYP2C9, CYP2C19, CYP2D6, CYP2E1 eller CYP3A4 isoenzymer. Den terminala halveringstiden är cirka 9 timmar. Ingen ackumulering observeras efter upprepad dosering.
Den totala plasmaclearance för candesartan är cirka 0,37 ml / min / kg, med en renal clearance på cirka 0,19 ml / min / kg. Renal utsöndring sker genom både glomerulär filtrering och aktiv tubulär utsöndring. Efter en oral dos av 14C-märkt candesartancilexetil utsöndras cirka 26% av dosen i urinen som candesartan och 7% som en inaktiv metabolit, medan cirka 56% av dos finns i avföringen som kandesartan och 10% som den inaktiva metaboliten.
Farmakokinetik i speciella populationer
Hos äldre (över 65 år) ökar både Cmax och AUC för candesartan med cirka 50% respektive 80%, jämfört med unga försökspersoner. Blodtryckssvaret och förekomsten av biverkningar är dock liknande efter administrering av samma dos Atacand till unga och äldre patienter (se avsnitt 4.2).
Hos patienter med lätt till måttligt nedsatt njurfunktion ökade Cmax och AUC för candesartan vid upprepad administrering med cirka 50% respektive 70%, men t½ förändrades inte jämfört med patienter med normal njurfunktion. Motsvarande förändringar hos patienter med svår njurinsufficiens var cirka 50% och 110%. Den terminala t½ kandesartan fördubblades ungefär hos patienter med allvarligt nedsatt njurfunktion. AUC för kandesartan hos hemodialyspatienter var liknande den hos patienter med allvarligt nedsatt njurfunktion.
I två studier, både hos patienter med lätt till måttligt nedsatt leverfunktion, var det en ökning av genomsnittlig AUC för Candesartan med cirka 20% i den ena studien och 80% i den andra studien (se avsnitt 4.2). Erfarenhet av patienter med allvarligt nedsatt leverfunktion.
05.3 Prekliniska säkerhetsdata -
Ingen onormal systemisk eller organtoxicitet observerades vid kliniskt relevanta doser. I prekliniska säkerhetsstudier hade candesartan effekter på parametrar för njurar och röda blodkroppar vid höga doser hos möss, råttor, hundar och apor. Candesartan orsakade en minskning av parametrar för röda blodkroppar (erytrocyter, hemoglobin, hematokrit). Effekter på njurarna (såsom interstitiell nefrit, tubulär distension, tubulär basofili, ökade plasmakoncentrationer av BUN och kreatinin) inducerades av candesartan och kan vara sekundära till den hypotensiva effekten som leder till nedsatt njurperfusion. Vidare inducerade candesartan hyperplasi / hypertrofi av juxtaglomerulära celler Dessa förändringar ansågs orsakas av candesartans farmakologiska verkan. Med terapeutiska doser av kandesartan hos människor verkar hyperplasi / hypertrofi av juxtaglomerulära celler inte ha någon relevans.
Foetotoxicitet har observerats i slutet av graviditeten (se avsnitt 4.6).
Uppgifterna om mutagenes in vitro och in vivo indikerar att kandesartan inte utövar mutagen eller klastogen aktivitet under klinisk användning.
Inga cancerframkallande fenomen observerades.
06.0 LÄKEMEDELSINFORMATION -
06.1 Hjälpämnen -
Kalciumkarmellos
Hydroxipropylcellulosa
Järnoxid, CI 77491 (E172) (endast för 8 mg, 16 mg och 32 mg tabletter)
Laktosmonohydrat
Magnesiumstearat
Majsstärkelse
Makrogol
06.2 Inkompatibilitet "-
Inte relevant.
06.3 Giltighetstid "-
3 år.
06.4 Särskilda förvaringsanvisningar -
Detta läkemedel kräver inga speciella förvaringstemperaturer.
06.5 Förpackningens innehåll och förpackningens innehåll -
PVC / PVDC -blister med 7, 14, 15, 15x1 (engångsdos), 20, 28, 30, 30x1 (endos), 50, 50x1 (endos), 56, 90, 98, 98x1 (endos), 100 och 300 tabletter.
HDPE -flaskor innehållande 100 och 250 tabletter
Alla förpackningsstorlekar kanske inte marknadsförs.
06.6 Anvisningar för användning och hantering -
Inga speciella instruktioner.
07.0 INNEHAVARE AV "MARKNADSFÖRINGANDE GODKÄNNANDE" -
AstraZeneca S.p.A. - Palazzo Ferraris, via Ludovico il Moro 6 / C - Basiglio (MI) 20080
08.0 NUMMER FÖR FÖRSÄLJNINGSTILLSTÅND -
Blisterförpackningar :
4 mg tabletter - 7 tabletter i PVC / PVDC -blister - AIC n. 033577038
4 mg tabletter - 14 tabletter i PVC / PVDC -blister - AIC n. 033577040
4 mg tabletter - 15 tabletter i PVC / PVDC -blister - AIC n. 033577584
4 mg tabletter - 15x1 tabletter i PVC / PVDC -blister - AIC n. 033577634
4 mg tabletter - 20 tabletter i PVC / PVDC -blister - AIC n. 033577053
4 mg tabletter - 28 tabletter i PVC / PVDC -blister - AIC n. 033577065
4 mg tabletter - 30 tabletter i PVC / PVDC -blister - AIC n. 033577572
4 mg tabletter - 30x1 tabletter i PVC / PVDC -blister - AIC n. 033577646
4 mg tabletter - 50 tabletter i PVC / PVDC -blister - AIC n. 033577077
4 mg tabletter - 50x1 tabletter i PVC / PVDC -blister - AIC n. 033577394
4 mg tabletter - 56 tabletter i PVC / PVDC -blister - AIC n. 033577089
4 mg tabletter - 90 tabletter i PVC / PVDC -blister - AIC n. 033577711
4 mg tabletter - 98 tabletter i PVC / PVDC -blister - AIC n. 033577091
4 mg tabletter - 98x1 tabletter i PVC / PVDC -blister - AIC n. 033577103
4 mg tabletter - 100 tabletter i PVC / PVDC -blister - AIC n. 033577115
4 mg tabletter - 300 tabletter i PVC / PVDC -blister - AIC n. 033577127
Flaskförpackningar :
4 mg tabletter - 100 tabletter i HDPE -AIC -flaska n. 033577139
4 mg tabletter - 250 tabletter i HDPE -flaska - AIC n. 033577141
Blisterförpackningar :
8 mg tabletter - 7 tabletter i PVC / PVDC -blister - AIC n. 033577154
8 mg tabletter - 14 tabletter i PVC / PVDC -blister - AIC n. 033577166
8 mg tabletter - 15 tabletter i PVC / PVDC -blister - AIC n. 033577608
8 mg tabletter - 15x1 tabletter i PVC / PVDC -blister - AIC n. 033577659
8 mg tabletter - 20 tabletter i PVC / PVDC -blister - AIC n. 033577178
8 mg tabletter - 28 tabletter i PVC / PVDC -blister - AIC n. 033577180
8 mg tabletter - 30 tabletter i PVC / PVDC -blister - AIC n. 033577596
8 mg tabletter - 30x1 tabletter i PVC / PVDC -blister - AIC n. 033577661
8 mg tabletter - 50 tabletter i PVC / PVDC -blister - AIC n. 033577192
8 mg tabletter - 50x1 tabletter i PVC / PVDC -blister - AIC n. 033577406
8 mg tabletter - 56 tabletter i PVC / PVDC -blister - AIC n. 033577204
8 mg tabletter - 90 tabletter i PVC / PVDC -blister - AIC n. 033577723
8 mg tabletter - 98 tabletter i PVC / PVDC -blister - AIC n. 033577216
8 mg tabletter - 98x1 tabletter i PVC / PVDC -blister - AIC n. 033577228
8 mg tabletter - 100 tabletter i PVC / PVDC -blister - AIC n. 033577230
8 mg tabletter - 300 tabletter i PVC / PVDC -blister - AIC n. 033577242
Flaskförpackningar :
8 mg tabletter - 100 tabletter i HDPE -flaska - AIC n. 033577255
8 mg tabletter - 250 tabletter i HDPE -flaska - AIC n. 033577267
Blisterförpackningar :
16 mg tabletter - 7 tabletter i PVC / PVDC -blister - AIC n. 033577279
16 mg tabletter - 14 tabletter i PVC / PVDC -blister - AIC n. 033577281
16 mg tabletter - 15 tabletter i PVC / PVDC -blister - AIC n. 033577622
16 mg tabletter - 15x1 tabletter i PVC / PVDC -blister - AIC n. 033577673
16 mg tabletter - 20 tabletter i PVC / PVDC -blister - AIC n. 033577293
16 mg tabletter - 28 tabletter i PVC / PVDC -blister - AIC n. 033577305
16 mg tabletter - 30 tabletter i PVC / PVDC -blister - AIC n. 033577610
16 mg tabletter - 30x1 tabletter i PVC / PVDC -blister - AIC n. 033577685
16 mg tabletter - 50 tabletter i PVC / PVDC -blister - AIC n. 033577317
16 mg tabletter - 50x1 tabletter i PVC / PVDC -blister - AIC n. 033577418
16 mg tabletter - 56 tabletter i PVC / PVDC -blister - AIC n. 033577329
16 mg tabletter - 90 tabletter i PVC / PVDC -blister - AIC n. 033577735
16 mg tabletter - 98 tabletter i PVC / PVDC -blister - AIC n. 033577331
16 mg tabletter - 98x1 tabletter i PVC / PVDC -blister - AIC n. 033577343
16 mg tabletter - 100 tabletter i PVC / PVDC -blister - AIC n. 033577356
16 mg tabletter - 300 tabletter i PVC / PVDC -blister - AIC n. 033577368
Flaskförpackningar :
16 mg tabletter - 100 tabletter i HDPE -flaska - AIC n. 033577370
16 mg tabletter - 250 tabletter i HDPE -flaska - AIC n. 033577382
Blisterförpackningar :
32 mg tabletter - 7 tabletter i PVC / PVDC -blister - AIC n. 033577420
32 mg tabletter - 14 tabletter i PVC / PVDC -blister - AIC n. 033577432
32 mg tabletter - 15 tabletter i PVC / PVDC -blister - AIC n. 033577444
32 mg tabletter - 15x1 tabletter i PVC / PVDC -blister - AIC n. 033577697
32 mg tabletter - 20 tabletter i PVC / PVDC -blister - AIC n. 033577457
32 mg tabletter - 28 tabletter i PVC / PVDC -blister - AIC n. 033577469
32 mg tabletter - 30 tabletter i PVC / PVDC -blister - AIC n. 033577471
32 mg tabletter - 30x1 tabletter i PVC / PVDC -blister - AIC n. 033577709
32 mg tabletter - 50 tabletter i PVC / PVDC -blister - AIC n. 033577483
32 mg tabletter - 50x1 tabletter i PVC / PVDC -blister - AIC n. 033577495
32 mg tabletter - 56 tabletter i PVC / PVDC -blister - AIC n. 033577507
32 mg tabletter - 90 tabletter i PVC / PVDC -blister - AIC n. 033577747
32 mg tabletter - 98 tabletter - i PVC / PVDC AIC -blister n. 033577519
32 mg tabletter - 98x1 tabletter i PVC / PVDC -blister - AIC n. 033577521
32 mg tabletter - 100 tabletter i PVC / PVDC -blister - AIC n. 033577533
32 mg tabletter - 300 tabletter i PVC / PVDC -blister - AIC n. 033577545
Flaskförpackningar :
32 mg tabletter - 100 tabletter i HDPE -flaska - AIC n. 033577558
32 mg tabletter - 250 tabletter i HDPE -flaska - AIC n. 033577560
09.0 DATUM FÖR FÖRSTA GODKÄNNANDE ELLER FÖRNYELSE AV GODKÄNNANDE -
4 mg
17 december 1997/28 april 2012
8 mg- 16 mg- 32 mg
22 december 2005/28 april 2012
10.0 DATUM FÖR REVISION AV TEXTEN -
09/2015