Aktiva ingredienser: Tranexamsyra
TRANEX 500 MG / 5 ML INJEKTIONSLÖSNING
Tranex förpackningsinsatser är tillgängliga för förpackningsstorlekar:- TRANEX 500 MG / 5 ML INJEKTIONSLÖSNING
- Tranex 250 mg kapslar, Tranex 500 mg kapslar
Indikationer Varför används Tranex? Vad är det för?
TRANEX innehåller tranexaminsyra, som tillhör en grupp läkemedel som kallas antiblödning, antifibrinolytika, aminosyror.
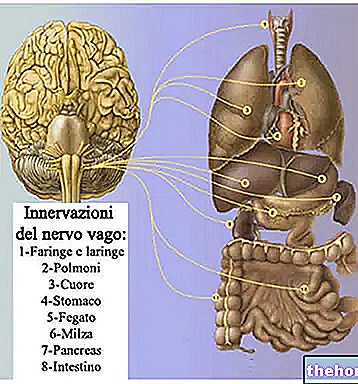
TRANEX används till vuxna och barn från ett års ålder för att förebygga och behandla blödning på grund av en process som hämmar blodproppar som kallas fibrinolys. De specifika indikationerna är:
- tung menstruationscykel;
- gastrointestinal blödning;
- blödningsstörningar i urinvägarna, efter prostatakirurgi eller urinvägsoperation;
- öron-, näs- eller halsoperation;
- hjärta, buk eller gynekologisk operation;
- blödning efter behandling med andra läkemedel för att lösa blodproppar.
Kontraindikationer När Tranex inte ska användas
Ta inte TRANEX om du:
- om du är allergisk mot tranexaminsyra eller något annat innehållsämne i detta läkemedel (anges i avsnitt 6)
- har en sjukdom som leder till bildning av blodproppar;
- har ett tillstånd som kallas 'konsumtionskoagulopati' där blod börjar koagulera i olika delar av kroppen;
- har njurproblem
- har haft anfall tidigare.
På grund av risken för cerebralt ödem och anfall rekommenderas intratekal och intraventrikulär injektion och intracerebral applicering.
Om du tror att något av detta gäller dig, eller om du har några andra frågor, tala med din läkare innan du tar TRANEX.
Försiktighetsåtgärder vid användning Vad du behöver veta innan du tar Tranex
Tala om för din läkare om något av följande gäller dig för att hjälpa dem att avgöra om TRANEX är rätt för dig:
- om du har märkt blod i urinen kan detta bero på en obstruktion i urinvägarna.
- om du löper risk för blodproppar
- om du har överdrivna blodproppar eller blödningar i hela kroppen (spridd intravaskulär koagulation), kanske TRANEX inte är lämpligt för dig, såvida du inte har akut svår blödning och dina blodprov har visat att processen som hämmar blodpropp, kallad fibrinolys, aktiveras ;
- om du har fått krampanfall ska TRANEX inte ges. Din läkare bör använda lägsta möjliga dos för att undvika kramper på grund av behandling med TRANEX;
- om du är på långvarig behandling med TRANEX bör du vara uppmärksam på eventuella störningar i färgsynen och vid behov bör behandlingen avbrytas. Vid långvarig användning av TRANEX injektionsvätska, rekommenderas regelbundna oftalmologiska undersökningar (ögonundersökningar inklusive synskärpa, färgseende, fundus, synfält etc.). Vid patologiska oftalmologiska förändringar, särskilt med näthinnesjukdomar, ska din läkare efter samråd med en specialist besluta om behovet av långvarig användning av TRANEX injektionsvätska, lösning i ditt fall.
Interaktioner Vilka läkemedel eller livsmedel som kan förändra effekten av Tranex
Tala om för din läkare eller apotekspersonal om du tar eller nyligen har tagit andra läkemedel, inklusive receptfria sådana, vitaminer, mineraler, växtbaserade läkemedel eller kosttillskott. Du bör särskilt tala om för din läkare om du tar:
- andra läkemedel som hjälper blodproppar som kallas antifibrinolytika;
- läkemedel som förhindrar blodproppar som kallas trombolytika;
- orala preventivmedel.
Varningar Det är viktigt att veta att:
Graviditet och amning
Fråga din läkare om du är gravid eller ammar innan du tar TRANEX.
Tranexaminsyra utsöndras i bröstmjölk, därför rekommenderas inte användning av TRANEX under amning.
Köra och använda maskiner
Inga studier har gjorts om förmågan att framföra fordon och använda maskiner.
Dos, metod och administreringstid Hur man använder Tranex: Dosering
Användning hos vuxna
TRANEX injektionsvätska, lösning ges till dig som en långsam injektion i en ven.
Din läkare kommer att bestämma rätt dos för dig och hur länge du behöver ta den.
Användning till barn
Om TRANEX injektionsvätska, lösning ges till ett barn från ett års ålder, beräknas dosen utifrån barnets vikt. Din läkare kommer att bestämma rätt dos för ditt barn och hur länge du behöver ta det.
Användning hos äldre
Det finns ingen anledning att minska dosen om det inte finns bevisad njurinsufficiens.
Användning till patienter med njurproblem
Om du har njurproblem minskar din dos av tranexaminsyra baserat på ett blodprov (serumkreatininnivå).
Användning till patienter med leverproblem
Det finns ingen anledning att minska dosen.
Administreringssätt
TRANEX måste administreras långsamt i en ven. TRANEX får inte injiceras i en muskel.
Överdosering Vad du ska göra om du har tagit för mycket Tranex
Om du får mer TRANEX än den rekommenderade dosen kan du ha en övergående blodtrycksfall. Tala omedelbart för din läkare eller apotekspersonal.
Biverkningar Vilka är biverkningarna av Tranex
Liksom alla läkemedel kan detta orsaka biverkningar men alla användare behöver inte få dem.
Biverkningar med TRANEX som har rapporterats är:
Följande biverkningar har observerats med TRANEX
Vanliga (kan förekomma hos upp till 1 av 10 patienter)
- effekter på mage och tarmar: illamående, kräkningar, diarré.
Mindre vanliga (kan förekomma hos 1 till 10 av 1000 patienter)
- effekter på huden: utslag.
Ingen känd frekvens (kan inte beräknas utifrån tillgängliga data)
- illamående med hypotoni (lågt blodtryck), särskilt om injektionen gavs för snabbt;
- blodproppar;
- effekter på nervsystemet: kramper
- effekter på ögonen: synstörningar inklusive nedsatt färgseende;
- effekter på immunsystemet: allergiska reaktioner.
Rapportering av biverkningar
Tala med din läkare eller apotekspersonal om du får några biverkningar. Detta inkluderar eventuella biverkningar som inte nämns i denna bipacksedel. Du kan också rapportera biverkningar direkt via det nationella rapporteringssystemet på http://www.agenziafarmaco.gov.it/it/responsabili. Genom att rapportera biverkningar kan du hjälpa till att ge mer information om läkemedlets säkerhet.
Giltighetstid och lagring
Detta läkemedel kräver inga särskilda förvaringsförhållanden.
Sammansättning och läkemedelsform
Vad TRANEX innehåller
Varje 5 ml injektionsflaska innehåller:
Aktiv ingrediens: 500 mg tranexaminsyra
Hjälpämnen: sterilt bidistillerat vatten efter smak en ml 5.
Hur TRANEX ser ut och förpackningens innehåll
Tranex 6 injektionsflaskor 5 ml
Varje injektionsflaska innehåller en klar och färglös lösning
Bipacksedel: AIFA (Italian Medicines Agency). Innehåll publicerat i januari 2016. Den information som finns finns kanske inte uppdaterad.
För att få tillgång till den senaste versionen är det lämpligt att gå till AIFA (Italian Medicines Agency) webbplats. Ansvarsfriskrivning och användbar information.
01.0 LÄKEMEDLETS NAMN
TRANEX 500 MG / 5 ML INJEKTIONSLÖSNING
02.0 KVALITATIV OCH KVANTITATIV SAMMANSÄTTNING
Varje injektionsflaska innehåller:
aktiv princip
tranexaminsyra 500 mg.
För fullständig förteckning över hjälpämnen, se avsnitt 6.1.
03.0 LÄKEMEDELSFORM
Injektionsvätska, lösning för intravenös användning.
04.0 KLINISK INFORMATION
04.1 Terapeutiska indikationer
Förebyggande och behandling av blödning på grund av generaliserad eller lokal fibrinolys hos vuxna och barn från ett års ålder.
De specifika indikationerna är:
• blödning orsakad av generaliserad eller lokal fibrinolys såsom:
- menorragi och metrorragi,
- gastrointestinal blödning,
- urinblödningsstörningar, efter prostatakirurgi eller kirurgiska ingrepp som involverar urinvägarna;
• ENT -operation (adenoidektomi, tonsillektomi, tandutdrag);
• gynekologisk kirurgi eller obstetriska störningar;
• bröstkorgs- och bukoperationer och andra större operationer såsom kardiovaskulär kirurgi;
• hantering av blödning på grund av administrering av ett fibrinolytikum.
04.2 Dosering och administreringssätt
Dosering
Vuxna
Om inte annat föreskrivs rekommenderas följande doser:
1. standardbehandling av lokal fibrinolys:
0,5 g (1 x 5 ml ampull) till 1 g (1 x 10 ml ampull eller 2 x 5 ml ampuller) tranexamsyra genom långsam intravenös injektion (= 1 ml / minut) två eller tre gånger om dagen
2. standardbehandling av generaliserad fibrinolys:
1 g (1 ampull om 10 ml eller 2 ampuller om 5 ml) tranexaminsyra genom långsam intravenös injektion (= 1 ml / minut) var 6-8 timme, lika med 15 mg / kg kroppsvikt.
Njursvikt
Vid njurinsufficiens som kan innebära risk för ackumulering är användning av tranexamsyra kontraindicerad hos patienter med svår njurinsufficiens (se avsnitt 4.3). För patienter med lätt till måttligt nedsatt njurfunktion bör dosen tranexaminsyra minskas baserat på serumkreatininnivån.
Leverinsufficiens
Ingen dosjustering krävs hos patienter med leverinsufficiens.
Pediatrisk population
För barn från ett års ålder, för de nuvarande godkända indikationerna som beskrivs i avsnitt 4.1, är dosen cirka 20 mg / kg / dag. Det finns dock få data om effekt, dosering och säkerhet för dessa indikationer.
Det finns inga uttömmande utvärderingar av effekt, dosering och säkerhet av tranexamsyra hos barn som genomgår hjärtoperation. För närvarande tillgängliga data är begränsade och presenteras i avsnitt 5.1.
Pensionärer
Det finns ingen anledning att minska dosen om det inte finns bevisad njurinsufficiens.
Administreringssätt
Administrering måste nödvändigtvis ske genom långsam intravenös injektion.
04.3 Kontraindikationer
Överkänslighet mot den aktiva substansen eller mot något hjälpämne som anges i avsnitt 6.1.
Akut venös eller arteriell trombos (se avsnitt 4.4).
Fibrinolytiska tillstånd på grund av konsumtionskoagulopati utom i de fall där det finns en övervägande aktivering av det fibrinolytiska systemet med akut svår blödning (se avsnitt 4.4).
Allvarlig njurinsufficiens (risk för ackumulering).
Anfallshistoria.
Intratekal och intraventrikulär injektion, intracerebral applikation (risk för cerebralt ödem och kramper)
04.4 Särskilda varningar och lämpliga försiktighetsåtgärder vid användning
Ovanstående indikationer och administreringssätt måste följas strikt:
• Intravenösa injektioner ska göras långsamt.
• Tranexamsyra får inte administreras intramuskulärt.
Kramper
Fall av anfall har rapporterats i samband med behandling med tranexamsyra. Vid koronar bypass -transplantation (CABG) har de flesta fall inträffat efter intravenös (IV) injektion av höga doser tranexaminsyra. Med lägre rekommenderade doser av tranexaminsyra, förekomsten av postoperativa anfall var densamma som hos obehandlade patienter.
Synstörningar
Uppmärksamhet bör ägnas åt eventuella synstörningar, inklusive synskada, dimsyn, nedsatt färgseende och vid behov behandlingen avbrytas. Vid långvarig användning av tranexaminsyralösning för injektion rekommenderas regelbundna oftalmologiska undersökningar (ögonundersökningar inklusive synskärpa, färgsyn, fundus, synfält etc.). Vid patologiska oftalmologiska förändringar, särskilt med patologier i näthinnan, bör läkaren, efter att ha rådfrågat en specialist, besluta om behovet av långvarig användning av tranexamsyra, injektionsvätska, lösning i varje enskilt fall.
Hematuri
Vid hematuri i övre urinvägarna finns risk för urinrörsobstruktion och mekanisk anuri.
Tromboemboliska händelser
Innan du använder tranexaminsyra bör riskfaktorer för tromboembolisk sjukdom övervägas. Hos patienter med tromboembolisk historia eller hos personer med en "hög förekomst av tromboemboliska händelser" i familjehistorien (patienter med hög risk för trombofili), lösning Tranexamsyra för injektion ska endast administreras om det uttryckligen anges av läkaren, efter samråd med en specialist på hemostaseologi och under noggrann medicinsk övervakning (se avsnitt 4.3).
Tranexaminsyra ska administreras med försiktighet till patienter som tar orala preventivmedel på grund av ökad risk för trombos (se avsnitt 4.5).
Spridad intravaskulär koagulation
Patienter med spridd intravaskulär koagulation (DIC) kan i de flesta fall inte behandlas med tranexamsyra (se avsnitt 4.3). Om ett beslut fattas att administrera tranexamsyra, bör detta endast göras hos patienter där det finns en "Övervägande aktivering av fibrinolytiskt system med akut allvarlig blödning Normalt sett närmar sig den hematologiska profilen följande: minskad lystid för euglobulinkoagulatet, förlängd protrombintid, minskade plasmanivåer av fibrinogen, faktorer V och VIII, plasminogen fibrinolysin och alfa-2 makroglobulin, normala plasmanivåer av protrombinkomplexet, dvs. faktorer II (protrombin), VIII och X; förhöjda plasmanivåer av fibrinogennedbrytningsprodukter, normalt antal trombocyter. Ovanstående antar att den underliggande sjukdomen inte förändras. för sig själv de olika elementen i denna profil. I dessa akuta fall en vanliga dos på 1 g tranexamsyra eller är det tillräckligt för att kontrollera blödning. Administrering av tranexaminsyra i DIC bör endast övervägas om tillräcklig hematologisk laboratorieutrustning finns tillgänglig och i närvaro av expert personal.
04.5 Interaktioner med andra läkemedel och andra former av interaktion
Inga interaktionsstudier har utförts. Samtidig behandling med antikoagulantia kan endast ske under noggrann övervakning av en läkare med erfarenhet inom detta område. Läkemedel som verkar på hemostas bör administreras med försiktighet till patienter som behandlas med tranexaminsyra. Det finns en teoretisk risk för en potentiell ökning av trombbildning, som sker med östrogen. Alternativt kan läkemedlets antifibrinolytiska verkan antagoniseras med trombolytiska läkemedel.
04.6 Graviditet och amning
Kvinnor i fertil ålder måste använda effektiva preventivmedel under behandlingen.
Graviditet
Det finns otillräckliga kliniska data om användning av tranexamsyra hos gravida kvinnor. Följaktligen, även om djurstudier inte rapporterar teratogena effekter, som en försiktighetsåtgärd för användning, rekommenderas inte användning av tranexamsyra under graviditetens första trimester. Begränsade kliniska data om användning av tranexamsyra vid olika blödningsförhållanden under andra och tredje trimestern av graviditeten har inte rapporterat någon skadlig effekt för fostret Tranexaminsyra kan endast användas under graviditet om de förväntade fördelarna motiverar den potentiella risken.
Graviditet
Tranexaminsyra utsöndras i bröstmjölk, därför rekommenderas inte amning.
Fertilitet
Det finns inga kliniska data om effekterna av tranexaminsyra på fertiliteten.
04.7 Effekter på förmågan att framföra fordon och använda maskiner
Inga studier har gjorts om förmågan att framföra fordon och använda maskiner.
04.8 Biverkningar
Biverkningar som rapporterats i kliniska prövningar och på grundval av erfarenhet efter marknadsföring listas nedan efter systemorganklass.
Tabell med listan över biverkningar
Biverkningar som rapporteras ingår i tabellen nedan och listas efter MedDRA primära organklass. Inom varje systemorganklass är biverkningarna rankade efter frekvens. Inom varje frekvenskategori listas biverkningarna efter minskande svårighetsgrad. Frekvenskategorier definieras enligt följande: mycket vanligt (≥1 / 10); vanliga (≥1 / 100
Rapportering av misstänkta biverkningar
Rapportering av misstänkta biverkningar som inträffar efter godkännande av läkemedlet är viktigt, eftersom det möjliggör kontinuerlig övervakning av nytta / riskbalansen för läkemedlet.Hälso- och sjukvårdspersonal uppmanas att rapportera alla misstänkta biverkningar via: www. Agenziafarmaco.gov. it/it/responsabili.
04.9 Överdosering
Inga fall av överdos har rapporterats.
Tecknen och symtomen kan vara yrsel, huvudvärk, hypotoni och anfall. Kramper har visat sig inträffa oftare vid ökad dos.
Hantering av överdos bör bestå av stödjande vård.
05.0 FARMAKOLOGISKA EGENSKAPER
05.1 Farmakodynamiska egenskaper
Farmakoterapeutisk grupp: antiblödning, antifibrinolytika.
ATC -kod: B02AA02.
Tranexaminsyra har en anti-hemorragisk aktivitet genom att hämma de fibrinolytiska egenskaperna hos plasmin.
Ett komplex bildas som inkluderar tranexaminsyra och plasminogen; tranexaminsyra binder till plasminogen när det omvandlas till plasmin.
Tranexaminsyra-plasminkomplexets aktivitet på fibrinaktivitet är lägre än aktiviteten av fritt plasmin enbart.
Utbildning in vitro visade att höga doser tranexaminsyra minskade komplementaktiviteten.
Pediatrisk population
Barn från ett år
I litteraturen identifierades 12 effektstudier vid barnkirurgi som inkluderade 1073 barn, 631 behandlade med tranexaminsyra. De flesta studierna var placebokontrollerade. Den studerade befolkningen var heterogen när det gäller ålder, typ av operation och doseringsregimer. Resultat från tranexaminsyrastudier indikerar mindre blodförlust och mindre behov av blodprodukter vid pediatrisk hjärtkirurgi med hjärt -bypass (CPB) när det är hög risk för blödning, särskilt hos cyanotiska patienter eller hos patienter som genomgår upprepade kirurgiska ingrepp. Det mest lämpliga doseringsschemat visade sig vara:
- första bolus på 10 mg / kg efter induktion av anestesi och före hudskärning,
- kontinuerlig infusion av 10 mg / kg / timme eller injektion i CPB -pumpens grundvätska i en dos som är lämplig för CPB -proceduren, eller enligt patientens vikt vid en dos av 10 mg / kg, eller enligt grundningsvolymen av pumpens CPB, med den sista injektionen av 10 mg / kg vid slutet av hjärt -lungpassagen.
Även om studierna omfattade ett mycket begränsat antal patienter, tyder de få tillgängliga uppgifterna på att kontinuerlig infusion är att föredra, eftersom den bibehåller terapeutiska plasmakoncentrationer under hela operationen.
Inga specifika dos-effekt- och farmakokinetiska studier har utförts på barn.
05.2 Farmakokinetiska egenskaper
Absorption:
De maximala plasmakoncentrationerna av tranexaminsyra uppnås snabbt efter en kort intravenös infusion, varefter plasmakoncentrationerna minskar på ett multi-exponentiellt sätt.
Distribution
Plasmaproteinbindningen av tranexaminsyra är cirka 3% vid terapeutiska plasmanivåer och tycks helt bero på dess bindning till plasminogen Tranexaminsyra binder inte till serumalbumin. Den initiala distributionsvolymen är cirka 9-12 liter.
Tranexaminsyra passerar placentan. Efter administrering av en intravenös injektion av 10 mg / kg till 12 gravida kvinnor var serumkoncentrationen av tranexaminsyra mellan 10 och 53 mcg / ml, medan den i navelsträngen i blodet var mellan 4 och 31 mcg / ml. Tranexaminsyra diffunderar snabbt in i ledvätskan och ledmembranet. Efter administrering av en intravenös injektion av 10 mg / kg till 17 patienter som genomgick en knäoperation, var koncentrationerna i ledvätskan liknande de som observerades i de relaterade serumproven. Koncentrationen av tranexaminsyra i ett antal andra vävnader motsvarar en bråkdel av den som observerats i blodet (en hundradel i bröstmjölk, en tiondel i cerebrospinalvätska, en tiondel i vattenhaltig humor). Tranexamsyra detekterades i sperma, där det hämmar fibrinolytisk aktivitet men påverkar inte spermier.
Exkretion
Det utsöndras huvudsakligen i urinen som oförändrat läkemedel. Urinutsöndring via glomerulär filtrering är den viktigaste elimineringsvägen. Renal clearance är lika med plasmaclearance (110-116 ml / min). Tranexaminsyra utsöndring är cirka 90% under de första 24 timmarna efter intravenös administrering av 10 mg / kg kroppsvikt. Halveringstiden för tranexaminsyra är cirka 3 timmar.
Särskilda populationer
Plasmakoncentrationerna ökar hos patienter med njurinsufficiens.
Inga specifika farmakokinetiska studier har utförts på barn.
05.3 Prekliniska säkerhetsdata
Icke-kliniska data avslöjar ingen specifik fara för människor baserat på konventionella studier av säkerhetsfarmakologi, toxicitet vid upprepade doser, gentoxicitet, cancerframkallande potential och reproduktionstoxicitet.
Epileptogen aktivitet observerades vid intratekal användning av tranexamsyra hos djur.
06.0 LÄKEMEDELSINFORMATION
06.1 Hjälpämnen
Injektionsflaskor:
vatten för injektionsvätskor q.s. till 5 ml.
06.2 Oförenlighet
Tranex visar inte kemisk inkompatibilitet med andra ämnen som eventuellt är associerade i terapin.
06.3 Giltighetstid
Tranex 500 mg / 5 ml injektionsvätska, lösning: fem år.
06.4 Särskilda förvaringsanvisningar
Detta läkemedel kräver inga särskilda förvaringsförhållanden.
06.5 Förpackningens innehåll och förpackningens innehåll
Tranex 6 injektionsflaskor 5 ml: Typ I -glas
06.6 Anvisningar för användning och hantering
Inga särskilda anvisningar för destruktion.
07.0 INNEHAVARE AV GODKÄNNANDE FÖR FÖRSÄLJNING
MALESCI ISTITUTO FARMACOBIOLOGICO SpA
Via Lungo l "Ema, 7 - Bagno a Ripoli FI
Återförsäljare till salu: Istituto Luso Farmaco d "Italia SpA - Milanofiori - Road 6 - Building L - Rozzano (MI).
08.0 NUMMER FÖR FÖRSÄLJNINGSTILLSTÅND
Tranex 500 mg / 5 ml injektionsvätska, lösning: A.I.C. n. 022019032
09.0 DATUM FÖR FÖRSTA GODKÄNNANDE ELLER FÖRNYELSE AV GODKÄNNANDET
Datum för första godkännandet: 21 juni 1979
Förnyelse av tillståndet: 31 maj 2010.
10.0 DATUM FÖR REVISION AV TEXTEN
April 2015