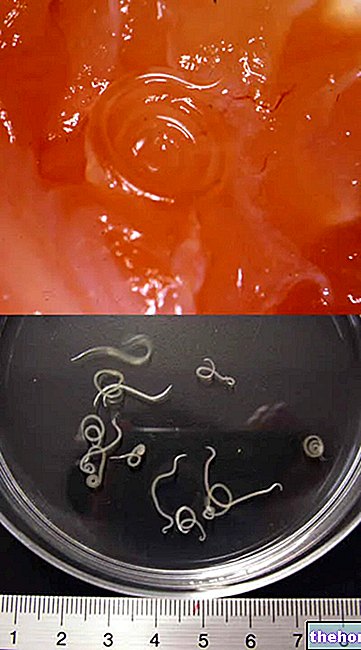
Glykogen är en makromolekyl (molekylmassa på cirka 400 miljoner dalton) av α-glukos där det huvudsakligen finns α-1,4 glykosidbindningar och förgreningar i ett förhållande av 1:10, på grund av α-1,6 glykosidbindningar.
Glykogen utgör reservmaterial och nedbryts och rekonstitueras kontinuerligt; i hela kroppens cellmassa finns det cirka 100 g glykogen: det mesta finns i levern där det är rörligt och kan därför användas som reserv för andra organ (glykogen i muskler är inte rörligt).
Enzymerna som katalyserar nedbrytningen och syntesen av glykogen finns alla i cytoplasman, därför behövs ett regleringssystem som gör den ena vägen inaktiv när den andra är aktiv: om det finns glukos tillgängligt omvandlas det senare till glykogen (anabolism) vilket är en reserv, vice versa, om c "krävs för glukos, nedbryts glykogenet (katabolism).

Enzymet som främst är inblandat i nedbrytningen av glykogen är glykogenfosforylas; detta enzym kan klyva en glykosidisk α-1,4-bindning med hjälp av ett oorganiskt ortofosfat som lytiskt medel: klyvningen sker på fosforolytiskt sätt och glukos 1-fosfat erhålls.
Vid fem eller sex enheter från en förgreningspunkt kan glykogenfosforylasenzymet inte längre verka, därför lossnar det från glykogenet och ersätts av ett deramifierande enzym som är ett transferas: i det katalytiska stället för detta enzym är c "en" histidin som möjliggör överföring av tre sackaridenheter till närmaste glykosidkedja (histidin angriper det första kolet i en glukosmolekyl). Det nyss nämnda enzymet är glykosyltransferas; vid slutet av verkan av detta enzym återstår endast en glukosenhet på sidokedjan med det första kolet bundet till det sjätte kolet av en glukos i huvudkedjan. Den sista glukosenheten i sidokedjan frigörs genom verkan av "enzym a-1,6 glykosidas (detta enzym utgör den andra delen av det deramifierande enzymet); med tanke på att grenarna i glykogen är i ett förhållande av 1:10 får vi från den fullständiga nedbrytningen av makromolekylen cirka 90% glukos 1-fosfat och cirka 10% av glukos.
Verkan av de ovannämnda enzymerna möjliggör eliminering av en sidokedja från glykogenmolekylen; aktiviteten hos dessa enzymer kan upprepas tills fullständig nedbrytning av kedjan sker.
Låt oss överväga en hepatocyt; glukos (assimileras genom kosten), när den kommer in i cellen omvandlas till glukos 6-fosfat och aktiveras därmed. Glukos 6-fosfat, genom verkan av fosfoglukomutas, omvandlas till glukos 1-fosfat: det senare är en icke-omedelbar föregångare till biosyntes; i biosyntes används en aktiverad form av socker som representeras av socker kopplat till ett difosfat: vanligtvis uridyldifosfat (UDP). Glukos 1- fosfat är omvandlas sedan till UDP-glukos, denna metabolit under verkan av glykogensyntas som kan binda UDP-glukos till en icke-reducerande ände av det växande glykogenet: långsträckt glykogen från en glukosidenhet och UDP erhålls.UDP omvandlas av det nukleosiderade difosfokinasenzymet till UTP som återgår till cirkulationen.
Nedbrytningen av glykogen sker genom verkan av glykogenfosforylas som frigör en glukosmolekyl och omvandlar den till glukos 1-fosfat. Därefter omvandlar fosfoglukomutas glukos 1-fosfat till glukos 6-fosfat.
Glykogen syntetiseras framför allt i levern och musklerna: i organismen finns 1-1,2 hektar glykogen fördelat över muskelmassan.
Glykogen i en myocyt representerar en energireserv endast för denna cell medan glykogenet i levern också är en reserv för andra vävnader, det vill säga att det kan skickas som glukos till andra celler.
Glukos 6-fosfatet som erhålls i musklerna från nedbrytningen av glykogen skickas sedan, vid energibehov, till glykolys; i levern omvandlas glukos 6-fosfat till glukos genom verkan av glukos 6-fosfatfosfatas (karakteristiskt enzym av hepatocyter) och transporteras in i blodomloppet.
Glykogensyntas och glykogenfosforylas fungerar båda på de icke-reducerande enheterna av glykogen så det måste finnas en hormonell signal som styr aktiveringen av en väg och blockering av den andra (eller vice versa).
I laboratoriet var det möjligt att förlänga glykogenkedjan genom att utnyttja glykogenfosforylas och använda glukos 1-fosfat i en mycket hög koncentration.
I celler katalyserar glykogenfosforylas endast nedbrytningsreaktionen eftersom koncentrationerna av metaboliterna är sådana att de förskjuter jämvikten för följande reaktion till höger (dvs mot nedbrytning av glykogen):

Låt oss se verkningsmekanismen för glykogenfosforylaset: acetalsyret (som fungerar som en brygga mellan glukosenheterna) binder till fosforylens väte: en reaktionsmellanprodukt bildas av en karbokation (på glukosen som är allt " extremiteter) till vilka fosforyl (Pi) binder mycket snabbt.
Glykogenfosforylas kräver en kofaktor som är pyridoxalfosfat (denna molekyl är också en kofaktor för transaminaser): den har en delvis protonerad fosforyl (pyridoxalfosfat omges av en hydrofob miljö som motiverar närvaron av protoner bundna till den). Fosforyl (Pi) kan överföra en proton till glykogenet eftersom denna fosforyl sedan återvinner protonen från den delvis protonerade fosforylen i pyridoxalfosfatet. Sannolikheten för att fosforyl vid fysiologiskt pH tappar sin proton och förblir helt deprotoniserad är mycket låg.
Låt oss nu se hur fosfoglukomutas fungerar. Detta enzym presenterar, på det katalytiska stället, en återstod av fosforylerad serin; serin ger fosforyl till glukos 1-fosfat (i position sex): glukos 1,6-bisfosfat bildas under en kort tid, sedan återfosforyleras serin med fosforyl i position ett. Fosfoglukomutas kan fungera i båda riktningarna, dvs omvandla glukos 1-fosfat till glukos 6-fosfat eller vice versa; om glukos 6-fosfat produceras kan det skickas direkt till glykolys, i musklerna eller omvandlas till glukos i levern.
Enzymet uridylfosfogluko -transferas (eller UDP -glukospyrofosforylas) katalyserar glukos 1-fosfatöverföringsreaktionen till UTP genom vidhäftning till fosforyl a.
Det enzym som just beskrivits är ett pyrofosforylas: detta namn beror på att den motsatta reaktionen till den som just beskrivits är en pyrofosforylering.
UDP -glukos, erhållet enligt beskrivningen, kan förlänga glykogenkedjan med en monosackaridenhet.
Det är möjligt att få reaktionen att utvecklas mot bildning av UDP -glukos genom att eliminera en produkt som är pyrofosfat; enzymet pyrofosfatas omvandlar pyrofosfat till två molekyler ortofosfat (hydrolys av en anhydrid) och håller därigenom koncentrationen av pyrofosfat så låg att processen för bildning av UDP -glukos termodynamiskt gynnas.
Som nämnts kan UDP -glukos tack vare glykogensyntasets verkan förlänga glykogenkedjan.
Förgreningarna (i ett förhållande av 1:10) beror på det faktum att när en glykogenkedja består av 20-25 enheter intervenerar ett förgreningsenzym (med ett "histidin på sitt katalytiska ställe) som kan överföra en serie av 7 -8 glykosidiska enheter längre nedströms 5-6 enheter: således genereras en ny förgrening.
Av skäl av nervöst ursprung eller om det behövs energi på grund av fysisk ansträngning utsöndras adrenalin från binjurarna.
Målcellerna för adrenalin (och noradrenalin) är de i levern, musklerna och fettvävnaden (i den senare sker nedbrytningen av triglycerider och cirkulationen av fettsyror: följaktligen produceras glukos i mitokondrier 6 -fosfat, skickas till glykolys, medan glukos 6-fosfat i adipocyter omvandlas till glukos genom verkan av enzymet glukos 6-fosfatfosfatas och exporteras till vävnaderna).
Låt oss nu se hur adrenalinet fungerar. Adrenalin binder till en receptor placerad på cellmembranet (av myocyter och hepatocyter) och detta bestämmer translationen av signalen från utsidan till inuti cellen.Proteinkinaset aktiveras som verkar samtidigt på de system som reglerar syntes och nedbrytning av glykogen:
Glykogensyntas finns i två former: en defosforylerad (aktiv) form och en fosforylerad (inaktiv) form; proteinkinas fosforylerar glykogensyntas och blockerar dess verkan.
Glykogenfosforylas kan existera i två former: en aktiv form där en fosforylerad serin är närvarande och en inaktiv form där serin defosforyleras. Glykogenfosforylas kan aktiveras av enzymet glykogenfosforylas -kinas. Glykogenfosforylas -kinas är aktivt om det är fosforylerat och inaktivt om det är defosforylerat; proteinkinaset har som substrat glykogenfosforylaskinas, det vill säga det kan fosforylera (och därför aktivera) det senare som i sin tur aktiverar glykogenfosforylaset.
När adrenalinsignalen väl är över måste den effekt den har på cellen också upphöra: fosfatasenzymer ingriper sedan på proteinslagen.

.jpg)