Elementaranalysen av proteiner ger följande medelvärden: 55% kol, 7% väte och 16% kväve; det är klart att proteiner skiljer sig från varandra, men deras genomsnittliga elementära sammansättning skiljer sig lite från de värden som anges ovan .
Konstitutionellt är proteiner makromolekyler bildade av naturliga a-aminosyror; aminosyrorna förenas genom amidbindningen som upprättas genom reaktionen mellan en aminogrupp i en a-aminosyra och karboxylen i en annan a-aminosyra.
Denna bindning (-CO-NH-) kallas också en peptidbindning eftersom den binder peptider (aminosyror i kombination):
den erhållna är en dipeptid eftersom den består av två aminosyror. Eftersom en dipeptid innehåller en fri aminogrupp i ena änden (NH2) och en karboxyl i den andra (COOH) kan den reagera med en eller flera aminosyror och förlänga kedjan både från höger och från vänster, med samma reaktion sett ovan.
Reaktionssekvensen (som förresten inte är så enkel) kan fortsätta på obestämd tid: tills det finns en polymer som heter polypeptid eller protein. Skillnaden mellan peptider och proteiner är kopplad till molekylvikten: vanligtvis för molekylvikter högre än 10 000 talar vi om proteiner.
Att binda aminosyror för att få till och med små proteiner är en svår uppgift, även om det nyligen har utvecklats en automatisk metod för att producera proteiner från aminosyror som ger utmärkta resultat.
Det enklaste proteinet består därför av 2 aminosyror: enligt internationell konvention startar den ordnade numreringen av aminosyror i en proteinstruktur från aminosyran med den fria a-aminogruppen.
kodning för detta protein) som stöter på icke försumbara kemiska svårigheter.
Det var möjligt att bestämma den ordnade sekvensen av aminosyror genom Edman-nedbrytning: proteinet omsattes med fenylisotiocyanat (FITC); initialt angriper a-aminokväve-dubletten fenylisotiocyanatet som bildar tiokarbamylderivatet; därefter cykliserar den erhållna produkten vilket ger fenyltiohydantoinderivatet som är fluorescerande.
Edman har tagit fram en maskin som kallas en sequencer som automatiskt justerar parametrarna (tid, reagenser, pH, etc.) för nedbrytning och ger proteinernas primära struktur (för detta fick han Nobelpriset).
Den primära strukturen är inte tillräcklig för att fullt ut tolka proteinmolekylernas egenskaper; man tror att dessa egenskaper på ett väsentligt sätt beror på den rumsliga konfiguration som proteinmolekylerna tenderar att anta, vikande på olika sätt: det vill säga antar det som har definierats som sekundär struktur av proteiner.
Proteinernas sekundära struktur flimrar, det vill säga att den tenderar att sönderfalla genom uppvärmning; då denaturerar proteinerna sig själva och förlorar många av sina karakteristiska egenskaper. Förutom uppvärmning över 70 ° C kan denaturering också orsakas av bestrålning eller av reaktionernas verkan (till exempel från starka syror).
Denaturering av proteiner på grund av den termiska effekten observeras till exempel genom att värma äggviten: det ses att det förlorar sitt gelatinartade utseende och blir till en olöslig vit substans. Denaturering av proteiner leder emellertid till förstörelsen av deras sekundära struktur, men lämnar deras primära struktur oförändrad (sammankopplingen av de olika aminosyrorna).
Proteiner tar på sig den tertiära strukturen när deras kedja, även om den fortfarande är flexibel trots böjningen av den sekundära strukturen, viker på ett sådant sätt att den uppstår ett förvrängt tredimensionellt arrangemang i form av en fast kropp. Ansvarig för den tertiära strukturen är framför allt disulfidbindningarna som kan upprättas mellan cystein -SH spridda längs molekylen.
Den kvartära strukturen å andra sidan tillhör endast proteiner som bildas av två eller flera subenheter. Hemoglobin, till exempel, består av två par proteiner (det vill säga i alla fyra proteinkedjor) belägna vid hörnen av en tetraeder för att ge upphov till en sfärisk struktur; de fyra proteinkedjorna hålls samman av krafter joniska och icke-kovalenta bindningar.
Ett annat exempel på en kvaternär struktur är insulinets, vilket tycks bestå av så många som sex proteinunderenheter arrangerade i par vid hörnen av en triangel i vars centrum är två zinkatomer.
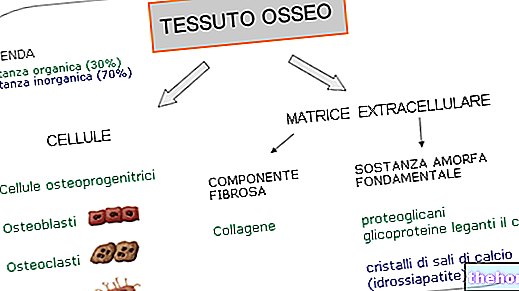
Fibrösa proteiner
De är proteiner med en viss styvhet och har en mycket längre axel än den andra; det fibrösa proteinet som finns i större mängder i naturen är kollagen (eller kollagen).
Ett fibröst protein kan anta olika sekundära strukturer: a-helix, β-ark och, för kollagen, trippel helix; α-helix är den mest stabila strukturen, följt av β-arket, medan den minst stabila av de tre är trippelhelixen.
höger om, efter huvudskelettet (orienterat från botten till toppen), utförs en rörelse som liknar skruvning av en högerskruv; medan helixen är av vänster hand om rörelsen är analog med skruvning av en vänsterhänt skruv. I de högra α-helixerna är aminosyrornas -R-substituenter vinkelräta mot proteinets huvudaxel och vänd utåt, medan de är i vänster- hand a -spiraler -R -substituenterna vetter inåt. Högerhänta a-spiraler är mer stabila än vänsterhänta eftersom mellan vati -R c "är det mindre interaktion och mindre steriskt hinder. Alla a-spiraler som finns i proteiner är dextrorotala.
Strukturen för a-helixen stabiliseras av vätebindningarna (vätebryggor) som bildas mellan karboxylgruppen (-C = O) för varje aminosyra och aminogruppen (-NH) som hittades fyra rester senare i linjär sekvens.
Ett exempel på ett protein som har en a-helixstruktur är hårkeratin.
Genom att förlänga a-helixstrukturen utförs övergången från a-helix till p-ark; även värmen eller den mekaniska påkänningen låter passera från a-helixen till p-arkstrukturen.
Vanligtvis, i ett protein, är p-arkstrukturerna nära varandra eftersom vätbindningar mellan kedjor kan upprättas mellan delar av själva proteinet.
I fibrösa proteiner är det mesta av proteinstrukturen organiserad i en a-helix eller β-ark.
Globulära proteiner
De har en nästan sfärisk rumslig struktur (på grund av de många ändringarna i riktningen för polypeptidkedjan); vissa delar av varande kan spåras tillbaka till en a-helix eller β-arkstruktur och andra delar kan inte i stället hänföras till dessa former: arrangemanget är inte slumpmässigt utan organiserat och repetitivt.
De proteiner som hänvisas till hittills är ämnen med en helt homogen konstitution: det vill säga rena sekvenser av kombinerade aminosyror; sådana proteiner sägs enkel; det finns proteiner som består av en proteindel och en icke-proteindel (prostatagrupp) som kallas proteiner konjugera.
, i naglarna, i hornhinnan och i ögonlinsen, mellan interstitiella utrymmen i vissa organ (t.ex. lever) och så vidare.
Dess struktur ger den speciella mekaniska förmågor; den har stor mekanisk styrka i samband med hög elasticitet (t.ex. i senor) eller hög styvhet (t.ex. i ben) beroende på vilken funktion den måste utföra.
En av de mest nyfikna egenskaperna hos kollagen är dess konstitutiva enkelhet: det består av cirka 30% prolin och cirka 30% glycin; de övriga 18 aminosyrorna behöver bara dela de återstående 40% av proteinstrukturen. Aminosyrasekvensen för kollagen är anmärkningsvärt regelbunden: för varje tre rester är den tredje glycin.
Proline är en cyklisk aminosyra där R-gruppen binder till a-aminokvävet och detta ger den en viss styvhet.
Den slutliga strukturen är en repetitiv kedja som har formen av en "helix; inom kollagenkedjan saknas vätebindningar. Kollagen är en "vänster helix med en tonhöjd (längd motsvarande ett varv av spiralen) större än" α-helixen; kollagenhelixen är så lös att tre proteinkedjor kan linda runt varandra och bilda en " enda rep: trippel helix struktur.
Trippelhelixen för kollagen är emellertid mindre stabil än både a-helixen och p-arkstrukturen.
Låt oss nu se den mekanism genom vilken kollagen produceras; Tänk till exempel på ett blodkärls bristning: denna bristning åtföljs av en myriad av signaler i syfte att stänga kärlet och därmed bilda koagulatet.
Koagulation kräver minst trettio specialiserade enzymer. Efter blodproppen är det nödvändigt att fortsätta med reparationen av vävnaden; celler nära såret producerar också kollagen. För att göra detta induceras först uttrycket av en gen, det vill säga organismer som utgår från informationen från en gen kan producera proteinet (den genetiska informationen transkriberas på mRNA som lämnar kärnan och når ribosomerna i cytoplasma där den genetiska informationen översätts till protein). Därefter syntetiseras kollagenet i ribosomerna (det ser ut som en vänster helix som består av cirka 1200 aminosyror och har en molekylvikt på cirka 150 000 d) och ackumuleras sedan i lumen där det blir ett substrat för enzymer som kan utföra posttranslationella modifieringar (modifieringar av språket översatt av "mRNA); i kollagen består dessa modifieringar i hydroxylering av vissa sidokedjor, särskilt prolin och lysin.
Misslyckandet hos de enzymer som leder till dessa förändringar orsakar skörbjugg: det är en sjukdom som initialt orsakar att blodkärlen bryts, att tänderna går sönder som kan följas av interintestinala blödningar och död; det kan orsakas av kontinuerlig användning av livsmedel med lång livslängd.
På grund av verkan av andra enzymer inträffar därefter andra modifieringar som består i glykosideringen av hydroxylgrupperna av prolin och lysin (ett socker binder till syret i OH); dessa enzymer finns i andra områden än lumen, därför att proteinet, medan det genomgår modifieringar, migrerar inuti det endoplasmatiska retikulum för att hamna i säckar (vesiklar) som stänger sig och lossnar från retikulumet: inuti dem finns det glykosiderade pro -kollagenmonomer; den senare når Golgi-apparaten där särskilda enzymer känner igen cystein som finns i den karboxiterminala delen av det glykosiderade pro-kollagenet och får de olika kedjorna att närma sig varandra och bilda disulfidbryggor: på detta sätt tre kedjor av glykosiderat pro-kollagen erhålls sammanlänkade och detta är utgångspunkten från vilken de tre kedjorna, som tränger igenom, spontant ger upphov till trippelhelixen.De tre kedjorna av glykoxiderat pro-kollagen som är sammanlänkade når, sedan en vesikel som, kväver sig själv, lossnar från Golgi -apparaten och transporterar de tre kedjorna mot cellens periferi, varigenom smältningen jon med plasmamembranet, utvisas trimetern från cellen.
I det extra cellulära utrymmet finns särskilda enzymer, pro-kollagenpeptidaserna, som tar bort från arten som utvisas från cellen, tre fragment (ett för varje helix) av 300 aminosyror l "ett, från den terminala karboxidelen och tre fragment (en för varje helix) på cirka 100 aminosyror vardera, från den aminoterminala delen: det finns en trippelspiral kvar som består av cirka 800 aminosyror per helix som kallas tropokollagen.
Tropokollagen ser ut som en ganska stel stav; de olika trimererna associeras med kovalenta bindningar för att ge större strukturer: mikrofibriller. I mikrofibriller är de olika trimrarna arrangerade på ett förskjutet sätt; många mikrofibriller utgör tropokollagenbuntar.
I benen, mellan kollagenfibrerna, finns interstitiella utrymmen där sulfater och fosfater av kalcium och magnesium deponeras: dessa salter täcker också alla fibrer; detta gör benen styva.
I senor är interstitiella utrymmen mindre rika på kristaller än i ben medan mindre proteiner finns närvarande än i tropokollagen: detta ger senor elasticitet.
Osteoporos är en sjukdom som orsakas av brist på kalcium och magnesium vilket gör det omöjligt att fixera salter i de interstitiella områdena i tropokollagenfibrerna.