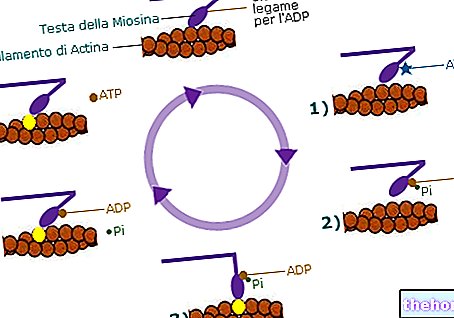
För att tala om de tjugo aminosyrorna som utgör proteinstrukturerna och de modifierade, skulle det vara nödvändigt att beskriva minst tolv specialiserade metaboliska vägar.
Men varför använder celler så många metaboliska vägar som kräver energi (till exempel för att regenerera enzymets katalytiska platser), var och en med en enzymatisk patrimonium, för att katabolisera aminosyror? Från nästan alla aminosyror är det möjligt att via specialiserade vägar erhålla metaboliter som till en liten del används för att producera energi (till exempel genom glukoneogenes och vägen för ketonkroppar) men som framför allt leder till bildandet av komplex molekyler, med ett stort antal kolatomer (till exempel från fenylalanin och tyrosin, hormoner produceras i binjurarna som är specialiserade för detta ändamål); om det å ena sidan skulle vara enkelt att producera energi från aminosyror, å andra sidan skulle det vara komplicerat att bygga komplexa molekyler utgående från små molekyler: katabolismen av aminosyror gör att de kan utnyttja sitt skelett för att få större arter.
Två eller tre hektar aminosyror bryts ned dagligen av en frisk person: 60-100 g av dem härrör från proteinerna som införs med kosten men mer än 2 hektar erhålls från den normala omsättningen av proteiner som är en integrerad del av organismen ( aminosyror av dessa proteiner, som skadas av redoxprocesser, ersätts av andra och kataboliseras).
Aminosyror ger ett energibidrag när det gäller ATP: efter avlägsnande av a-aminogruppen kan det återstående kolhaltiga skelettet av aminosyror, efter lämpliga transformationer, komma in i krebscykeln. När tillgången på näringsämnen saknas och mängden glukos minskar, aktiveras glukoneogenes: glukoneogenetiska aminosyror sägs vara de som efter lämpliga modifieringar kan införas i glukoneogenesen; glukoneogenetiska aminosyror är de som kan omvandlas till pyruvat eller i fumarat (fumarat kan omvandlas till malat som lämnar mitokondrionen och i cytoplasman omvandlas till oxaloacetat från vilket fosfoenolpyruvat kan erhållas). vinäger-acetat.
Den som just beskrivits är en mycket viktig aspekt eftersom aminosyror kan avhjälpa en sockerbrist vid omedelbar fasta; om fastan kvarstår, efter två dagar ingriper lipidmetabolismen (eftersom proteinstrukturerna inte kan attackeras för mycket) är det i denna fas som, eftersom glukoneogenesen är mycket begränsad, omvandlas fettsyrorna till acetylkoenzym A och ketonkroppar. Från ytterligare fasta anpassar hjärnan sig också för att använda ketonkropparna.
Överföringen av a-aminogruppen från aminosyror sker genom en transamineringsreaktion; enzymerna som katalyserar denna reaktion, säger de faktiskt transaminaser (eller aminotransferas). Dessa enzymer använder en enzymatisk kofaktor som kallas pyridoxalfosfat, som intervenerar med dess aldehydgrupp. Pyridoxalfosfat är produkten av fosforyleringen av pyridoxin som är ett vitamin (B6) som främst finns i grönsaker.
Transaminaser har följande egenskaper:
Hög specificitet för ett ketoglutarat-glutamat-a-par;
De är uppkallade efter det andra paret.
Transaminase-enzymer involverar alltid paret a-ketoglutarat-glutamat och skiljer sig utifrån det andra paret som är inblandat.
Exempel:
L "aspartattransaminas dvs GOT (Glutamat-Ossalacetat Transaminas): enzymet överför a-aminogruppen från aspartat till a-ketoglutarat, erhållande av oxaloacetat och glutamat.
L "alanintransaminas dvs GTP (Glutamat-Pyruvat Transaminas): enzymet överför a-aminogruppen från "alanin till" a-ketoglutarat, erhållande av pyruvat och glutamat.
De olika transaminaserna använder a-ketoglurat som en acceptor för aminosyragruppen av aminosyror och omvandlar det till glutamat; medan aminosyrorna som bildas används i ketonkropparnas väg.
Denna typ av reaktion kan ske i båda riktningarna eftersom de bryts och bildar bindningar med samma energiinnehåll.
Transaminaserna finns både i cytoplasman och i mitokondrionen (de är mest aktiva i cytoplasman) och skiljer sig åt i sin isoelektriska punkt.
Transaminaserna kan också dekarboxylera aminosyror.
Det måste finnas ett sätt att konvertera glutamat tillbaka till α-ketoglutarat: detta görs genom deaminering.
där glutamatdehydrogenas det är ett enzym som kan omvandla glutamat till a-ketoglutarat och därför omvandla aminogrupperna i aminosyror som finns i form av glutamat till ammoniak. Det som sker är en redoxprocess som passerar genom mellanprodukten a-aminoglutarat: ammoniak och α-ketoglutarat frigörs och återgår till cirkulationen.
Därefter går deponeringen av aminosyrornas aminogrupper genom transaminaserna (som skiljer sig beroende på substratet) och glutamatdehydrogenaset, som bestämmer bildningen av ammoniak.
Det finns två typer av glutamatdehydrogenas: cytoplasmatisk och mitokondriell; kofaktorn, som också är underubstansen för detta enzym är NAD (P) +: glutamatdehydrogenas använder antingen NAD + eller NADP + som acceptor för reducerande effekt. Den cytoplasmatiska formen föredrar, men inte uteslutande, NADP + medan den mitokondriella formen föredrar NAD +. Den mitokondriella formen har till syfte att avyttra aminogrupper: den leder till bildandet av ammoniak (som är ett substrat för ett specialiserat enzym i mitokondrionen) och NADH (som skickas till andningskedjan). Den cytoplasmatiska formen fungerar i motsatt riktning, det vill säga den använder ammoniak och α-ketoglutarat för att ge glutamat (som har en biosyntetisk destination): denna reaktion är en reduktiv biosyntes och kofaktorn som används är NADPH.
Glutamatdehydrogenas fungerar när det är nödvändigt att avyttra aminogrupperna i aminosyror som ammoniak (via urin) eller när skelett av aminosyror behövs för att producera energi: detta enzym kommer därför att ha negativa modulatorer de system som är en indikation med god energitillgänglighet (ATP, GTP och NAD (P) H) och som positiva modulatorer, de system som indikerar ett behov av energi (AMP, ADP, BNP, NAD (P) +, aminosyror och sköldkörtelhormoner).
Aminosyror (huvudsakligen leucin) är positiva modulatorer av glutamatdehydrogenas: om aminosyror finns i cytoplasman kan de användas för proteinsyntes, eller de måste kasseras eftersom de inte kan ackumuleras (detta förklarar varför aminosyror är positiva modulatorer ).
Kassering av ammoniak: ureacykel
Fisk kasserar ammoniak genom att föra den i vatten genom gälarna; fåglar omvandlar den till urinsyra (som är en kondensationsprodukt) och eliminerar den med avföring. Låt oss se vad som händer hos människor: vi har sagt att glutamatdehydrogenas omvandlar glutamat i α- ketoglutarat och ammoniak men vi har inte sagt att detta bara sker i mitokondrier i levern.
En grundläggande roll för bortskaffande av ammoniak, genom ureacykeln, spelas av mitokondriella transaminaser.

Koldioxid, i form av bikarbonatjon (HCO3-), aktiveras av biotinkofaktorn som bildar karboxibiotin som reagerar med ammoniak för att ge karbaminsyra; nästa reaktion använder ATP för att överföra ett fosfat till den karbaminsyra som bildar karbamylfosfat och ADP (omvandlingen av ATP till ADP är drivkraften för att erhålla karboxybiotin.) Denna fas katalyseras av karbamylfosfatsyntetas och förekommer i mitokondrionen. Karbamylfosfat och ornitin är substrat för enzymet ornitintrans -karbamylas som omvandlar dem till citrullin; denna reaktion sker i mitokondrier (hepatocyter). Den producerade citrullinen lämnar mitokondrionen och går i cytoplasman under "verkan av"argininsuccinatsyntetas: det finns en sammansmältning mellan det kolhaltiga skelettet av citrullin och ett aspartat genom en nukleofil attack och efterföljande eliminering av vatten. Argininsuccinatsyntetasenzymet kräver en ATP -molekyl så det finns en energisk koppling: hydrolysen av ATP till AMP och pyrofosfat (det senare omvandlas sedan till två molekyler ortofosfat) sker genom utvisning av en molekyl d "vatten från substratet och inte genom verkan av vattnet i mediet.
"Nästa enzym är"argininsuccinas: detta enzym kan dela argininsuccinat till arginin och fumarat inom cytoplasman.
Ureacykeln slutförs av enzymet arginas: urea och ornitin erhålls; urea kasseras av njurarna (urinen) medan ornitin återvänder till mitokondrionen och återupptar cykeln.
Ureacykeln är föremål för indirekt modulering av arginin: ackumuleringen av arginin indikerar att ureacykeln måste påskyndas; moduleringen av arginin är indirekt eftersom arginin positivt modulerar acetylglutamatsyntetasenzymet. Den senare kan överföra en acetylgrupp på kvävet i ett glutamat: N-acetylglutamat bildas som är en direkt modulator av karbamyl-fosfo-syntetasenzymet.
Arginin ackumuleras som en metabolit i ureacykeln om produktionen av karbamylfosfat inte är tillräcklig för att avyttra ornitinet.
Urea produceras endast i levern men det finns andra platser där de första reaktionerna äger rum.
Hjärnan och musklerna använder speciella strategier för att eliminera aminogrupper. Hjärnan använder en mycket effektiv metod där ett enzym används glutaminsyntetas och ett enzym glutamas: den första finns i neuroner, medan den andra finns i levern. Denna mekanism är mycket effektiv av två skäl:
Två aminogrupper transporteras från hjärnan till levern i ett enda fordon;
Glutamin är mycket mindre giftigt än glutamat (glutamat utför också neuronal överföring och får inte överstiga den fysiologiska koncentrationen).
Hos fisk leder en liknande mekanism aminogruppen aminosyror till gälarna.
Från muskeln (skelett och hjärta) når aminogrupperna levern genom glukos-alanincykeln; enzymet som berörs är glutamin-pyruvat-transaminas: det möjliggör transposition av aminogrupper (som är i form av glutamat), omvandlar pyruvat till alanin och samtidigt glutamat till a-ketoglutarat i muskeln och katalyserar omvänd process i levern.
Transaminaser med olika uppgifter eller positioner har också strukturella skillnader och kan fastställas genom elektrofores (de har olika isoelektriska punkter).
Närvaron av transaminaser i blodet kan vara ett symptom på lever- eller hjärtskador (dvs. vävnadsskada på lever eller hjärtceller); transaminaserna är i mycket höga koncentrationer både i levern och i hjärtat: genom elektrofores är det möjligt att fastställa om skadan har inträffat i levern eller hjärtcellerna.