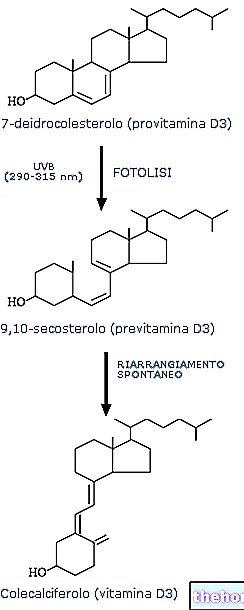
I naturen finns magnesium i form av föreningar och magnesiumsalter på grund av dess höga reaktivitet.
Om vi observerar den elektroniska konfigurationen av detta kemiska element noterar vi faktiskt närvaron av två elektroner i den yttersta banan; dessa elektroner överförs med viss lätthet till andra kemiska element som behöver elektroner för att slutföra sin yttre energinivå; magnesium berövas två elektroner är positivt laddade → magnesiumjon Mg ++; om vi istället observerar den elektroniska konfigurationen av kloret märker vi närvaron av sju elektroner i den yttre orbitalen; därför tenderar klor att girigt locka till sig en elektron för att fullborda oktetten; på detta sätt, när den saknade elektronen har förvärvats, tar den namnet klorjon Cl-. Här förklaras hur magnesiumklorid (Mg Cl2) bildas.

Efter denna korta kemiska nedbrytning, låt oss kort se hälsoegenskaperna hos de olika föreningarna och magnesiumsalterna.
Den första egenskapen att tänka på när man utvärderar en magnesiumförening ur hälsosynpunkt är mängden elementärt magnesium som finns i den; i det fall som rapporterats ovan är det uppenbart att ett gram magnesiumklorid innehåller en viss procentandel elementärt klor och en viss mängd elementärt magnesium.
Att veta hur mycket elementärt magnesium som finns i de olika föreningarna och salterna gör att vi kan veta mängden produkt som ska tas för att täcka det dagliga behovet av detta mineral.
(år)
(mg / dag)
(mg / dag)
(mg / dag)
(mg / dag)
Eftersom föreningarna och magnesiumsalterna ofta tas för att öka halterna av detta mineral inuti kroppen och fylla eventuella brister, verkar det logiskt att gå mot intag av föreningar och salter med ett högre elementärt magnesiuminnehåll. I verkligheten är denna aspekt underordnad till tarmens förmåga att absorbera magnesiumet i föreningen (se fördjupad analys). Av denna anledning, för att fylla specifika magnesiumbrister, är det viktigt att välja de bästa absorberbara källorna, medan för andra applikationer - som antacida eller laxerande effekt - föredras föreningar som inte absorberas signifikant av den mänskliga tarmen.
Generellt sett är de bäst absorberade magnesiumsalterna i vilka mineralet är bundet till organiska föreningar (glukonat, aspartat, pyruvat, malat, citrat, pidolat, laktat, orotat). Men även magnesiumklorid representerar en välabsorberbar källa, och - jämfört med de tidigare - har den fördelen med låg kostnad.Å andra sidan är de andra källorna till oorganiskt magnesium (magnesiumoxid, magnesiumkarbonat, magnesiumsulfat) föremål för stor kritik angående biotillgängligheten för magnesiumet som de innehåller. Tyvärr är de vetenskapliga studier som publicerats i ämnet fortfarande otillräckliga för att med säkerhet fastställa hälsoapplikationerna för de olika magnesiumföreningarna, med tanke på närvaron av ett litet antal undersökningar med ofta motstridiga resultat. Av den anledningen måste vad som följer - resultatet av omläsning av vetenskapliga artiklar och universitetstekster - beaktas med vederbörlig försiktighet.
Det anses vara ett välabsorberbart magnesiumsalt; till exempel har det i en studie visat sig absorberas 4,5 gånger bättre än den oorganiska föreningen Magnesiumoxid; närvaron av citrat kan vara användbart om det är nödvändigt att öka pH -värdet för urin, till exempel vid tendens till urinsyra och / eller cystinstenar
Det är framför allt känt för en studie som visade dess möjliga effekt vid behandling av premenstruellt syndrom, närvaron av pyruglataminsyra verkar ge detta salt neurosedativa effekter.
Organiskt salt tillskrivs en bättre tolerabilitet på mag -tarmnivå och en absorberbarhet jämförbar med andra organiska former; EFSA, den europeiska myndigheten som utvärderar livsmedelssäkerheten, har uttryckt oro över risken att orotsyra främjar bildandet av tumörer som initieras av olika kända cancerframkallande ämnen
Den är mycket löslig i vatten och verkar ha utmärkt absorberbarhet
Denna magnesiumkälla har den bästa vattenlösligheten av alla oorganiska former. Som olika studier har visat har den följaktligen en biotillgänglighet liknande eller i alla fall något lägre än de mest kända organiska salterna, med fördelen av en lägre kostnad. På marknaden, för specifika mineraltillskott, finns magnesiumklorid också i form av belagda tabletter för att förbättra gastrisk tolerans.
Även om det är den rikaste föreningen i elementärt magnesium, är det den som väcker den största kritiken mot möjligheten att absorberas av organismen.Dåligt lösligt i vatten, det har visat i flera studier en dålig biotillgänglighet jämfört med andra former av magnesium. är det troligt att de fina preparaten, som är mer lösliga i vatten, absorberas bättre än de med ett grövre korn.
Det används som antacida och laxermedel: det är till exempel en av de två aktiva ingredienserna i Maalox. Med tanke på den låga lösligheten i vatten tillskrivs det i allmänhet en låg biotillgänglighet, även om det i en studie har visat sig öka urinnivåerna av magnesium i jämförbar utsträckning till vissa organiska salter, såsom magnesiumcitrat.
Mycket olöslig i vatten och dåligt absorberbar av människokroppen, den används INTE i allmänhet som en källa till magnesium i kosttillskott eller förstärkta livsmedel. Den används snarare som antacida
Det används på sjukhus för intramuskulär eller intravenös administrering av magnesium. Det används också som ett laxermedel i höga doser (20 g), ofta under namnet engelskt salt eller Epsom salt. Biotillgängligheten för magnesiumet i detta salt, när det tas oralt, anses vara lågt