Aktiva ingredienser: Fingolimod
GILENYA 0,5 mg hårda kapslar
Varför används Gilenya? Vad är det för?
Vad är Gilenya
Den aktiva ingrediensen i Gilenya är fingolimod.
Vad Gilenya är till för
Gilenya används hos vuxna för behandling av multipel skleros (recidiverande remitterande multipel skleros), särskilt vid:
Patienter som inte har svarat på terapi med MS -behandling.
eller
Patienter med snabbt utvecklande svår MS.
Gilenya botar inte MS, men det hjälper till att minska antalet återfall och bromsa utvecklingen av fysisk handikapp som orsakas av MS.
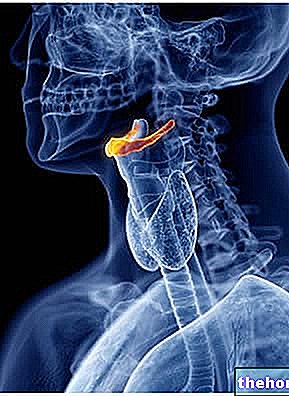
Vad är multipel skleros
MS är en kronisk sjukdom som påverkar centrala nervsystemet (CNS), som inkluderar hjärnan och ryggmärgen. Vid MS förstör inflammation det skyddande höljet (kallat myelin) som leder nerverna i CNS och hindrar nerverna från att fungera som de ska. Denna process kallas demyelinisering.
Återfallande remitterande MS kännetecknas av återfallande attacker (återfall) av neurologiska symptom som återspeglar ett inflammatoriskt tillstånd i centrala nervsystemet. Symtomen varierar från patient till patient, men innebär oftast svårigheter att gå, domningar, syn eller balansstörningar. Återfallssymtom kan försvinna helt när återfallet är över, men vissa klagomål kan kvarstå.
Hur Gilenya fungerar
Gilenya hjälper till att skydda nervsystemet från attacker av immunsystemet genom att minska förmågan hos vissa vita blodkroppar (lymfocyter) att cirkulera fritt i kroppen och förhindra att de når hjärnan och ryggmärgen. Detta begränsar nervskadorna som orsakas. Från MS.
Kontraindikationer När Gilenya inte ska användas
Ta inte Gilenya
- om du har nedsatt immunsvar (på grund av ett immunbristsyndrom, en sjukdom eller läkemedel som försämrar immunsystemet).
- om du har en allvarlig pågående infektion eller en kronisk pågående infektion som hepatit eller tuberkulos.
- om du har aktiv cancer (förutom om det är en typ av hudcancer som kallas basalcells hudcancer).
- om du har allvarliga leverproblem.
- om du är allergisk mot fingolimod eller något annat innehållsämne i detta läkemedel.
Om något av detta gäller dig, tala om för din läkare innan du tar Gilenya.
Försiktighetsåtgärder för användning Vad du behöver veta innan du tar Gilenya
Tala med din läkare innan du tar Gilenya:
- om du har en oregelbunden, onormal hjärtslag.
- om du upplever symtom på låg puls (t.ex. yrsel, illamående eller hjärtklappning).
- om du har några hjärtproblem, blockering av blodkärlen i ditt hjärta, tidigare har haft hjärtinfarkt eller hjärtstopp eller har angina.
- om du har haft en stroke tidigare.
- om du lider av hjärtsvikt.
- om du har allvarliga andningsproblem medan du sover (svår sömnapné).
- om du har fått veta att du har en onormal EKG.
- om du tar eller nyligen har tagit läkemedel mot oregelbunden hjärtslag som kinidin, disopyramid, amiodaron eller sotalol.
- om du tar eller nyligen har tagit läkemedel som bromsar hjärtslaget (t.ex. betablockerare, verapamil, diltiazem eller ivabradin, digoxin, antikolinesterasläkemedel eller pilokarpin).
- om du någonsin har haft episoder av plötslig medvetslöshet eller svimning (synkope).
- om du tänker vaccinera dig.
- om du aldrig har haft vattkoppor.
- om du har eller har haft synstörningar eller andra tecken på svullnad i det centrala synområdet (makula) på baksidan av ögat (ett tillstånd som kallas makulaödem, se nedan), om du har eller har haft en "inflammation eller" infektion i ögat (uveit) eller om du har diabetes (vilket kan orsaka ögonproblem).
- om du har leverproblem.
- om du har högt blodtryck som inte kan kontrolleras av läkemedel.
- om du har allvarliga lungproblem eller om du har hosta av rökning.
Om något av detta gäller dig, tala om för din läkare innan du tar Gilenya.
Långsam hjärtslag (bradykardi) och oregelbunden hjärtslag: I början av behandlingen orsakar Gilenya pulsen sänkning. Som ett resultat kan du uppleva yrsel eller trötthet, medvetenhet om ditt hjärtslag eller blodtrycksfall. Om dessa effekter uttalas kontakta din läkare, eftersom du kan behöva omedelbar behandling. Gilenya kan också orsaka oregelbunden hjärtslag, särskilt efter den första dosen. Oregelbunden hjärtslag återgår vanligtvis till det normala på mindre än ett dygn. Långsam puls återgår vanligtvis. återgår till det normala inom en månad .
Din läkare kommer att be dig att stanna på kliniken eller sjukhuset i minst 6 timmar efter administrering av den första dosen Gilenya, under vilken din puls och blodtryck kommer att mätas när som helst: på detta sätt kan lämpliga åtgärder vidtas om av biverkningar som uppstår i början av behandlingen. Du måste ha ett elektrokardiogram tillgängligt före den första dosen Gilenya och efter 6 timmars övervakning. Din läkare kan kontrollera ditt elektrokardiogram kontinuerligt under denna period. Om efter 6 timmar din hjärtfrekvens är mycket låg eller sjunker, eller om din EKG visar avvikelser kan du behöva observeras under en längre period (minst ytterligare 2 timmar och eventuellt till nästa morgon), tills dessa problem är lösta. Samma kan hända om hon tar G igen ilenya efter avbrott i behandlingen, beroende på hur länge avbrottet var och hur länge du har tagit Gilenya före avbrottet.
Om du har eller riskerar att få oregelbunden eller onormal hjärtslag, om ditt EKG är onormalt eller om du har hjärtsjukdom eller hjärtsvikt, kanske Gilenya inte är lämpligt för dig.
Om du någonsin har haft episoder av plötslig medvetslöshet eller nedsatt hjärtfrekvens kanske Gilenya inte passar dig. Du kommer att ses av en kardiolog (hjärtspecialist) som kommer att ge dig råd om hur du påbörjar din behandling med Gilenya, inklusive övervakning till nästa morgon.
Om du tar läkemedel som kan orsaka en minskning av hjärtfrekvensen kanske Gilenya inte passar dig. Du kommer att ses av en kardiolog som kommer att bedöma om du kan ta läkemedel som inte sänker din puls som ett alternativ, så att du kan börja behandlingen med Gilenya. Om denna förändring i terapi inte är möjlig kommer din kardiolog att ge dig råd om hur du påbörjar behandling med Gilenya, inklusive övervakning till nästa morgon.
Om du aldrig har haft vattkoppor: Om du aldrig har haft vattkoppor kommer din läkare att kontrollera din immunitet mot det virus som orsakar det (varicella zoster -virus). Om du inte är skyddad mot viruset kan du behöva vaccinera dig innan du påbörjar behandling med Gilenya. Om detta inträffar kommer din läkare att skjuta upp starten av Gilenya -behandlingen i upp till en månad efter att hela vaccinationskuren har slutförts.
Infektioner: Gilenya minskar antalet vita blodkroppar (särskilt lymfocyter). Vita blodkroppar bekämpar infektioner. När du tar Gilenya (och upp till 2 månader efter avslutad behandling) kan du lättare få infektioner. Varje befintlig infektion kan bli värre. Infektioner kan vara allvarliga och livshotande. Kontakta din läkare direkt ...
Makulaödem: Innan behandling påbörjas med Gilenya, om du har eller har haft synstörningar eller andra tecken på svullnad i det centrala synområdet (macula) på baksidan av ögat, om du har eller har haft ett "inflammation eller" infektionsöga (uveit) eller om du har diabetes kan din läkare be dig att göra en ögonundersökning.
Din läkare kan be dig att få en ögonundersökning 3-4 månader efter att behandlingen med Gilenya påbörjats.
Makula är ett litet område av näthinnan som ligger på baksidan av ögat som gör att du kan se former, färger och detaljer tydligt och skarpt. Gilenya kan orsaka svullnad av makula, ett tillstånd som kallas makulaödem. svullnad uppstår. vanligtvis under de första 4 månaderna av behandlingen med Gilenya.
Makulaödem är mer sannolikt att uppstå om du har diabetes eller har haft en "ögoninflammation" som kallas uveit. I dessa fall kommer din läkare att vilja kontrollera dig regelbundet för de första tecknen på makulaödem.
Om du har drabbats av makulaödem, tala med din läkare innan du börjar behandlingen med Gilenya igen.
Makulaödem kan orsaka några av de visuella symtomen (optisk neurit) som också uppstår under MS -attacker. I det första skedet kan det inte finnas några symtom. Var noga med att berätta för din läkare om eventuella synförändringar. Din läkare kan be dig att hänvisa till dem . genomgå en ögonundersökning, särskilt om:
- det centrala visningsområdet är ur fokus eller har skuggor;
- en blind fläck utvecklas i det centrala synområdet;
- har svårt att skilja färger eller fina detaljer.
Leverfunktionstester: Om du har allvarliga leverproblem ska du inte ta Gilenya. Behandling med Gilenya kan påverka din leverfunktion. Du kommer troligen inte att märka några symtom, men om du märker gulning av din hud eller ögonvitor, onormalt mörkt urin eller oförklarligt illamående och kräkningar, kontakta din läkare omedelbart.
Om du får något av dessa symtom efter påbörjad behandling med Gilenya, kontakta din läkare omedelbart.
Under de första tolv månaderna av behandlingen kommer din läkare att be dig ta blodprov för att kontrollera din leverfunktion. Om resultaten indikerar att det finns ett leverproblem kan behandlingen med Gilenya behöva avbrytas.
Högt tryck
Eftersom Gilenya orsakar en liten ökning av blodtrycket kan din läkare regelbundet kontrollera ditt blodtryck. Lungproblem Gilenya har en svag effekt på lungfunktionen. Biverkningar kan lättare uppstå hos patienter med allvarliga lungproblem eller hosta från rökning.
Blodtal Den önskade effekten av behandling med Gilenya är att minska mängden vita blodkroppar i blodet. Dessa återgår vanligtvis till det normala inom 2 månader efter avslutad behandling. Om du behöver ta blodprov, tala om för din läkare att du tar Gilenya .
Innan behandlingen påbörjas med Gilenya, kommer din läkare att bekräfta om ditt vita blodkroppar är tillräckligt och kan be dig att upprepa antalet regelbundet. Om du inte har tillräckligt med vita blodkroppar kan du behöva sluta ta Gilenya.
Posteriort reversibelt encefalopatisyndrom (PRES)
Ett syndrom som kallas posterior reversibel encefalopati (PRES) har sällan rapporterats hos patienter med multipel skleros som behandlats med Gilenya. Symtomen kan innefatta plötslig allvarlig huvudvärk, förvirring, anfall och synförändringar. Tala om för din läkare om något av dessa symtom uppstår under behandling med Gilenya.
Användning hos äldre
Erfarenhet av Gilenya hos äldre patienter över 65 år är begränsad. Fråga din läkare om du har ytterligare frågor.
Barn och ungdomar
Gilenya är inte avsett för barn och ungdomar under 18 år eftersom det inte har studerats hos MS -patienter under 18 år.
Interaktioner Vilka läkemedel eller livsmedel kan förändra effekten av Gilenya
Tala om för din läkare eller apotekspersonal om du tar, nyligen har tagit eller kan tänkas ta andra läkemedel. Tala om för din läkare om du tar någon av följande mediciner:
- Läkemedel som undertrycker eller modifierar immunsystemet, inklusive andra läkemedel som används för att behandla MS, såsom interferon beta, glatirameracetat, natalizumab, mitoxantron, teriflunomid, dimetylfumarat eller alemtuzumab. Du ska inte använda Gilenya med dessa läkemedel eftersom de kan förstärka effekten på immunsystemet (se även "Ta inte Gilenya").
- Kortikosteroider, på grund av den möjliga additiva effekten på immunsystemet.
- Vacciner. Om du behöver vaccinera dig, rådfråga din läkare först. Under och upp till 2 månader efter behandling med Gilenya ska du inte få vissa typer av vacciner (levande försvagade vacciner) eftersom de kan utlösa den infektion de skulle förhindra. Andra vacciner kanske inte fungerar lika bra som vanligt om de ges vid denna tidpunkt ...
- Läkemedel som bromsar hjärtslaget (t.ex. betablockerare, såsom atenolol). Samtidig användning av Gilenya med dessa läkemedel kan öka effekten på hjärtfrekvensen under de första dagarna av Gilenya -behandlingen.
- Läkemedel mot oregelbunden hjärtslag, såsom kinidin, disopyramid, amiodaron eller sotalol. Din läkare kan besluta att inte förskriva Gilenya om du tar dessa typer av läkemedel eftersom de kan förstärka effekten på oregelbunden hjärtslag.
- Andra läkemedel:
- proteashämmare, anti-infektionsmedel såsom ketokonazol, azol-svampmedel, klaritromycin eller telitromycin.
- karbamazepin, rifampicin, fenobarbital, fenytoin, efavirenz eller johannesört (potentiell risk för minskad effekt).
Varningar Det är viktigt att veta att:
Graviditet och amning
Innan behandlingen påbörjas med Gilenya kan din läkare be dig att göra ett graviditetstest för att säkerställa att du inte är gravid. När du tar Gilenya eller i två månader efter avslutad behandling bör du undvika att bli gravid eftersom det finns risk för skada på barnet. Tala med din läkare om pålitliga preventivmetoder att använda under behandlingen. Med Gilenya och i 2 månader efter att behandlingen har avslutats .
Om du blir gravid medan du tar Gilenya, avsluta behandlingen och tala omedelbart för din läkare. Din läkare bestämmer tillsammans med dig vad som är bäst för dig och ditt barn.
Amma inte när du tar Gilenya. Gilenya utsöndras i bröstmjölk med risk för allvarliga biverkningar för den nyfödda.
Fråga din läkare eller apotekspersonal om råd innan du tar något läkemedel.
Köra och använda maskiner
Din läkare kommer att berätta om din sjukdom gör att du kan köra bil och använda maskiner på ett säkert sätt. Gilenya förväntas inte påverka förmågan att framföra fordon och använda maskiner.
Men i början av behandlingen måste du stanna på din läkares kontor eller sjukhus i 6 timmar efter att du tagit den första dosen Gilenya. Förmågan att framföra fordon och använda maskiner kan försämras under denna tid och eventuellt längre fram.
Dosering och användningssätt Hur man använder Gilenya: Dosering
Behandling med Gilenya kommer att övervakas av en läkare med erfarenhet av behandling av multipel skleros.
Ta alltid detta läkemedel enligt läkarens anvisningar.
Kontakta din läkare om du är osäker. Dosen är en kapsel en gång om dagen. Ta Gilenya en gång om dagen med ett glas vatten. Gilenya kan tas med eller utan mat.
Att ta Gilenya vid samma tid varje dag hjälper dig att komma ihåg när du ska ta medicinen.
Överskrid inte den rekommenderade dosen.
Din läkare kan byta dig direkt från behandling med interferon beta, glatirameracetat eller dimetylfumarat till Gilenya om det inte finns några tecken på avvikelser som orsakats av tidigare behandling. Din läkare kan låta dig göra ett blodprov för att utesluta dessa abnormiteter. Efter avslutad behandling med natalizumab kan det vara nödvändigt att vänta 2-3 månader innan behandling med Gilenya påbörjas. För att byta från teriflunomid kan din läkare råda dig att vänta en viss tid eller fortsätta med en påskyndad eliminationsprocedur. Om du har behandlats med alemtuzumab krävs noggrann utvärdering och diskussion med din läkare för att avgöra om Gilenya är lämpligt för dig.
Fråga din läkare eller apotekspersonal om du är osäker på hur länge du kommer att ta Gilenya.
Överdosering Vad du ska göra om du har tagit för mycket Gilenya
Om du har tagit för stor mängd av Gilenya
Tala omedelbart för din läkare om du har tagit för många Gilenya -kapslar.
Om du har glömt att ta Gilenya
Om du har tagit Gilenya i mindre än 1 månad och glömt att ta 1 dos under en hel dag, tala med din läkare innan du tar nästa dos. Din läkare kan besluta att observera dig när du tar din nästa dos.
Om du har tagit Gilenya i minst en månad och har glömt att ta ditt läkemedel i mer än 2 veckor, tala med din läkare innan du tar din nästa dos. Din läkare kan besluta att observera dig när du tar din nästa dos.Men om du har glömt att ta din medicin i 2 veckor eller mindre kan du ta din nästa dos som planerat.
Ta aldrig en dubbel dos för att kompensera för en glömd dos.
Om du slutar att ta Gilenya
Sluta inte ta Gilenya eller ändra din dos utan att först tala med din läkare.
Gilenya kommer att förbli i kroppen i upp till 2 månader efter avslutad behandling. Antalet vita blodkroppar (lymfocyter) kan förbli lågt under denna tid och biverkningarna som beskrivs i denna bipacksedel kan fortfarande uppstå. Efter avslutad behandling med Gilenya kan det vara nödvändigt att vänta 6-8 veckor innan en ny behandling för multipel skleros påbörjas.
Om du behöver starta om Gilenya efter mer än 2 veckors behandlingstopp, kan den effekt på hjärtfrekvensen som normalt inträffar vid behandlingens början inträffa igen. Sjukhus under observation Starta inte om Gilenya efter att ha stoppat det i mer än två veckor utan att rådfråga din läkare.
Om du har ytterligare frågor om användningen av detta läkemedel, fråga din läkare eller apotekspersonal
Biverkningar Vilka är biverkningarna av Gilenya
Liksom alla läkemedel kan detta läkemedel orsaka biverkningar men alla användare behöver inte få dem.
Vissa biverkningar kan vara eller bli allvarliga
Vanliga (kan förekomma hos upp till 1 av 10 personer):
- Hosta med slem, obehag i bröstet, feber (tecken på lungsjukdomar)
- Herpesvirusinfektion (St. Anthony's fire eller herpes zoster), med symtom som blåsor, sveda, klåda eller smärta i huden, vanligtvis i överkroppen eller i ansiktet. Andra symtom kan vara feber och svaghet i de tidiga stadierna infektion, följt av domningar, klåda eller röda fläckar med svår smärta
- Långsam hjärtslag (bradykardi), oregelbunden hjärtrytm
Mindre vanliga (kan förekomma hos upp till 1 av 100 personer):
- Lunginflammation med symtom som feber, hosta, andningssvårigheter
- Makulaödem (svullnad i det centrala synområdet på näthinnan på baksidan av ögat) med symtom som skuggor eller blinda fläckar i synens centrum, dimsyn, problem med att skilja färger eller detaljer
Sällsynta (kan förekomma hos upp till 1 av 1000 personer):
- Ett syndrom som kallas posterior reversibel encefalopati. Symtomen kan innefatta plötslig allvarlig huvudvärk, förvirring, anfall och / eller synstörningar
Isolerade fall:
- Kryptokockinfektioner (en typ av svampinfektion), inklusive kryptokock meningit med symtom som huvudvärk åtföljt av stelhet i nacken, ljuskänslighet, illamående och / eller förvirring.
Tala omedelbart för din läkare om du får någon av dessa biverkningar.
Andra biverkningar
Mycket vanliga (kan förekomma hos fler än 1 av 10 personer):
- Influensavirusinfektion med symtom som trötthet, frossa, halsont, led- eller muskelsmärta, feber
- Känsla av tryck eller smärta i kinderna och pannan (bihåleinflammation)
- Huvudvärk
- Diarre
- Ryggont
- Blodprov som visar högre nivåer av leverenzymer
- Hosta
Vanliga (kan förekomma hos upp till 1 av 10 personer):
- Ringorm, en "svampinfektion i huden (pityriasis versicolor)
- Yrsel
- Allvarlig huvudvärk åtföljs ofta av illamående, kräkningar och ljuskänslighet (migrän)
- Låga nivåer av vita blodkroppar (lymfocyter, leukocyter)
- Svaghet
- Hudutslag med klåda, rodnad och sveda (eksem)
- Klåda
- Ökade nivåer av fetter (triglycerider) i blodet
- Håravfall
- Väsande andning
- Depression
- Dimsyn (se även avsnittet om "makulaödem" Vissa biverkningar kan vara eller bli allvarliga)
- Hypertoni (Gilenya kan orsaka en liten ökning av blodtrycket)
Mindre vanliga (kan förekomma hos upp till 1 av 100 personer):
- Låga nivåer av vissa vita blodkroppar (neutrofiler)
- Deppigt humör
Sällsynta (kan förekomma hos upp till 1 av 1000 personer):
- Blodkärlssjukdomar
- Störningar i nervsystemet
- Cancer i lymfsystemet (lymfom)
Ingen känd frekvens (kan inte beräknas utifrån tillgängliga data):
- Allergisk reaktion och hudutslag
Tala om för din läkare om någon av dessa biverkningar inträffar allvarligt.
Rapportering av biverkningar
Tala med din läkare eller apotekspersonal om du får några biverkningar. Detta inkluderar eventuella biverkningar som inte nämns i denna bipacksedel. Du kan också rapportera biverkningar direkt via det nationella rapporteringssystemet som anges i bilaga V. Genom att rapportera biverkningar kan du hjälpa till att ge mer information om säkerheten för detta läkemedel.
Giltighetstid och lagring
Förvara detta läkemedel utom syn- och räckhåll för barn.
Använd inte detta läkemedel efter utgångsdatum som anges på kartongen och blisterförpackningen efter "EXP" / "EXP". Utgångsdatumet avser den sista dagen i den månaden.
Förvaras vid högst 25 ºC.
Förvara i originalförpackningen för att skydda läkemedlet från fukt.
Använd inte förpackningar som är skadade eller visar tecken på manipulering.
Kasta inga läkemedel i avloppsvatten eller hushållsavfall. Fråga din apotekare om hur du ska kasta läkemedel som du inte längre använder. Detta hjälper till att skydda miljön.
Vad Gilenya innehåller
- Den aktiva ingrediensen är fingolimod. Varje kapsel innehåller 0,5 mg fingolimod (som hydroklorid).
- Övriga innehållsämnen är: Kapselinnehåll: magnesiumstearat, mannitol Kapselskal: gul järnoxid (E172), titandioxid (E171), gelatin Bläck: lack (E904), dehydratiserad alkohol, isopropylalkohol, butylalkohol, propylenglykol, renat vatten , koncentrerad ammoniaklösning, kaliumhydroxid, svart järnoxid (E172), gul järnoxid (E172), titandioxid (E171), dimetikon
Beskrivning av hur Gilenya ser ut och förpackningens innehåll
Gilenya 0,5 mg hårda kapslar har en ogenomskinlig vit ogenomskinlig kropp och en djup gul ogenomskinlig lock. Den svarta texten "FTY0,5mg" är graverad på huvudet och två gula band är graverade på kroppen.
Gilenya finns i förpackningar innehållande 7, 28 eller 98 kapslar, eller i flerförpackningar som innehåller 84 kapslar (3 förpackningar med 28 kapslar). Alla förpackningsstorlekar kanske inte marknadsförs.
Bipacksedel: AIFA (Italian Medicines Agency). Innehåll publicerat i januari 2016. Den information som finns finns kanske inte uppdaterad.
För att få tillgång till den senaste versionen är det lämpligt att gå till AIFA (Italian Medicines Agency) webbplats. Ansvarsfriskrivning och användbar information.
01.0 LÄKEMEDLETS NAMN
GILENYA 0,5 mg hårda kapslar
▼ Läkemedlet är föremål för ytterligare övervakning. Detta gör det möjligt att snabbt identifiera ny säkerhetsinformation. Vårdpersonal uppmanas att rapportera alla misstänkta biverkningar. Se avsnitt 4.8 för information om hur du rapporterar biverkningar.
02.0 KVALITATIV OCH KVANTITATIV SAMMANSÄTTNING
Varje hård kapsel innehåller 0,5 mg fingolimod (som hydroklorid).
För fullständig förteckning över hjälpämnen, se avsnitt 6.1.
03.0 LÄKEMEDELSFORM
Hård kapsel.
16 mm kapsel med intensivt gult ogenomskinligt lock och vit ogenomskinlig kropp; svart "FTY0,5 mg" gravering på huvudet och två gula cirkulära band graverade på kroppen.
04.0 KLINISK INFORMATION
04.1 Terapeutiska indikationer
Gilenya indikeras på egen hand som ett sjukdomsmodifierande läkemedel vid mycket aktiv återfallssjuka multipel skleros i följande vuxna patientgrupper:
- Patienter med hög sjukdomsaktivitet trots behandling med minst en behandling sjukdomsmodifierande (se avsnitt 4.4 och 5.1 för undantag och information om fiasko).
Dessa patienter kan definieras som de som inte har svarat på en fullständig och adekvat behandling (vanligtvis minst ett års behandling) med minst en behandling sjukdomsmodifierande. Patienter måste ha haft minst 1 återfall under föregående år under behandling och ha minst 9 T2 hyperintensiva skador på hjärnans MR eller minst 1 gadoliniumförstärkande lesion. En patient icke-svarare det kan också definieras som en patient som har en oförändrad eller ökad återfallshastighet jämfört med föregående år eller som har allvarliga återfall.
eller
-Patienter med snabbt utvecklande allvarlig återfallssänkande multipel skleros, definierad av två eller flera funktionshindrande återfall på ett år, och med 1 eller flera gadoliniumförstärkande lesioner på hjärnans MRI eller med en signifikant ökning av T2-lesionsbelastning jämfört med tidigare MRI nyligen utförd.
04.2 Dosering och administreringssätt
Behandlingen ska initieras och övervakas av en läkare med erfarenhet av multipel skleros.
Dosering
Den rekommenderade dosen Gilenya är en 0,5 mg kapsel som tas oralt en gång om dagen. Gilenya kan tas både under och bort från måltider.
Det rekommenderas att utföra samma övervakning som vid behandlingens början efter den första dosen om behandlingen avbryts för:
• 1 eller flera dagar under de två första behandlingsveckorna
• mer än 7 dagar under den tredje och fjärde behandlingsveckan
• mer än 2 veckor efter en månads behandling.
Om behandlingen avbryts är kortare än beskrivet ovan, ska behandlingen fortsätta med administrering av nästa dos som planerat (se avsnitt 4.4).
Särskilda populationer
Pensionärer
Gilenya ska användas med försiktighet till patienter 65 år och äldre eftersom det inte finns tillräckliga data om säkerhet och effekt (se avsnitt 5.2).
Nedsatt njurfunktion
I de viktigaste avgörande studierna vid multipel skleros har Gilenya inte studerats på patienter med nedsatt njurfunktion. Baserat på kliniska farmakologiska studier krävs ingen dosjustering hos patienter med lätt till svårt nedsatt njurfunktion.
Nedsatt leverfunktion
Gilenya får inte användas till patienter med allvarligt nedsatt leverfunktion (Child-Pugh klass C) (se avsnitt 4.3). Även om ingen dosjustering krävs hos patienter med lätt eller måttligt nedsatt leverfunktion, rekommenderas försiktighet när behandling påbörjas hos dessa patienter (se avsnitt 4.4 och 5.2).
Diabetespatienter
Gilenya har inte studerats hos patienter med multipel skleros och diabetes mellitus. Gilenya ska användas med försiktighet hos dessa patienter på grund av en möjlig ökad risk för makulaödem (se avsnitt 4.4 och 4.8). Dessa patienter bör genomgå regelbundna oftalmologiska undersökningar för tecken på makulaödem.
Pediatrisk population
Säkerhet och effekt för Gilenya för barn i åldrarna 0-18 år har ännu inte fastställts. För närvarande finns tillgängliga data beskrivna i avsnitt 5.2 men ingen rekommendation om dosering kan ges.
04.3 Kontraindikationer
- Diagnostiserat immunbristsyndrom.
- Patienter som har en ökad risk för opportunistiska infektioner, inklusive immunkompromitterade patienter (inklusive de som behandlas med samtidig immunsuppressiv behandling eller de som är immunkompromitterade av tidigare behandlingar).
- Allvarliga aktiva infektioner, kroniska aktiva infektioner (hepatit, tuberkulos).
- Diagnostiserade aktiva maligna tumörer, med undantag för patienter med basalcells hudcancer.
- Allvarligt nedsatt leverfunktion (Child-Pugh klass C).
- Överkänslighet mot den aktiva substansen eller mot något hjälpämne som anges i avsnitt 6.1.
04.4 Särskilda varningar och lämpliga försiktighetsåtgärder vid användning
Bradyarytmi
Inledande av behandling med Gilenya resulterar i en övergående minskning av hjärtfrekvensen och kan också vara förknippad med förseningar i atrioventrikulär ledning, inklusive isolerade episoder av fullständigt, övergående och spontant upplösande atrioventrikulärt block (se avsnitt 4.8 och 5.1).
Efter administrering av den första dosen börjar minskningen av hjärtfrekvensen inom en "timme och är maximal inom de första 6 timmarna. Under de följande dagarna kvarstår denna efterdoseffekt, även om den i allmänhet är av mindre intensitet, och minskar vanligtvis under de följande veckorna ... Med fortsatt dosering återgår medelpulsen till baslinjen inom en månad. I synnerhet kan patienter dock inte komma tillbaka till baslinjen i slutet av den första månaden. Konduktionsavvikelser har vanligtvis varit övergående och asymptomatiska. I allmänhet krävs ingen behandling och försvann inom de första 24 timmarna efter att behandlingen påbörjats. Om det behövs kan minskningen av hjärtfrekvensen som induceras av fingolimod reverseras genom parenteral administrering av doser av atropin eller isoprenalin.
Alla patienter ska ha ett elektrokardiogram och blodtrycksmätning före den första dosen Gilenya och efter 6 timmar. Alla patienter bör övervakas i 6 timmar för tecken och symtom på bradykardi, med pulsmätning och blodtrycksmätning per timme. Kontinuerlig (realtid) EKG-övervakning rekommenderas under dessa 6 timmar.
Om symtom på bradyarytmi uppstår efter administrering, bör lämpliga kliniska patienthanteringsprocedurer påbörjas och övervakningen fortsätta tills symptomen har försvunnit. Om en patient behöver farmakologiskt ingrepp under övervakningen efter den första dosen, ska övervakningen göras till nästa morgon på sjukhus och ska upprepas efter den andra dosen Gilenya.
Om hjärtfrekvensen i slutet av 6 timmar är det lägsta efter den första dosen (vilket tyder på att den maximala farmakodynamiska effekten på hjärtat ännu inte är uppenbar), ska övervakningen fortsätta i minst 2 timmar och tills hjärtat Ytterligare övervakning krävs också (åtminstone till nästa morgon och i alla fall tills symtomen försvinner) om pulsen efter 6 timmar efter administrering av den första dosen är slag per minut eller om elektrokardiogram visar nystartad andra grad eller högre atrioventrikulärt block, eller om QTc -intervallet är ≥500 msek. Uppkomsten av tredje graders atrioventrikulärt block när som helst måste också leda till en förlängning av övervakningen (åtminstone till följande morgon).
På grund av risken för allvarliga rytmstörningar ska Gilenya inte användas till patienter med andra gradens Mobitz typ II eller högre atrioventrikulärt block, hos patienter med sjukt sinus syndrom eller sino-förmaksblock, tidigare symtomatisk bradykardi eller återkommande synkope eller hos patienter med signifikant QT -förlängning (QTc> 470 msek (kvinnor) eller> 450 msek (män)). Eftersom signifikant bradykardi kan tolereras dåligt hos patienter med känd ischemisk hjärtsjukdom (inklusive angina pectoris), cerebrovaskulär sjukdom, hjärtinfarkt, kronisk hjärtsvikt, hjärtstopp, okontrollerad hypertoni eller svår sömnapné, bör Gilenya inte användas vid dessa patienter. Behandling med Gilenya bör endast övervägas hos dessa patienter om de förväntade fördelarna uppväger de potentiella riskerna. Om det beslutas att starta behandling med Gilenya, bör en kardiolog konsulteras innan behandlingen påbörjas för att definiera den lämpligaste övervakningen. Övervakning rekommenderas åtminstone till nästa morgon för behandlingens början (se även avsnitt 4.5).
Gilenya har inte studerats hos patienter med arytmier som kräver behandling med klass Ia (t.ex. kinidin, disopyramid) eller klass III (t.ex. amiodaron, sotalol) antiarytmika.Klass Ia och klass III antiarytmika har associerats med fall av torsades de pointes hos patienter med bradykardi. Eftersom behandlingen med Gilenya påbörjar en minskning av hjärtfrekvensen bör Gilenya inte användas samtidigt med dessa läkemedel.
Erfarenhet av Gilenya hos patienter i samtidig behandling med betablockerare, kalciumkanalblockerare som orsakar en minskning av hjärtfrekvensen (t.ex. verapamil, diltiazem eller ivabradin) eller med andra läkemedel som kan sänka hjärtfrekvensen (t.ex. digoxin, antikolinesterasläkemedel eller pilokarpin Eftersom initiering av Gilenya -behandling också är associerad med minskad hjärtfrekvens (se även avsnitt 4.8 Bradyarytmi), kan samtidig användning av dessa läkemedel vid initiering av Gilenya -behandling associeras med allvarlig bradykardi och hjärtblockering. På grund av de potentiella additiva effekterna på hjärtfrekvensen bör behandling med Gilenya inte påbörjas hos patienter som får dessa läkemedel (se även avsnitt 4.5). Hos dessa patienter ska behandling med Gilenya endast övervägas om de förväntade fördelarna uppväger de potentiella riskerna. Om behandling med Gilenya övervägs rekommenderas att en kardiolog konsulteras innan behandlingen påbörjas för att överväga att byta till andra läkemedel som inte orsakar en minskning av hjärtfrekvensen. Om det inte är möjligt att avbryta behandlingen med dessa läkemedel bör en kardiolog konsulteras för att definiera adekvat övervakning vid behandlingens början. Övervakning åtminstone till nästa morgon rekommenderas (se även avsnitt 4.5).
Beroende på varaktigheten av avbrottet och behandlingstiden (tiden mellan behandlingens början och dess avbrott) kan effekterna på hjärtfrekvensen och atrioventrikulär ledning återkomma när behandlingen med Gilenya startas om. Det rekommenderas att utföra samma övervakning som vid behandlingens början efter den första dosen om behandlingen avbryts för:
• 1 eller flera dagar under de två första behandlingsveckorna
• mer än 7 dagar under den tredje och fjärde behandlingsveckan
• mer än 2 veckor efter en månads behandling.
Om behandlingen avbryts är kortare än vad som beskrivits ovan, bör behandlingen fortsätta med administrering av nästa dos som planerat.
QT -intervall
I en grundlig QT -intervallstudie utförd med fingolimoddoser på 1,25 mg eller 2,5 mg, vid steady state (när den negativa kronotropa effekten av fingolimod fortfarande fanns), inducerade behandling med fingolimod förlängning av dosen. Korrigerat QT -intervall (QTc), med den övre gränsen för 90% konfidensintervall ≤ 13,0 ms. Inget dos-respons eller exponering-respons-korrelation observerades mellan fingolimod och QTc-intervallförlängning, varken som ett absolut värde eller som en förändring från baslinjen.
Den kliniska betydelsen av dessa fynd är okänd. Ingen kliniskt signifikant förlängning av QT -intervallet observerades i studier på patienter med multipel skleros, men patienter med risk att utveckla QT -intervallförlängning ingick inte i kliniska prövningar.
Läkemedel som kan förlänga QTc -intervallet bör undvikas hos patienter med betydande riskfaktorer, såsom hypokalemi eller medfödd förlängning av QT -intervallet.
Infektioner
En relevant farmakodynamisk effekt av Gilenya är den dosberoende minskningen av perifera lymfocytantal till 20-30% av utgångsvärdena. Detta beror på reversibel bindning av lymfocyter i lymfoida vävnader (se avsnitt 5.1).
Ett färskt blodantal (dvs. tagen inom 6 månader före eller efter avslutad tidigare behandling) bör finnas tillgängligt innan behandling med Gilenya påbörjas. Det rekommenderas också under behandlingen att utvärdera blodvärden regelbundet efter 3 månader och minst årligen därefter, och vid tecken på infektion. Ett absolut lymfocyttal på mindre än 0,2x109 / l, om det bekräftas, bör leda till avbrott. behandling tills det återgår till det normala, eftersom fingolimod avbröts i kliniska prövningar på patienter med absoluta lymfocytantal under 0,2x109 / l.
Behandlingsstart med Gilenya bör skjutas upp hos patienter med pågående allvarliga infektioner till återhämtning.
Patienter bör utvärderas med avseende på deras immunitetsstatus för vattkoppor innan behandling med Gilenya påbörjas. I avsaknad av en läkarbekräftad historia av vattkoppor eller bevis på en fullständig varicellavaccination, rekommenderas att patienter testas för antikroppar mot varicella-zoster-virus (VZV) innan behandling med Gilenya påbörjas. För patienter med en negativ antikroppstiter rekommenderas en fullständig vaccinationskurs mot varicella innan behandling med Gilenya påbörjas (se avsnitt 4.8). Behandlingsstart med Gilenya bör skjutas upp med 1 månad för att vaccinationen ska bli fullt effektiv.
Gilenyas effekter på immunsystemet kan öka risken för infektioner (se avsnitt 4.8). Effektiva diagnostiska och terapeutiska strategier bör implementeras hos patienter behandlade med Gilenya som uppvisar symptom på infektioner. Patienter bör instrueras att rapportera symptom på infektion till sin läkare under behandling med Gilenya.
Om en allvarlig infektion utvecklas hos en patient bör övervägande av behandlingen av Gilenya övervägas och nytta-risk-balansen bör bedömas innan behandlingen återupptas.
Eliminering av fingolimod efter avslutad behandling kan ta upp till två månader och därför bör infektionskontroll fortsätta under denna period. Patienter ska instrueras att rapportera symtom på infektion inom två månader efter att fingolimod avslutats.
Makulärt ödem
Makulaödem med eller utan synstörningar har rapporterats hos 0,5% av patienterna som behandlats med 0,5 mg fingolimod, främst under de första 3-4 månaderna av behandlingen (se avsnitt 4.8). En oftalmologisk utvärdering rekommenderas därför 3-4 månader efter behandlingsstart.Om patienter rapporterar synstörningar när som helst under behandlingen, bör en fundusundersökning inklusive macula utföras.
Patienter med tidigare uveit och patienter med diabetes har ökad risk att utveckla makulaödem (se avsnitt 4.8). Gilenya har inte studerats hos patienter med multipel skleros och samtidig diabetes mellitus. Det rekommenderas att patienter med multipel skleros och samtidig diabetes mellitus eller som tidigare har haft uveit genomgår en oftalmologisk utvärdering innan behandling påbörjas och uppföljningskontroller under behandlingen.
Fortsättning av Gilenya -behandling hos patienter med makulaödem har inte studerats. Det rekommenderas att behandlingen med Gilenya avbryts om makulaödem uppstår hos en patient. När man beslutar om behandlingen med Gilenya ska återupptas efter återhämtning eller inte, bör man överväga de potentiella fördelarna och riskerna för den enskilda patienten.
Leverfunktion
Förhöjningar av leverenzymer, särskilt alaninaminotransferas (ALT) men även gammaglutamyltranspeptidas (GGT) och aspartattransaminas (AST) har rapporterats hos patienter med multipel skleros som behandlats med Gilenya. I kliniska prövningar inträffade ALAT -förhöjningar ≥3 gånger den övre gränsen för normalområdet (ULN) hos 8,0% av patienterna som behandlades med fingolimod 0,5 mg jämfört med 1,9% av patienterna som behandlades med placebo .. Ökningar med 5 gånger den övre gränsen för normalintervallet förekom hos 1,8% av patienterna som behandlades med fingolimod och hos 0,9% av patienterna som behandlades med placebo.I kliniska prövningar avbröts behandlingen med fingolimod om ökningen var> 5 gånger den övre gränsen för det normala intervallet. Hos vissa patienter som återbehandlades efter avbrott uppträdde förhöjningar av levertransaminas igen, vilket bekräftade ett samband mellan denna ökning och läkemedlet. I kliniska studier inträffade förhöjningar av levertransaminaser när som helst under behandlingen, även om de flesta inträffade under de första 12 månaderna. Blodtransaminasnivåerna återgick till normala cirka 2 månader efter att fingolimod avbröts.
Gilenya har inte studerats hos patienter med befintligt allvarligt nedsatt leverfunktion (Child-Pugh klass C) och bör därför inte användas till dessa patienter (se avsnitt 4.3).
På grund av fingolimods immunsuppressiva egenskaper bör behandlingens början fördröjas hos patienter med aktiv viral hepatit tills den aktiva fasen har upphört.
Nya analyser (dvs under de senaste 6 månaderna) av transaminas- och bilirubinnivåer bör finnas tillgängliga innan behandling påbörjas med Gilenya. I avsaknad av kliniska symptom bör levertransaminasnivåer kontrolleras efter 1, 3, 6, 9 och 12 månader behandling och regelbundet därefter. Om levertransaminasnivåer når värden som överstiger 5 gånger normalgränsen (ULN), bör frekventa kontroller ordnas, inklusive kontroller av serumbilirubin och alkaliskt fosfatas (ALP) Om efter upprepade kontroller lever transaminasvärden förblir mer än 5 gånger normalgränsen (ULN), bör behandlingen med Gilenya avbrytas och startas om endast när levertransaminasvärdena har återgått till det normala.
Hos patienter som uppvisar symtom på nedsatt leverfunktion, såsom oförklarligt illamående, kräkningar, buksmärtor, trötthet, anorexi, gulsot och / eller mörk urin, bör leverenzymnivåer utvärderas; om signifikant leverskada bekräftas (t.ex. levertransaminasnivåer som överskrider den övre gränsen för det normala intervallet mer än 5 gånger och / eller ökningar i serumbilirubinnivåer), ska behandlingen med Gilenya avbrytas. Återupptagande av behandlingen beror på om en annan orsak till leverskada identifieras eller inte och patientens fördel med att återuppta behandlingen kontra risken för leversvikt återkommer.
Även om det inte finns några data som visar att patienter med befintlig leversjukdom har en ökad risk att utveckla förhöjda leverfunktionstester, bör försiktighet iakttas vid administrering av Gilenya till patienter med en historisk signifikant leversjukdom.
Interferens med serologiska analyser
Eftersom fingolimod minskar antalet blodlymfocyter genom att omfördela dem till sekundära lymfoida organ kan det inte användas för att bedöma lymfocytstatus för en patient som behandlats med Gilenya. Laboratorietester med användning av cirkulerande mononukleära celler kräver högre blodvolymer på grund av minskningen av antalet cirkulerande lymfocyter.
Effekter på blodtrycket
Patienter med icke-läkemedelskontrollerad hypertoni uteslöts från kliniska prövningar som genomfördes före marknadsföringen av Gilenya; Därför rekommenderas särskild uppmärksamhet om patienter med okontrollerad hypertoni behandlas med Gilenya.
I kliniska studier på patienter med multipel skleros var behandling med fingolimod 0,5 mg associerad med en genomsnittlig ökning av cirka 3 mmHg i systoliskt blodtryck och cirka 1 mmHg av diastoliskt blodtryck: dessa ökningar inträffade cirka 1 månad senare. Behandlingsstart och fortsatte med Fortsatt behandling I en tvåårig placebokontrollerad studie rapporterades hypertoni som en biverkning hos 6,5% av patienterna som behandlades med Gilenya 0,5 mg och hos 3,3% av patienterna som behandlades med placebo. Därför bör ditt blodtryck kontrolleras regelbundet under behandling med Gilenya.
Effekter på andningsorganen
Lätt dosberoende minskningar av forcerad utandningsvolym (FEV1) och diffusionskapacitet för kolmonoxid (Dlco) observerades under behandling med Gilenya, minskningar som inträffade under den första månaden och förblev stabila under behandlingen. Gilenya ska användas med försiktighet till patienter med allvarliga andningsbesvär, lungfibros och kronisk obstruktiv lungsjukdom (se avsnitt 4.8).
Posteriort reversibelt encefalopatisyndrom
Sällsynta fall av posteriort reversibelt encefalopatisyndrom (PRES) har rapporterats i kliniska prövningar och efter marknadsföring med 0,5 mg-dosen (se avsnitt 4.8). störningar och anfall Symtom på PRES är vanligtvis reversibla men kan utvecklas till ischemisk stroke eller hjärnblödning.
Tidigare behandling med immunsuppressiva eller immunmodulerande behandlingar
Inga studier har gjorts för att utvärdera Gilenyas effekt och säkerhet när patienter byter från teriflunomid, dimetylfumarat eller alemtuzumab till Gilenya. När patienter byter från annan behandling. sjukdomsmodifierande i Gilenya måste halveringstiden och verkningsmekanismen för den andra behandlingen beaktas för att undvika en additiv effekt på immunsystemet och samtidigt minimera risken för reaktivering av sjukdomen. fullständigt blodtal innan start behandling med Gilenya för att säkerställa att effekterna på immunsystemet som orsakats av tidigare behandling (t.ex. cytopeni) har löst sig.
Behandling med Gilenya kan vanligtvis påbörjas omedelbart efter att behandling med interferon eller glatirameracetat avbryts.
När det gäller dimetylfumarat är perioden av fiasko Det måste vara tillräckligt att återställa tillräckliga blodvärden innan behandling med Gilenya påbörjas.
På grund av natalizumabs långa halveringstid tar elimineringen i allmänhet upp till 2-3 månader efter avslutad behandling. Teriflumonid elimineras också långsamt från plasma. Utan ett påskyndat elimineringsförfarande kan clearance av teriflunomid från plasma ta från flera månader till 2 år. Det rekommenderas att utföra ett accelererat elimineringsförfarande enligt beskrivningen i produktresumén för teriflunomid, eller alternativt bör tvätttiden inte vara mindre än 3,5 månader. Försiktighet bör iakttas vid byte av patienter från natalizumab eller teriflunomidbehandling till Gilenya beträffande eventuella samtidiga effekter på immunsystemet.
Alemtuzumab har intensiva och långvariga immunsuppressiva effekter. Eftersom den verkliga varaktigheten av dessa effekter är okänd, rekommenderas det att inte påbörja behandling med Gilenya efter alemtuzumab såvida inte fördelarna med behandlingen för den enskilda patienten klart uppväger riskerna.
Beslutet att samadministrera långvariga kortikosteroidbehandlingar måste fattas efter noggrant övervägande.
Samtidig administrering med potenta CYP450 -inducerare
Fingolimod ska användas med försiktighet i kombination med potenta CYP450 -inducerare. Det rekommenderas att inte ge johannesört samtidigt (se avsnitt 4.5).
Avbrytande av behandlingen
Baserat på läkemedlets halveringstid, om ett beslut fattas att avbryta behandlingen med Gilenya, bör ett intervall på 6 veckor utan behandling lämnas så att fingolimod kan rensas från blodet (se avsnitt 5.2) .Lymfocyten räknar successivt återgår till normala värden inom 1-2 månader efter avslutad behandling (se avsnitt 5.1). Att starta andra behandlingar under detta tidsintervall resulterar i samtidig exponering för fingolimod. Användning av immunsuppressiva läkemedel strax efter att behandlingen med Gilenya avbrutits kan ha ytterligare effekt på immunsystemet och därför rekommenderas försiktighet.
04.5 Interaktioner med andra läkemedel och andra former av interaktion
Antineoplastiska, immunmodulerande eller immunsuppressiva behandlingar
Antineoplastiska, immunmodulerande eller immunsuppressiva behandlingar ska inte ges samtidigt på grund av risken för ytterligare effekter på immunsystemet (se avsnitt 4.3 och 4.4).
Försiktighet bör också iakttas när patienter påbörjar Gilenya-behandling efter avslutad behandling med långtidsverkande behandlingar med effekter på immunsystemet, såsom natalizumab eller mitoxantron (se avsnitt 4.4) I kliniska prövningar vid skleros. av kortikosteroider var inte associerad med en ökad infektionshastighet.
Vaccinationer
Vaccinationer kan vara mindre effektiva under behandlingen och upp till två månader efter avslutad behandling med Gilenya. Användning av levande försvagade vacciner kan utgöra en risk för infektioner och bör därför undvikas (se avsnitt 4.4 och 4.8).
Ämnen som framkallar bradykardi
Fingolimod studerades i kombination med atenolol och diltiazem.När fingolimod administrerades med atenolol i en interaktionsstudie på friska frivilliga, inträffade ytterligare 15% minskning av hjärtfrekvensen vid behandlingens början; denna effekt observerades inte med diltiazem. På grund av den potentiella additiva effekten. Hjärtfrekvens bör behandling med Gilenya inte initieras hos patienter som tar betablockerare eller andra läkemedel som kan sänka hjärtfrekvensen, såsom klass Ia och III-antiarytmika, kalciumkanalblockerare (t.ex. ivabradin, verapamil eller diltiazem), digoxin, antikolinesteraser eller pilokarpin (se avsnitt 4.4 och 4.8) Om behandling med Gilenya övervägs för dessa patienter bör en kardiolog konsulteras för att överväga att byta till andra läkemedel som inte orsakar sänkt hjärtfrekvens eller för att definiera adekvat övervakning i början av behandlingen. Om det inte är möjligt att avbryta behandlingen med läkemedel som sänker hjärtfrekvensen rekommenderas övervakning åtminstone till nästa morgon.
Förändringar i fingolimods farmakokinetik inducerade av andra ämnen
Fingolimod metaboliseras främst av CYP4F2. Andra enzymer som CYP3A4 kan också vara involverade i dess metabolisering, särskilt vid kraftig induktion av CYP3A4. Kraftiga hämmare av transportproteiner förväntas inte påverka beteendet hos fingolimod. Samtidig administrering av fingolimod och ketokonazol resulterade i en 1,7-faldig ökning av exponeringen (AUC) för fingolimod och fingolimodfosfat via hämning av CYP4F2. Försiktighet bör iakttas vid administrering av fingolimod med ämnen som kan hämma CYP3A4 (proteashämmare, azolantifungaler, vissa makrolider såsom klaritromycin eller telitromycin).
Samtidig administrering av karbamazepin 600 mg två gånger dagligen, nådde steady state och en engångsdos fingolimod 2 mg reducerade AUC för fingolimod och dess metabolit med cirka 40%Andra potenta inducerare av CYP3A4 -enzymet, såsom rifampicin, fenobarbital, fenytoin, efavirenz och johannesört, kan inducera en minskning av AUC för fingolimod och dess metabolit med åtminstone denna storlek. Eftersom detta kan försämra deras effekt bör försiktighet iakttas vid administrering i kombination. Samtidig administrering med johannesört rekommenderas dock inte (se avsnitt 4.4).
Förändringar i farmakologi för andra ämnen inducerade av fingolimod
Det är osannolikt att Fingolimod interagerar med ämnen som främst metaboliseras av CYP450 -enzymer eller substrat av viktiga bärarproteiner.
Samtidig administrering av fingolimod och cyklosporin resulterade inte i någon förändring i exponeringen för cyklosporin eller fingolimod.Fingolimod förväntas därför inte förändra farmakokinetiken för läkemedel som är substrat för CYP3A4.
Samtidig administrering av fingolimod med orala preventivmedel (etinylestradiol och levonorgestrel) resulterade inte i någon förändring i exponeringen för orala preventivmedel. Inga interaktionsstudier har gjorts med orala preventivmedel som innehåller gestagener, men en effekt av fingolimod på gestagen förväntas inte. till sådana droger.
04.6 Graviditet och amning
Kvinnor i fertil ålder / preventivmedel hos kvinnor
Innan behandling med Gilenya påbörjas bör kvinnor i fertil ålder informeras om eventuella allvarliga risker för fostret och om behovet av att använda effektiva preventivmedel under behandling med Gilenya. Eftersom det tar ungefär två månader efter avslutad behandling att rensa fingolimod från kroppen (se avsnitt 4.4), kan den potentiella risken för fostret finnas och därför måste preventivmedel fortsätta under den tiden.
Graviditet
Ett negativt graviditetstest måste finnas tillgängligt innan behandling påbörjas hos kvinnor i fertil ålder. Kvinnor ska inte bli gravida under behandlingen och effektivt preventivmedel rekommenderas. Om en kvinna blir gravid när hon tar Gilenya, rekommenderas att behandlingen avbryts.
Djurstudier har visat reproduktionstoxicitet, inklusive fosterförlust och organdefekter, särskilt ihållande artärstam och ventrikelseptaldefekt (se avsnitt 5.3) .Receptorn på vilken fingolimod verkar (sfingosin 1-fosfat) är involverad i kärlbildning under embryogenes. Det finns mycket begränsade data från användning av fingolimod hos gravida kvinnor.
Det finns inga data om effekterna av fingolimod på arbete och förlossning.
Matdags
Fingolimod utsöndras i mjölk från djur som behandlats under amning i koncentrationer 2-3 gånger högre än de som finns i moderns plasma (se avsnitt 5.3) På grund av risken för allvarliga biverkningar av fingolimod hos ammande barn, kvinnor i behandling med Gilenya ska inte amma.
Fertilitet
Data från prekliniska studier tyder inte på att fingolimod är förknippat med en ökad risk för försämrad fertilitet (se avsnitt 5.3).
04.7 Effekter på förmågan att framföra fordon och använda maskiner
Gilenya har ingen eller försumbar påverkan på förmågan att framföra fordon eller använda maskiner.
Ibland kan dock yrsel eller somnolens uppstå vid behandlingens början med Gilenya Det rekommenderas att patienter observeras i 6 timmar när behandling med Gilenya påbörjas (se avsnitt 4.4 Bradyarytmi).
04.8 Biverkningar
Sammanfattning av säkerhetsprofilen
Säkerhetspopulationen för Gilenya härrör från två fas III placebokontrollerade kliniska prövningar och en aktivt kontrollerad fas III klinisk studie som utförts på patienter med återfallssänkande multipel skleros. Den omfattar totalt 2 431 patienter som behandlats med Gilenya (0,5 eller 1,25 mg). I den 2-åriga placebokontrollerade kliniska studien D2301 (FREEDOMS) behandlades 854 patienter (placebo: 418 patienter) med fingolimod. I den 2-åriga, placebokontrollerade studien D2309 (FREEDOMS II) behandlades 728 patienter med multipel skleros (placebo: 355 patienter) med fingolimod. Samlade resultat från dessa två studier indikerar att de allvarligaste biverkningarna som inträffade med Gilenya 0,5 mg var infektioner, makulaödem och övergående atrioventrikulärt block i början av behandlingen.De vanligaste biverkningarna (incidens ≥ 10%) som inträffade med Gilenya 0,5 mg var influensa, bihåleinflammation, huvudvärk, diarré, ryggsmärta, förhöjda leverenzymer och hosta. Den vanligaste biverkningen med Gilenya 0,5 mg som ledde till "avbrytande av behandlingen var" ökade ALAT-nivåer i blodet (2,2%). I 1-års studie D2302 (TRANSFORMS) som involverade 849 patienter som behandlats med fingolimod och som använde interferon beta-1α som en kontroll, de biverkningar som inträffade var i allmänhet liknande dem i de placebokontrollerade studierna, med beaktande av den olika studiens varaktighet.
Biverkningar som rapporterats för Gilenya 0,5 mg i studierna D2301 (FREEDOMS) och D2309 (FREEDOMS II) listas nedan. Frekvenskategorier definieras med följande konvention: mycket vanligt (≥1 / 10); vanliga (≥1 / 100,
Sammanfattningstabell över biverkningar
* Rapporteras inte i FREEDOMS-, FREEDOMS II- och TRANSFORMS -studier. Händelsefrekvenskategorisering baserades på en uppskattad "fingolimod -exponering av cirka 10 000 patienter i alla kliniska prövningar."
Beskrivning av vissa specifika biverkningar
Infektioner
I kliniska prövningar på patienter med multipel skleros var den totala infektionshastigheten (65,1%) som rapporterades med dosen 0,5 mg liknande den som observerades med placebo. Emellertid var infektioner i nedre luftvägarna, främst bronkit och i mindre utsträckning herpetiska infektioner och lunginflammation, vanligare hos patienter som behandlats med Gilenya.
Några fall av spridd herpetisk infektion, inklusive dödliga fall, har rapporterats även med dosen 0,5 mg.
Makulärt ödem
I kliniska studier på patienter med multipel skleros förekom makulaödem hos 0,5% av patienterna som behandlades med den rekommenderade dosen 0,5 mg och hos 1,1% av patienterna som behandlades med den högre dosen (1, 25 mg). De flesta fallen inträffade under de första 3-4 månaderna av behandlingen. Vissa patienter rapporterade dimsyn och minskad synskärpa, andra var asymptomatiska och diagnosen ställdes under ett rutinmässigt oftalmologiskt besök. Makulaödem förbättrades eller försvann i allmänhet spontant efter avslutad behandling. Risken för återfall efter återexponering för behandling har inte studerats .
Förekomsten av makulaödem ökar hos patienter med multipel skleros som tidigare har haft uveit (17% med uveit jämfört med 0,6% utan uveit). Gilenya har inte studerats hos patienter med multipel skleros och diabetes mellitus. sjukdom i samband med ökad risk för makulaödem (se avsnitt 4.4) I kliniska studier på njurtransplanterade patienter inklusive patienter med diabetes mellitus, resulterade behandling med fingolimod 2,5 mg och 5 mg i ökad dubbelt så hög förekomst av makulaödem.
Bradyarytmi
Inledande av behandling med Gilenya resulterar i en övergående minskning av hjärtfrekvensen och kan också vara förknippad med förseningar i atrioventrikulär ledning. I kliniska prövningar på patienter med multipel skleros observerades den maximala minskningen av hjärtfrekvensen inom de första 6 timmarna efter operationen. " behandling påbörjas, med minskning av frekvensen med i genomsnitt 12-13 slag per minut under behandling med Gilenya 0,5 mg. En minskning av hjärtfrekvensen under 40 slag per minut har sällan observerats hos patienter som behandlats med Gilenya 0,5 mg. Medelpuls återgick till baslinjen inom 1 månad efter fortsatt behandling. Bradykardi var generellt asymptomatisk, men vissa patienter upplevde milda till måttliga symtom, inklusive hypotoni, yrsel, trötthet och / eller hjärtklappning, som försvann inom de första 24 timmarna efter behandlingens början (se även avsnitt 4.4 och 5.1).
I kliniska studier på patienter med multipel skleros observerades första gradens atrioventrikulärt block (förlängning av PR-intervallet till EKG) hos 4,7% av patienterna som behandlades med fingolimod 0,5 mg, hos 2,8% av patienterna. Patienter som behandlades med intramuskulärt interferon beta-1α och hos 1,6% av patienterna som behandlats med placebo. Andra gradens atrioventrikulärt block har rapporterats hos mindre än 0,2% av patienterna som behandlats med Gilenya 0,5 mg. Efter marknadsföring har isolerade episoder av övergående, spontant upplösande fullständigt atrioventrikulärt block rapporterats under 6 timmars övervakning efter den första dosen Gilenya. Erfarenhet efter marknadsföring var vanligtvis övergående, asymptomatisk och försvann inom de första 24 Även om inga medicinska ingrepp krävdes för de flesta patienter, gav en patient som behandlades med Gilenya 0, 5 mg isoprenalin efter en asymptomatisk episod av andra gradens Mobitz typ 1 atrioventrikulärt block.
Efter marknadsföring uppstod isolerade händelser med sen debut, inklusive övergående asystol och oförklarlig död, inom 24 timmar efter administrering av den första dosen. Utvärdering av dessa fall kompliceras av närvaron av samtidiga läkemedel och / eller redan existerande tillstånd Korrelationen mellan dessa händelser med Gilenya är osäker.
Blodtryck
I kliniska studier på patienter med multipel skleros var behandling med Gilenya 0,5 mg associerad med en genomsnittlig ökning av systoliskt blodtryck på cirka 3 mmHg och diastoliskt blodtryck på cirka 1 mmHg: dessa ökningar inträffade cirka 1 månad senare. Behandlingsstart och bibehölls med fortsatt behandling Hypertoni rapporterades hos 6,5% av patienterna som behandlades med fingolimod 0,5 mg och hos 3,3% av patienterna som behandlades med placebo. fall av hypertoni som kan kräva behandling med antihypertensiva läkemedel eller avbrytande av Gilenya har rapporterats inom den första månaden och den första behandlingsdagen (se även avsnitt 4.4 Effekter på blodtrycket).
Leverfunktion
Förhöjningar av leverenzymer har rapporterats hos patienter med multipel skleros som behandlats med Gilenya. I kliniska studier observerades asymtomatisk förhöjning av ALAT-nivåerna i blodet ≥3 gånger och ≥5 gånger den övre gränsen för normalintervall (ULN) hos 8,0% respektive 1,8% av patienterna som behandlades med Gilenya. 0,5 mg. behandling efter avbrott uppträdde förhöjda levertransaminas igen, vilket bekräftade ett samband mellan denna ökning och läkemedlet.I kliniska prövningar inträffade förhöjningar av levertransaminaser när som helst under behandlingen, även om de flesta inträffade under de första 12 månaderna.ALAT -nivåerna återvände till normala cirka 2 månader efter avslutad behandling med Gilenya. Hos ett litet antal patienter (N = 10 vid dosen 1,25 mg, N = 2 vid dosen 0,5 mg), som upplevde ALAT -förhöjningar ≥5 gånger den övre gränsen för normalområdet och som fortsatte behandlingen med Gilenya, ALT -värden återgått till det normala inom cirka 5 månader (se även avsnitt 4.4 Leverfunktion).
Nervsystemet
I kliniska studier har sällsynta händelser som involverar nervsystemet, inklusive ischemisk och hemorragisk stroke och atypiska neurologiska störningar, t.ex. t.ex. händelser som liknar akut disseminerad encefalomyelit (EAD).
Vaskulära patologier
Sällsynta fall av perifer artärsjukdom har inträffat hos patienter som behandlats med fingolimod vid högre doser (1,25 mg).
Andningssystem
Lätt dosberoende minskningar av forcerad utandningsvolym (FEV1) och diffusionskapacitet för kolmonoxid (Dlco) observerades under behandling med Gilenya, minskningar som inträffade under den första månaden och förblev stabila under behandlingen. Vid månad 24 var den procentuella minskningen från baslinjen i förväntad FEV1 2,7% för fingolimod 0,5 mg och 1,2% för placebo, en skillnad som försvann efter att behandlingen avbröts. Dlco -minskningarna vid månad 24 var 3,3% för fingolimod 0,5 mg och 2,7% för placebo.
Lymfom
Fall av olika typer av lymfom har rapporterats i både kliniska prövningar och efter marknadsföring, inklusive ett dödligt fall av Epstein-Barr-virus (EBV) positivt B-celllymfom. Förekomst av lymfomfall (B-cell och T-cell ) var högre i kliniska studier än förväntat i den allmänna befolkningen.
Hemofagocytiskt syndrom
Mycket sällsynta fall av hemofagocytiskt syndrom har rapporterats (Hemofagocytiskt syndrom, HPS) med dödlig utgång hos patienter behandlade med fingolimod i samband med en "infektion." HPS är ett sällsynt tillstånd som har beskrivits i samband med infektioner, immunsuppression och en mängd olika autoimmuna sjukdomar.
Rapportering av misstänkta biverkningar
Rapportering av misstänkta biverkningar som inträffar efter godkännande av läkemedlet är viktigt eftersom det möjliggör kontinuerlig övervakning av läkemedlets nytta / riskbalans.Hälso- och sjukvårdspersonal uppmanas att rapportera alla misstänkta biverkningar via det nationella rapporteringssystemet. I "bilaga V .
04.9 Överdosering
Enstaka doser upp till 80 gånger den rekommenderade dosen (0,5 mg) tolererades väl hos friska frivilliga. Vid 40 mg -dosen rapporterade 5 av de 6 försökspersonerna om svag brösttäthet eller sjukdomskänsla som var kliniskt relaterad till luftvägsreaktivitet.
Fingolimod kan framkalla bradykardi i början av behandlingen, minskningen av hjärtfrekvensen sker vanligtvis inom en timme efter den första dosen och är maximal inom de första 6 timmarna. Den negativa kronotropa effekten av Gilenya kvarstår längre än 6 timmar och avtar gradvis under de följande behandlingsdagarna (se avsnitt 4.4 för ytterligare detaljer) .Det har rapporterats att atrioventrikulär ledning saktar ner, med isolerade rapporter om atrioventrikulärt block. Komplett, övergående och spontan upplösning (se avsnitt 4.4 och 4.8).
Om överdosen sammanfaller med den första exponeringen för Gilenya är det viktigt att ha patienten kontinuerlig (realtid) elektrokardiografisk övervakning med pulsmätning per timme och blodtryck, åtminstone under de första 6 timmarna (se avsnitt 4.4).
Ytterligare övervakning krävs också (åtminstone fram till nästa morgon och i alla fall tills symtomen försvinner) om pulsen efter 6 timmar efter administrering av den första dosen
Fingolimod elimineras inte genom varken dialys eller plasmaferes.
05.0 FARMAKOLOGISKA EGENSKAPER
05.1 Farmakodynamiska egenskaper
Farmakoterapeutisk grupp: selektiva immunsuppressiva medel.
ATC -kod: L04AA27.
Handlingsmekanism
Fingolimod är en sfingosin-1-fosfat (S1P) receptormodulator. Med hjälp av sfingosinkinas omvandlas fingolimod till den aktiva metaboliten fingolimodfosfat som vid låga nanomolära koncentrationer binder till S1P1-receptorn på lymfocytytan och lätt korsar blod-hjärnbarriären för att binda till receptorn i centrala nervsystemet system S1P1 placerat på cellerna i centrala nervsystemet. Fingolimodfosfat, som fungerar som en funktionell antagonist av S1P -receptorer uttryckta på lymfocyter, hämmar lymfocyternas förmåga att fly från lymfkörtlarna, vilket resulterar i omfördelning snarare än förstörelse av lymfocyterna. Denna omfördelning minskar infiltrationen av patogena lymfocyter i centrala nervsystemet, där de är inblandade i nervinflammation och vävnadsskada. Djurstudier och experiment in vitro indikerar att fingolimod också kan verka genom att interagera med S1P -receptorer uttryckta på celler i centrala nervsystemet.
Farmakodynamiska effekter
Inom 4-6 timmar efter den första administreringen av fingolimod 0,5 mg reduceras antalet lymfocyter i det perifera blodet till cirka 75% av basvärdet. Fortsatt med den dagliga administreringen fortsätter antalet lymfocyter att minska i två veckor och nå ett minimivärde på cirka 500 celler / mikroliter, eller cirka 30% av basvärdet. 18% av patienterna nådde ett minimivärde under 200 celler / mikroliter minst en gång. Med kontinuerlig daglig behandling förblir antalet lymfocyter lågt. De flesta T- och B -lymfocyter migrerar regelbundet genom lymfoidorganen: fingolimod verkar huvudsakligen på dessa celler. Ungefär 15-20% av T-lymfocyterna har en TEM (minne-effektor) fenotyp: dessa celler är viktiga för perifer immunövervakning. Eftersom denna typ av lymfocyter i allmänhet inte migrerar till lymfoida organ, verkar fingolimod inte på dessa celler. Ökningen av antalet perifera lymfocyter är tydlig under dagarna efter att behandlingen med fingolimod avbrutits; lymfocytantal återgår vanligtvis till det normala inom en till två månader. Kronisk administrering av fingolimod resulterar i en liten minskning av antalet neutrofiler motsvarande cirka 80% av basvärdet.Fingolimod verkar inte på monocyter.
Fingolimod orsakar en övergående minskning av hjärtfrekvensen och minskad atrioventrikulär ledning vid behandlingens början (se avsnitt 4.4 och 4.8). 70% av den negativa kronotropa effekten. Med efterföljande administreringar återgår pulsen till baslinjen inom en månad. Minskningen av hjärtfrekvensen inducerad av fingolimod kan reverseras genom parenteral administrering av atropin eller isoprenalin. Inhalerad salmeterol har också visat sig ha en blygsam positiv kronotrop effekt. Vid påbörjad behandling med fingolimod ökar för tidiga förmakskontraktioner, men det finns ingen ökad förmaksflimmer / fladdrande eller ventrikulär arytmi eller ektopi. Behandling med fingolimod resulterar inte i minskad hjärteffekt och påverkar inte hjärtets sympatomimetiska svar, inklusive variation i dagspuls och svar på ansträngning.
Behandling med fingolimod, enstaka eller upprepade doser på 0,5 mg och 1,25 mg i två veckor, resulterar inte i en märkbar ökning av luftvägsresistens mätt som FEV1 och Forced Expiratory Flow (FEF) 25-75. Med enstaka doser av fingolimod ≥5 mg (10 gånger den rekommenderade dosen) uppstår dock en dosberoende ökning av luftvägsresistensen. Behandling med upprepade doser av fingolimod på 0,5 mg, 1,25 mg eller 5 mg resulterar inte i nedsatt syresättning eller syredesaturation under träning eller ökad luftvägsrespons på metakolin.Personer som behandlas med fingolimod svarar med normal bronkodilatation till inhalerade beta-agonister.
Klinisk effekt och säkerhet
Effekten av Gilenya visades i två studier som utvärderade en gång dagligen administrering av fingolimod 0,5 mg och 1,25 mg hos patienter med återfallssänkande multipel skleros (RRMS). ≥1 återfall under föregående år. Poängen på Expanded Disability Status Scale (EDSS) var 0-5,5. En tredje studie utförd i samma patientpopulation slutfördes efter Gilenyas registrering.
I den 2-åriga, randomiserade dubbelblinda kontrollerade placebokontrollerade studien D2301 (FREEDOMS) inkluderades 1272 patienter (n = 425 behandlade med fingolimod 0,5 mg, 429 med fingolimod 1,25 mg, 418 med placebo). Medianvärden för baslinjekarakteristika var: 37 år, sjukdomstid 6,7 år, EDSS -poäng på 2,0. Resultaten presenteras i tabell 1. Det fanns inga signifikanta skillnader mellan doserna 0,5 mg och 1,25 mg för alla slutpunkter.
Tabell 1: Studie D2301 (FREEDOMS): Huvudresultat
† Handikappens utveckling definieras som en 1-punkts ökning av EDSS bekräftad efter 3 månader
** s
Alla kliniska slutpunkter utvärderades genom analys avsikt att behandla. Analyser relaterade till MR -data använde utvärderbara datamängder.
Patienter som hade avslutat fasen kärna av 24-månaders FREEDOMS-studien kunde gå in i den dosblinda förlängningsfasen (D2301E1) och få fingolimod. Totalt kom 920 patienter in (n = 331 fortsatte med 0,5 mg dosen, 289 vid dosen 1,25 mg, 155 bytte från placebo till 0,5 mg och 145 från placebo till 1,25 mg). Efter 12 månader (månad 36) var 856 patienter (93%) fortfarande inskrivna. Mellan månad 24 och månad 36, den årliga återfallshastigheten (ARR) för patienter som får fingolimod 0,5 mg i fas kärna av studien och som hade fortsatt med samma dos (0,5 mg) var 0,17 (0,21 i fas kärna av studier). Den årliga återfallsfrekvensen för patienter som bytte från placebo till fingolimod 0,5 mg var 0,22 (0,42 i fas kärna av studier).
Liknande resultat erhölls i en fas III, 2-årig, randomiserad, dubbelblind placebokontrollerad studie (D2309; FREEDOMS 2) utförd på 1083 patienter med återfallssänkande multipel skleros (n = 358 behandlade med fingolimod 0, 5 mg, 370 med fingolimod 1,25 mg, 355 med placebo). Medianvärden för baslinjeegenskaper var: ålder 41 år, sjukdomstid 8,9 år, EDSS -poäng på 2,5.
Tabell 2: Studie D2309 (FREEDOMS 2): Huvudresultat
† Handikappens utveckling definieras som en 1-punkts ökning av EDSS bekräftad efter 3 månader
** s
Alla kliniska slutpunkter utvärderades genom analys avsikt att behandla. Analyser relaterade till MR -data använde utvärderbara datamängder.
I studie D2302 (TRANSFORMS), fas III, varar 1 år, randomiserad, dubbelblind kontrollerad och dubbel-dummy kontra aktivt läkemedel (interferon beta-1α) inkluderades 1280 patienter (n = 429 behandlade med fingolimod 0,5 mg, 420 med fingolimod 1,25 mg, 431 med intramuskulär injektion av interferon beta-1α i en dos av 30 mikrogram en gång per vecka). Medianvärden för baslinjekarakteristika var: ålder 36 år, sjukdomstid 5,9 år, EDSS -poäng på 2,0. Studieresultaten presenteras i tabell 3. Det fanns ingen signifikant skillnad mellan doserna 0,5 mg och 1,25 mg med avseende på studiens slutpunkter.
Tabell 3: Studie D2302 (TRANSFORMS): Huvudresultat
† Handikappens utveckling definieras som en 1-punkts ökning av EDSS bekräftad efter 3 månader
** s
Alla kliniska slutpunkter utvärderades genom analys avsikt att behandla. Analyser relaterade till MR -data använde utvärderbara datamängder.
Patienter som hade avslutat fasen kärna av 12-månaders TRANSFORMS-studien kunde gå in i den dosblinda förlängningsfasen (D2302E1) och få fingolimod. Totalt kom 1 030 patienter in, men 3 av dessa fick ingen behandling (n = 356 fortsatte med 0,5 mg dosen, 330 vid dosen 1,25 mg, 167 bytte från interferon beta-1α till 0, 5 mg och 174 från interferon beta -1α vid 1,25 mg). Efter 12 månader (månad 24) var 882 patienter (86%) fortfarande inskrivna. Mellan månaderna 12 och 24, den årliga återfallshastigheten (ARR) för patienter som fick fingolimod 0,5 mg i fas kärna av studien och som hade fortsatt med samma dos (0,5 mg) var 0,20 (0,19 i fas kärna av studier). Den årliga återfallsfrekvensen för patienter som bytte från interferon beta-1α till fingolimod 0,5 mg var 0,33 (0,48 i fas kärna av studier).
Samlade resultat från studierna D2301 och D2302 visade en konsekvent och statistiskt signifikant minskning från kontrollen av den årliga återfallsfrekvensen i undergrupper definierade av kön, ålder, tidigare MS -terapi, sjukdomsaktivitet eller funktionshinder vid baslinjen.
Ytterligare analys av kliniska prövningsresultat visar signifikanta behandlingseffekter i undergrupper av patienter med mycket aktiv återfallssänkande multipel skleros.
Europeiska läkemedelsmyndigheten har skjutit upp skyldigheten att lämna in resultaten av studier med Gilenya i en eller flera undergrupper av den pediatriska populationen vid multipel skleros (se avsnitt 4.2 för information om pediatrisk användning).
05.2 "Farmakokinetiska egenskaper
Farmakokinetiska data erhölls från friska frivilliga, njurtransplanterade patienter och patienter med multipel skleros.
Den farmakologiskt aktiva metaboliten som är ansvarig för effekten är fingolimodfosfat.
Absorption
Absorption av fingolimod sker långsamt (Tmax på 12-16 timmar) och är omfattande (≥85%). Den uppenbara absoluta biotillgängligheten efter oral administrering är 93%(konfidensintervall: 79-111%). Koncentrationer blod vid stabilt läge uppnås inom 1 till 2 månader efter administrering av enstaka dagliga doser av fingolimod och allo -nivåer stabilt läge de är cirka 10 gånger högre än de som ses med startdosen.
Matintag förändrar inte toppkoncentrationen (Cmax) eller systemisk exponering (AUC) för fingolimod. Fingolimodfosfat Cmax ökade något med 34% medan AUC var oförändrad. Därför kan Gilenya tas antingen på full eller tom mage (se avsnitt 4.2).
Distribution
Fingolimod distribueras snabbt i röda blodkroppar och finns i 86% av blodkropparna. Fingolimodfosfat har en 17% lägre fördelning i röda blodkroppar. Plasmaproteinbindning av fingolimod och fingolimodfosfat är hög (> 99%).
Fingolimod distribueras i stor utsträckning i vävnader med en distributionsvolym på cirka 1200 ± 260 liter.
Biotransformation
Hos människor metaboliseras fingolimod genom reversibel stereoselektiv fosforylering med bildning av den farmakologiskt aktiva (S) -enantiomeren av fingolimodfosfat. Fingolimod elimineras genom oxidativ biotransformation, huvudsakligen katalyserad av CYP4F2 och eventuellt andra isoenzymer, och efterföljande nedbrytning till inaktiva metaboliter, liknande fettsyrornas. Bildning av farmakologiskt inaktiva icke-polära ceramidanaloger av fingolimod observerades också. Det huvudsakliga enzymet som är involverat i metabolismen av fingolimod identifieras delvis och kan vara CYP4F2 eller CYP3A4.
Efter en enda oral administrering av fingolimod [14C] är huvudkomponenterna relaterade till fingolimod, detekterade i blodet genom deras bidrag till AUC upp till 34 dagar efter administrering av de totala radiomärkta komponenterna, själva fingolimod (23%), fingolimodfosfat ( 10%) och några inaktiva metaboliter (M3 -karboxylsyra -metabolit (8%), M29 -ceramidmetabolit (9%) och M30 -ceramidmetabolit (7%)).
Eliminering
Blodclearance för fingolimod är 6,3 ± 2,3 L / h och den genomsnittliga terminala eliminationshalveringstiden (t1 / 2) är 6-9 dagar. Blodnivåerna av fingolimod och fingolimodfosfat minskar parallellt i terminalfasen, vilket resulterar i liknande hälft -lever för båda molekylerna.
Efter oral administrering utsöndras cirka 81 % av dosen långsamt i urinen som inaktiva metaboliter. Fingolimod och fingolimodfosfat utsöndras inte oförändrat i urinen utan finns som huvudkomponenter i avföringen, varvid mängderna representerar mindre än 2,5 % av dosen Efter 34 dagar är återhämtningen av den administrerade dosen 89%.
Linjäritet
Koncentrationerna av fingolimod och fingolimodfosfat ökar på ett till synes dosproportionellt sätt efter upprepad administrering av enstaka dagliga doser på 0,5 mg eller 1,25 mg.
Egenskaper hos specifika populationer
Farmakokinetiken för fingolimod och fingolimodfosfat skiljer sig inte mellan män och kvinnor, hos patienter med olika etniskt ursprung eller hos patienter med lätt till allvarligt nedsatt njurfunktion.
Hos patienter med lätt, måttligt eller allvarligt nedsatt leverfunktion (Child-Pugh klass A, B och C) observerades ingen förändring av fingolimod Cmax, medan fingolimods AUC ökade med 12%, 44%och 103%. Hos patienter med allvarligt nedsatt leverfunktion ( Child-Pugh klass C), fingolimodfosfat Cmax minskade med 22% och AUC ändrades inte väsentligt. Farmakokinetiken för fingolimodfosfat har inte utvärderats hos patienter med lätt till måttligt nedsatt leverfunktion. Den uppenbara eliminationshalveringstiden för fingolimod var oförändrad hos personer med lätt nedsatt leverfunktion, medan den ökade med cirka 50% hos patienter med måttligt eller allvarligt nedsatt leverfunktion.
Fingolimod får inte användas till patienter med allvarligt nedsatt leverfunktion (Child-Pugh klass C) (se avsnitt 4.3). Fingolimodbehandling bör inledas med försiktighet hos patienter med lätt till måttligt nedsatt leverfunktion (se avsnitt 4.2).
Klinisk erfarenhet och farmakokinetiska data från patienter över 65 år är begränsade.Gilenya ska användas med försiktighet hos patienter över 65 år (se avsnitt 4.2).
Pediatrisk population
Data från en njurtransplantationsstudie inklusive 7 barn över 11 år är begränsade (studie FTY720A0115). Jämförelse av dessa uppgifter med friska vuxna volontärer är av liten relevans och inga meningsfulla slutsatser kan dras avseende de farmakokinetiska egenskaperna hos fingolimod hos barn.
05.3 Prekliniska säkerhetsdata
Den prekliniska säkerhetsprofilen för fingolimod utvärderades hos möss, råttor, hundar och apor.De viktigaste målorganen var lymfoidsystemet (lymfopeni och lymfoid atrofi), lungorna (viktökning, glatt muskelhypertrofi vid bronkioloalveolär korsning) och i olika arter hjärtat (negativ kronotrop effekt, förhöjt blodtrycksblod, perivaskulära förändringar och hjärtinfarkt degeneration); i en 2-årig studie var fingolimod endast aktivt på blodkärl (vaskulopati) hos råttor vid doser på 0,15 mg / kg och högre, motsvarande cirka 4 gånger den mänskliga systemiska exponeringen (AUC) vid en daglig dos av 0., 5 mg.
Inga tecken på cancerframkallande effekter observerades i en 2-årig studie på råttor med orala doser fingolimod upp till den högsta tolererade dosen 2,5 mg / kg, vilket motsvarar en marginal på cirka 50 gånger den humana systemiska exponeringen (AUC) vid en dos av 0,5 mg. I en 2-årig studie på möss observerades dock en högre förekomst av malignt lymfom vid doser på 0,25 mg / kg och högre, motsvarande cirka 6 gånger den mänskliga exponeringen. Systemisk (AUC) vid en daglig dos av 0,5 mg.
I djurstudier befanns fingolimod inte vara mutagent eller klastogent.
Fingolimod hade ingen effekt på spermier / rörlighet eller fertilitet hos han- och honråttor upp till den maximala testade dosen (10 mg / kg), vilket motsvarar en marginal på cirka 150 gånger den humana systemiska exponeringen (AUC) vid en daglig dos av 0,5 mg.
Fingolimod visade sig vara teratogent hos råttor vid administrering i doser av 0,1 mg / kg eller högre. De vanligaste fosterviscerala missbildningarna inkluderar ihållande artärstam och ventrikelseptaldefekt. Den teratogena potentialen hos kaniner kan inte bedömas fullständigt, men ökad embryofostal dödlighet observerades vid doser på 1,5 mg / kg och högre och minskade livskraftiga foster samt fostertillväxthämning vid doser av 5 mg / kg. Kg.
Hos råttor minskade överlevnaden för F1 -generationen av valpar i tidig postpartumperiod vid doser som inte orsakade maternell toxicitet. F1 -generationen påverkades dock inte av fingolimodbehandling med avseende på kroppsvikt, utveckling, beteende och fertilitet.
Fingolimod utsöndrades i mjölk från behandlade lakterande djur Fingolimod och dess metaboliter passerade placentabarriären hos dräktiga kaniner.
Miljöriskbedömning (Miljöriskbedömning, VAR)
Ingen miljörisk förväntas från användning av Gilenya av patienter med återfallande multipel skleros.
06.0 LÄKEMEDELSINFORMATION
06.1 Hjälpämnen
Kapselinnehåll:
Magnesiumstearat
Mannitol
Kapselskal:
Gul järnoxid (E172)
Titandioxid (E171)
Gelé
Bläck:
Lack (E904)
Torkad alkohol
Isopropylalkohol
Butylalkohol
Propylenglykol
Renat vatten
Koncentrerad ammoniaklösning
Kaliumhydroxid
Svart järnoxid (E172)
Gul järnoxid (E172)
Titandioxid (E171)
Dimetikon
06.2 Oförenlighet
Inte relevant.
06.3 Giltighetstid
2 år.
06.4 Särskilda förvaringsanvisningar
Förvaras vid högst 25 ° C.
Förvara i originalförpackningen för att skydda läkemedlet från fukt.
06.5 Förpackningens innehåll och förpackningens innehåll
Förpackningar innehållande 7, 28 eller 98 hårda kapslar eller multipelförpackningar innehållande 84 (3 förpackningar med 28) i PVC / PVDC / aluminiumblister.
Förpackningar innehållande 7 x 1 hårda kapslar i perforerade endosblister i PVC / PVDC / aluminium.
Alla förpackningsstorlekar kanske inte marknadsförs.
06.6 Anvisningar för användning och hantering
Inga speciella instruktioner.
07.0 INNEHAVARE AV GODKÄNNANDE FÖR FÖRSÄLJNING
Novartis Europharm Limited
Wimblehurst Road
Horsham
West Sussex, RH12 5AB
Storbritannien
08.0 NUMMER FÖR FÖRSÄLJNINGSTILLSTÅND
EU / 1/11/677 / 001-006
040949012
040949024
040949036
040949048
040949051
09.0 DATUM FÖR FÖRSTA GODKÄNNANDE ELLER FÖRNYELSE AV GODKÄNNANDET
17.03.2011
10.0 DATUM FÖR ÖVERSYN AV TEXTEN
Juni 2014