Allmänt och definition
Epigenetik behandlar studier av alla de ärftliga modifieringar som leder till variationer i genuttryck utan att förändra DNA -sekvensen, och därför utan att orsaka ändringar i sekvensen för de nukleotider som utgör den.

Med hjälp av ett mer tekniskt språk kan vi dock bekräfta att epigenetik studerar alla dessa modifieringar och alla de förändringar som kan variera fenotypen hos en individ, utan att dock ändra genotypen.
Fördelen med att "ha myntat termen" epigenetik "tillskrivs biologen Conrad Hal Waddington som 1942 definierade det som" den gren av biologin som studerar kausala interaktioner mellan gener och deras produkt och ger upphov till fenotypen ".
Förklarat i dessa termer kan epigenetik verka ganska komplex; för att bättre förstå konceptet kan det vara användbart att öppna en liten parentes om hur DNA skapas och hur transkriptionen av generna det innehåller sker.
DNA och gentranskription
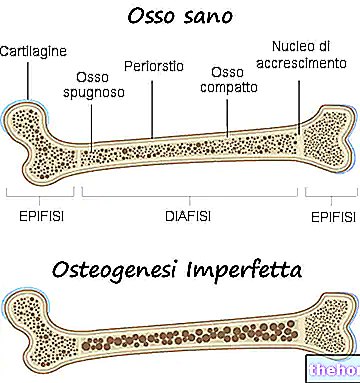
DNA finns i cellkärnan. Det har en dubbel spiralstruktur och består av repetitiva enheter, kallade nukleotider.
Det mesta av DNA: t som finns i våra celler är organiserat i särskilt underenheter som kallas nukleosomer.
Nukleosomer består av en central del (kallad kärna) som består av proteiner som kallas histoner runt vilka DNA lindas.
Uppsättningen av DNA och histoner utgör det så kallade kromatinet.
Transkriptionen av generna i DNA: n beror just på "förpackningen av det senare" inuti nukleosomerna. Faktum är att gentranskriptionsprocessen regleras av transkriptionsfaktorer, speciella proteiner som binder till specifika regulatoriska sekvenser som finns på DNA: t och som kan aktivera eller undertrycka - beroende på fallspecifika gener.
DNA med låg packningsnivå kommer därför att tillåta transkriptionsfaktorer att få åtkomst till regulatoriska sekvenser. Omvänt kommer DNA med hög packningsnivå inte att tillåta dem att komma åt.
Förpackningsnivån bestäms av histonerna själva och de förändringar som kan göras i deras kemiska struktur.
Mer specifikt orsakar "acetylering av histoner (dvs tillsats av en acetylgrupp vid särskilda ställen på aminosyrorna som utgör dessa proteiner) att kromatinet antar en" mer avslappnad "konformation som möjliggör inträde av transkriptionsfaktorer, därav gentranskription Å andra sidan avlägsnar deacetylering acetylgrupper, vilket får kromatinet att tjockna och därmed blockera gentranskription.

Epigenetiska signaler
Mot bakgrund av vad som har sagts hittills kan vi bekräfta att om epigenetik studerar de modifieringar som kan ändra fenotypen, men inte genotypen för en individ, är en epigenetisk signal den modifieringen som kan förändra uttrycket av en given gen , utan att ändra nukleotidsekvensen.
Följaktligen kan vi bekräfta att acetyleringen av histoner som nämns i föregående stycke kan betraktas som en epigenetisk signal; med andra ord är det en epigenetisk modifiering som kan påverka genens aktivitet (som kan transkriberas eller mindre) utan att förändras dess struktur.
En annan typ av epigenetisk modifiering utgörs av metyleringsreaktionen, både av DNA: n och av histonerna själva.
Till exempel minskar metyleringen (dvs tillsatsen av en metylgrupp) av DNA vid ett promotorställe transkriptionen av genen, vars aktivering regleras av promotorstället självt. Faktum är att promotorstället är en specifik sekvens av DNA lokaliserat uppströms generna, vars uppgift är att tillåta transkription av densamma att börja. Tillsatsen av en metylgrupp på denna plats orsakar därför en slags hämning som hindrar gentranskription.
Fortfarande är andra exempel på för närvarande kända epigenetiska modifikationer fosforylering och ubiquitination.
Alla dessa processer som involverar DNA och histonproteiner (men inte bara) regleras av andra proteiner som syntetiseras efter transkription av andra gener, vars aktivitet i sin tur kan ändras.
Den mest intressanta egenskapen hos en epigenetisk modifiering är i alla fall att den kan ske som svar på yttre miljöstimuli som just berör miljön som omger oss, vår livsstil (inklusive näring) och vårt hälsotillstånd.
På ett sätt kan en epigenetisk modifiering förstås som en adaptiv förändring som drivs av cellerna.
Dessa förändringar kan vara fysiologiska, som det händer när det gäller neuroner som antar epigenetiska mekanismer för inlärning och minne, men de kan också vara patologiska, till exempel vid psykiska störningar eller tumörer.
Andra viktiga kännetecken för epigenetiska modifieringar är reversibilitet och ärftlighet. Faktum är att dessa modifieringar kan överföras från en cell till en annan, även om de fortfarande kan genomgå ytterligare förändringar över tiden, alltid som svar på yttre stimuli.
Slutligen kan epigenetiska modifieringar inträffa i olika livsfaser och inte bara på embryonal nivå (när cellerna differentieras) som man en gång trodde, utan också när organismen redan är utvecklad.
Terapeutiska aspekter
Upptäckten av epigenetik och epigenetiska modifieringar kan i stor utsträckning utnyttjas inom det terapeutiska området för potentiell behandling av olika typer av patologier, inklusive de av neoplastisk typ (tumörer).
Faktum är att, som nämnts, de epigenetiska modifieringarna också kan vara av patologisk karaktär; därför kan de i dessa fall definieras som verkliga avvikelser.
Forskarna antog därför att om dessa förändringar kan påverkas av yttre stimuli och kan manifestera sig och ytterligare modifiera sig under hela organismens liv, är det möjligt att intervenera på dem med hjälp av specifika molekyler i syfte att återföra situationen till normala förhållanden. av normalitet. Detta är något som inte kan göras (åtminstone inte ännu) när orsaken till sjukdomen ligger i en verklig genetisk mutation.
För att bättre förstå detta koncept kan vi ta som ett exempel den användning som forskare har gjort av kunskapen om epigenetik inom området cancerbehandlingar.


-cos-cause-e-terapia.jpg)