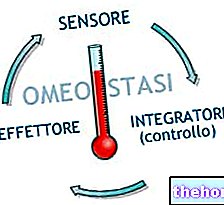
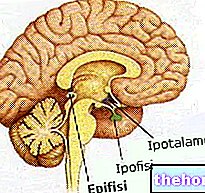
Struktur och funktioner
Hemoglobin är ett metalloprotein som finns i röda blodkroppar, som ansvarar för att transportera syre i blodet. Faktum är att syre bara är måttligt lösligt i vatten; därför är de kvantiteter som är upplösta i blodet (mindre än 2% av totalen) inte tillräckliga för att tillgodose vävnadens metaboliska krav. Behovet av en specifik bärare är därför uppenbart.
I blodomloppet kan syre inte binda direkt och reversibelt till proteiner, vilket i stället förekommer för metaller som koppar och järn. Inte överraskande finner vi i mitten av varje proteinunderenhet av hemoglobin, insvept i ett proteinskal, den så kallade protesen grupp EME, med ett metalliskt hjärta representerat av en järnatom i Fe2 + oxidationstillståndet (reducerat tillstånd), som binder syre på ett reversibelt sätt.
Blodanalys
- Normala hemoglobinvärden i blodet: 13-17 g / 100 ml
Hos kvinnor är värdena i genomsnitt 5-10% lägre än hos män.
Möjliga orsaker till högt hemoglobin
- Polycytemier
- Förlängd vistelse på hög mark
- Kroniska lungsjukdomar
- Hjärtsjukdom
- Bloddopning (användning av erytropoietin och derivat eller substanser som efterliknar deras verkan)
Möjliga orsaker till lågt hemoglobin
- Anemier
- Järnbrist (järnbrist)
- Riklig blödning
- Carcinom
- Graviditet
- Thalassemias
- Brännskador
Syrehalten i blodet ges därför genom summering av den lilla mängd som är upplöst i plasma med fraktionen bunden till hemoglobinjärn.
Mer än 98% av syret som finns i blodet är bundet till hemoglobin, vilket i sin tur cirkulerar i blodomloppet som är tilldelat inom de röda blodkropparna. Utan hemoglobin kunde erytrocyterna därför inte utföra sin uppgift som syretransportörer i blodet.
Med tanke på denna metalls centrala roll kräver syntesen av hemoglobin ett tillräckligt intag av järn i kosten. Cirka 70% av det järn som finns i kroppen finns faktiskt i hemgruppens hemgrupper.
Hemoglobin består av 4 subenheter som strukturellt liknar myoglobin *.
* Medan hemoglobin transporterar syre från lungorna till vävnaderna, transporterar myoglobin det syre som frigörs av hemoglobin till de olika cellulära organellerna som använder det (t.ex. mitokondrier).

Hemoglobin är ett stort och komplext metalloprotein, som kännetecknas av fyra globulära proteinkedjor respektive lindade runt en hemgrupp som innehåller Fe2 +.
För varje hemoglobinmolekyl hittar vi därför fyra hemgrupper inslagna i den relativa globulära proteinkedjan. Eftersom det finns fyra järnatomer i varje hemoglobinmolekyl kan varje hemoglobinmolekyl binda fyra syreatomer till sig själv, enligt den reversibla reaktionen:
Hb + 4O2 ← → Hb (O2) 4
Som de flesta känner till är hemoglobins uppgift att ta syre i lungorna, släppa ut det till cellerna som behöver det, ta koldioxid från dem och släppa ut det i lungorna där chilon börjar igen.
Under blodets passage i kapillärerna i lungalveolerna binder hemoglobin syre till sig själv, vilket sedan frigörs till vävnaderna i den perifera cirkulationen. Detta utbyte sker eftersom syrebindningarna med järnet i EME -gruppen är labila och känsliga för många faktorer, varav den viktigaste är syrgasens spänning eller partiella tryck.
Bindning av syre till hemoglobin och Bohr -effekten
I lungorna ökar plasmasyrusspänningen på grund av diffusion av gas från alveolerna till blodet (↑ PO2); denna ökning får hemoglobin att binda ivrig till syre; det motsatta inträffar i de perifera vävnaderna, där koncentrationen av upplöst syre i blodet minskar (↓ PO2) och det partiella trycket av koldioxid ökar (↑ CO2); detta får hemoglobin att släppa ut syre och laddas med CO2. Förenkla konceptet så mycket som möjligt, ju mer koldioxid som finns i blodet, desto mindre syre förblir bunden till hemoglobin.
Även om mängden syre fysiskt löst i blodet är mycket låg, spelar det därför en grundläggande roll. Faktum är att denna kvantitet påverkar kraftigt bindningsstyrkan mellan syre och hemoglobin (liksom representerar ett "viktigt referensvärde för att reglera lungventilation).
Genom att sammanfatta allt med en graf växer mängden syre kopplat till hemoglobin i förhållande till pO2 efter en sigmoidkurva:

Det faktum att platuområdet är så stort placerar en viktig säkerhetsmarginal vid den maximala mättnaden av hemoglobin under passagen till lungorna. Även om pO2 vid alveolär nivå normalt är lika med 100 mm Hg, observerar vi den siffra som vi faktiskt noterar hur även ett partiellt syretryck lika med 70 mmHg (typiskt förekomst av vissa sjukdomar eller vistelse på höga höjder), andelarna av mättat hemoglobin förblir nära 100%.
I området med maximal lutning, när syrespänningen sjunker under 40 mmHg, sjunker hemoglobins förmåga att binda syre plötsligt.
Vid vilande förhållanden är PO2 i intracellulära vätskor cirka 40 mmHg; på denna plats, på grund av gaslagarna, diffunderar syret som är upplöst i plasma mot de sämre vävnaderna i O2 och passerar kapillärmembranet. Följaktligen sjunker plasmaspänningen av O2 ytterligare och detta gynnar frisättningen av syre från hemoglobinet. . Vid intensiv fysisk ansträngning sjunker å andra sidan syrespänningen i vävnaderna till 15 mmHg eller mindre, vilket resulterar i att blodet är kraftigt utarmat av syre.
För vad som har sagts lämnar en viktig mängd syresatt hemoglobin i viloläge vävnaderna och förblir tillgängliga vid behov (till exempel för att hantera en plötslig ökning av ämnesomsättningen i vissa celler).
Den heldragna linjen som visas på bilden ovan kallas hemoglobindissociationskurvan; det bestäms vanligtvis in vitro vid pH 7,4 och vid en temperatur av 37 ° C.
Bohr -effekten har konsekvenser både för intaget av O2 på lungnivå och för dess frisättning på vävnadsnivå.
Där det finns mer upplöst koldioxid i form av bikarbonat, frigör hemoglobin lättare syre och laddas med koldioxid (i form av bikarbonat).

Samma effekt uppnås genom försurning av blodet: ju mer blodets pH sjunker och desto mindre syre förblir bunden till hemoglobinet; inte överraskande löses koldioxid i blodet huvudsakligen i form av kolsyra, som dissocierar.



För att upptäcka dess upptäckare är effekten av pH eller koldioxid på syredissociation känd som Bohr -effekten.
Som förväntat frigör hemoglobin i en sur miljö lättare syre, medan bindningen till syre i en grundläggande miljö är starkare.

Andra faktorer som kan ändra hemoglobins affinitet för syre inkluderar temperatur. I synnerhet minskar hemoglobins affinitet för syre med ökande kroppstemperatur. Detta är särskilt fördelaktigt under vinter- och vårmånaderna, eftersom lungblodets temperatur (i kontakt med luften i den yttre miljön) är lägre än den som nås i vävnaderna, där frigöring av syre därför underlättas.

2.3 difosfoglycerat är en mellanprodukt i glykolys som påverkar hemoglobins affinitet för syre. Om dess koncentrationer i de röda blodkropparna ökar, minskar hemoglobins affinitet för syre, vilket underlättar frisättningen av syre till vävnaderna. Inte överraskande, erytrocytkoncentrationerna av 2,3 difosfoglycerat ökar till exempel i anemi, hjärt-lunginsufficiens och under vistelsen på hög höjd.
I allmänhet är effekten av 2,3 bisfosfoglycerat relativt långsam, särskilt jämfört med det snabba svaret på förändringar i pH, temperatur och partiellt tryck av koldioxid.

Bohr -effekten är mycket viktig under intensivt muskelarbete; i sådana förhållanden, i de vävnader som är mest utsatta för stress, finns det en lokal ökning av temperaturen och trycket av koldioxid, därför i blodets surhet. Som förklarats ovan gynnar allt detta frisättning av syre till vävnaderna, vilket förskjuter hemoglobindissociationskurvan till höger.