Aktiva ingredienser: Midodrina
GUTRON 2,5 mg tabletter
GUTRON 2,5 mg / ml orala droppar, lösning
GUTRON 5 mg / 2 ml injektionsvätska, lösning
Indikationer Varför används Gutron? Vad är det för?
FARMAKOTERAPEUTISK KATEGORI
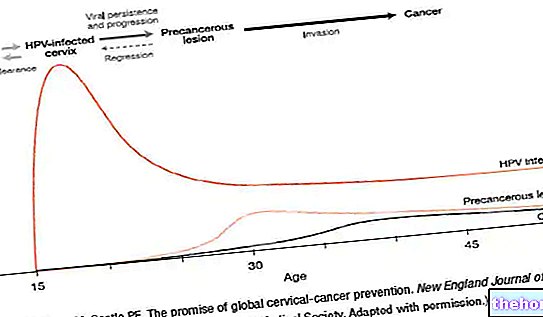
Gutron är ett preparat med antihypotensiv aktivitet som innehåller den aktiva ingrediensen midodrinhydroklorid som, genom att öka aktiviteten i det sympatiska autonoma nervsystemet (α-sympatomimetisk verkan), orsakar venös och arteriolär sammandragning på perifer nivå med en följdhöjning av blodtrycket . arteriell.
TERAPEUTISKA INDIKATIONER
Ortostatisk dysreglering (sympatisk, asympatisk) vid diagnosen:
- hypotensivt-asteniskt syndrom; väsentlig hypotoni; ortostatisk hypotension; postoperativa, postinfektiösa, postpartum hypotensiva tillstånd; hypotoni på klimatbasis;
- hypotoni efter behandling med psykofarmaka.
Kontraindikationer När Gutron inte ska användas
Arteriell hypertoni, hjärtsjukdom, feokromocytom, kärlsjukdomar av utplånande eller spastisk art, svår kranskärlssjukdom, avancerad vaskulär skleros, sluten vinkelglaukom, prostatahypertrofi med urinretention, mekaniska hinder för urinutflöde, tyrotoxikos. Individuellt konstaterat överkänslighet mot produkten.
Försiktighetsåtgärder vid användning Vad du behöver veta innan du tar Gutron
Använd endast under graviditet vid absolut och säkerställd nödvändighet och under direkt medicinsk övervakning. Hos diabetespatienter är det lämpligt att utföra en mer frekvent bestämning av glykemiska värden. Under långvariga behandlingar rekommenderas periodisk övervakning av njurfunktionen.
Interaktioner Vilka läkemedel eller livsmedel kan ändra effekten av Gutron
Vasopressoreffekten av Gutron kan förstärkas med mono-amino-oxidashämmare (MAO-hämmare), vars samtidig administrering därför bör undvikas.
Varningar Det är viktigt att veta att:
För dem som bedriver sport: användning av läkemedlet utan terapeutisk nödvändighet utgör dopning och kan i alla fall avgöra positiva antidopningstester.
För dem som bedriver sport kan användningen av läkemedel som innehåller etylalkohol bestämma positiva antidopningstester, i förhållande till de alkoholkoncentrationsgränser som vissa sportförbund anger.
EFFEKTER PÅ MÖJLIGHETEN ATT KÖRA OCH PÅ ANVÄNDNING AV MASKINER
Inget särskilt att rapportera.
Dosering och användningssätt Hur man använder Gutron: Dosering
Dosen av Gutron måste fastställas individuellt i förhållande till patientens olika respons. Det är lämpligt att påbörja behandling med doser som är proportionella mot symtomens enhet och därefter ändra dem enligt det terapeutiska svaret.
I milda och medelstora former är den vägledande dosen 10-20 droppar eller 1/2 - 1 tablett upp till 3 gånger om dagen. Dropparna kan tas utspädda i vatten eller på en sockerbit.
I de allvarligaste hypotensiva tillstånden och i hypotoni efter behandling med psykofarmaka: 2,5 - 5 mg (1-2 tabletter eller 1 ampull) upp till 3 gånger om dagen. Ampullerna kan administreras intramuskulärt, långsamt intravenöst, eventuellt utspädd i vanliga infusionslösningar.
Överdosering Vad du ska göra om du har tagit för mycket Gutron
Den möjliga förekomsten av reflexbradykardi (överdriven saktning av hjärtslaget), en överdriven ökning av blodtrycket och andra symptom på överdosering (se biverkningar) kan snabbt kontrolleras av läkaren genom att administrera atropin vid vanliga terapeutiska doser och / eller α- blockera droger.
Biverkningar Vilka är biverkningarna av Gutron
Yrsel eller yrsel och stickande huvud och bål kan förekomma hos vissa patienter. Den möjliga uppkomsten av dessa fenomen, med oral administrering, inträffar efter cirka 1-2 timmar efter intaget och kan bestå i cirka 3-5 timmar.
Överdrivna doser av Gutron kan orsaka pilomotoriska reaktioner (gåshud), särskilt i hårbotten, känsla av kyla, ökad urinlängtan, huvudvärk, hjärtklappning och ibland reflexbradykardier. Broschyr.
Giltighetstid och lagring
För utgångsdatum, se det som visas på förpackningen. Varning: använd inte läkemedlet efter utgångsdatumet som anges på förpackningen. Förvara läkemedlet på en torr plats.
Sammansättning och läkemedelsform
SAMMANSÄTTNING
2,5 mg tabletter
Varje 0,130 g tablett innehåller:
Aktiv ingrediens: 2,5 mg Midodrinhydroklorid
Hjälpämnen: Stärkelse, mikrokristallin cellulosa, kiseldioxid, talk, magnesiumstearat.
2,5 mg / ml orala droppar, lösning
Varje 100 ml lösning innehåller:
Aktiv ingrediens: Midodrinhydroklorid g 0,25
Hjälpämnen: 95% etylalkohol, renat vatten.
5 mg / 2 ml injektionsvätska, lösning
Varje injektionsflaska på 2 ml innehåller:
Aktiv ingrediens: Midodrinhydroklorid 5 mg
Hjälpämnen: Natriumklorid, propylenglykol, vatten för injektionsvätskor.
LÄKEMEDELSFORM OCH INNEHÅLL
30 delbara tabletter med 0,130 g flaska med 30 ml 6 ampuller om 2 ml
Bipacksedel: AIFA (Italian Medicines Agency). Innehåll publicerat i januari 2016. Den information som finns finns kanske inte uppdaterad.
För att få tillgång till den senaste versionen är det lämpligt att gå till AIFA (Italian Medicines Agency) webbplats. Ansvarsfriskrivning och användbar information.
01.0 LÄKEMEDLETS NAMN
GUTRON
02.0 KVALITATIV OCH KVANTITATIV SAMMANSÄTTNING
2,5 mg / ml orala droppar, lösning
Varje 100 ml lösning innehåller:
Midodrinhydroklorid g 0,25
2,5 mg tabletter
Varje 0,130 g tablett innehåller:
Midodrinhydroklorid 2,5 mg
5 mg / 2 ml injektionsvätska, lösning
Varje 2 ml injektionsflaska innehåller:
Midodrinhydroklorid 5 mg
03.0 LÄKEMEDELSFORM
Orala droppar, lösning
Delbara tabletter
Injektionsflaskor
04.0 KLINISK INFORMATION
04.1 Terapeutiska indikationer
Ortostatisk dysreglering (sympatisk, asympatisk) vid diagnosen:
hypotensivt-asteniskt syndrom; väsentlig hypotoni; ortostatisk hypotension; postoperativa, postinfektiösa, postpartum hypotensiva tillstånd; hypotoni på klimatbasis;
hypotoni efter behandling med psykofarmaka.
04.2 Dosering och administreringssätt
Dosen av Gutron måste bestämmas individuellt i förhållande till det autonoma nervsystemets olika reaktivitet och patientens vasotoniska situation.
Det är lämpligt att påbörja behandling med doser som är proportionella mot symtomens enhet och därefter ändra dem enligt det terapeutiska svaret.
I milda och medelstora former är den vägledande dosen 10-20 droppar eller 1 / 2-1 tablett upp till tre gånger om dagen. Dropparna kan tas utspädda i vatten eller på en sockerbit.
I de allvarligaste hypotensiva tillstånden och i hypotoni efter behandling med psykofarmaka: 2,5-5 mg (1-2 tabletter eller 1 ampull) upp till tre gånger om dagen. Ampulformuleringen kan administreras intramuskulärt, långsamt intravenöst, eventuellt utspädd i vanliga infusionslösningar.
04.3 Kontraindikationer
Arteriell hypertoni, feokromocytom, utplånande och spastiska vaskulopatier, svår kranskärlssjukdom, avancerad vaskulär skleros, sluten vinkelglaukom, prostatahypertrofi med urinretention, mekaniska hinder för urinutflöde, tyrotoxikos. Individuellt konstaterat överkänslighet mot produkten.
04.4 Särskilda varningar och lämpliga försiktighetsåtgärder vid användning
Den möjliga förekomsten av reflexbradykardi och andra symtom på överdosering, såsom en överdriven ökning av blodtrycket, kan snabbt kontrolleras genom administrering av atropin vid vanliga terapeutiska doser och / eller blockerande läkemedel.
Produkten, även om den inte stimuleras av b-receptorerna, kan indirekt påverka hjärtfunktionen på grund av den större ansträngningen på grund av ökad venös återgång och perifert motstånd.
Under långvariga behandlingar rekommenderas periodisk övervakning av njurfunktionen.
Hos diabetespatienter är det lämpligt att utföra en mer frekvent bestämning av glykemiska värden.
Förvara utom räckhåll för barn.
04.5 Interaktioner med andra läkemedel och andra former av interaktion
Produktens vasopressoreffekt kan förstärkas med I.M.A.O. -läkemedel, vars samtidig administrering därför måste undvikas.
04.6 Graviditet och amning
Produkten kan endast användas under graviditet under absoluta förhållanden och fastställd nödvändighet.
04.7 Effekter på förmågan att framföra fordon och använda maskiner
Inget särskilt att rapportera.
04.8 Biverkningar
Vissa patienter kan uppleva yrsel eller yrsel och stickningar i huvudet och bålen. Den möjliga uppkomsten av dessa fenomen, med oral administrering, inträffar efter cirka 1 eller 2 timmar efter intag och kan kvarstå i cirka 3-5 timmar. Överdrivna doser av Gutron kan orsaka pilomotoriska reaktioner (gåshud), särskilt i hårbotten, känsla av förkylning, ökad urinlängtan, huvudvärk, hjärtklappning och ibland reflexbradykardi.
04.9 Överdosering
Se punkterna 4.4 och 4.8.
05.0 FARMAKOLOGISKA EGENSKAPER
05.1 Farmakodynamiska egenskaper
Midodrin, strukturellt sammansatt av sammanslutningen av två väldefinierade molekylära enheter (en katekolamin, 1- (2,5-dimetoxifenyl) -2-aminoetanol och en aminosyra, glycin), kännetecknas särskilt av egenskapen att inducera en perifer nivå en ökning av venös och arteriolär ton som resulterar i en progressiv ökning av venös återkomst till hjärtat och en därmed ökad blodtrycksvärden.
Den speciella farmakodynamiska egenskapen för midodrin består i att den utövar en direkt och selektiv stimulerande verkan på perifera a-adrenerga receptorer, vilket utesluter eventuell interferens på b-adrenerga receptorer, vars stimulering skulle orsaka hjärt-, bronkial- och metaboliska effekter.
05.2 Farmakokinetiska egenskaper
Midodrinmolekylen är inte aktiv av sig själv, utan bara efter metabolisk transformation. Farmakokinetiska undersökningar, utförda med tritiummärkt midodrin (3H-midodrin), krediterar midodrin som en "transportform" av dess farmakologiskt aktiva metabolit, 1- (2,5-dimetoxifenyl) -2-aminoetanol, som det frisätts i organismen genom enzymatisk uppdelning av glycinresten. Detta förhindrar snabb metabolisering av preparatet i den enterohepatiska cirkulationen och garanterar en hög biotillgänglighet även för oral administrering.
Efter cirka 25 minuter absorberas 3H-midodrin helt.
Den farmakologiskt aktiva metaboliten släpps ut i cirkulationen genom enzymatisk klyvning och når den högsta plasmanivån efter cirka en timme.
Den långsamma och gradvisa frigivningen av den aktiva principen bestämmer en progressiv och långvarig effekt upp till ungefär den tolfte timmen.
Eliminering av 3H-midodrin och dess metaboliter sker nästan uteslutande via urinen.
Den viktigaste eliminationsprodukten efter intravenös administrering är dess farmakologiskt aktiva metabolit.
Under de 8 timmarna efter injektionen är denna eliminering 54% och når 90% efter cirka 24 timmar.
05.3 Prekliniska säkerhetsdata
Från toxicitetsstudier som utförts på olika djurarter framgår det att midodrin har dålig akut toxicitet och god tolerabilitet efter medellång och lång sikt administrering.
Det påverkar inte heller fertilitet, dräktighet och foster- och neonatal utveckling; slutligen har den inte teratogena effekter.
06.0 LÄKEMEDELSINFORMATION
06.1 Hjälpämnen
2,5 mg / ml orala droppar, lösning
95% etylalkohol, renat vatten.
2,5 mg tabletter
Stärkelse, mikrokristallin cellulosa, kiseldioxid, talk, magnesiumstearat.
5 mg / 2 ml injektionsvätska, lösning
Natriumklorid, propylenglykol, vatten för injektionsvätskor.
06.2 Oförenlighet
Ingen.
06.3 Giltighetstid
36 månader
06.4 Särskilda förvaringsanvisningar
2,5 mg tabletter
Förvaras torrt
Att hållas borta från ljus
2,5 mg / ml orala droppar, lösning och 5 mg / 2 ml injektionsvätska, lösning
Att hållas borta från ljus
06.5 Förpackningens innehåll och förpackningens innehåll
2,5 mg tabletter
Blister termoformade av ogenomskinlig styv PVC-tejp, förseglade genom värmeförsegling med aluminiumtejp filmad med värmeförseglingsharts för PVC, förpackade i en litograferad kartong.
Låda med 30 delbara tabletter
2,5 mg / ml orala droppar, lösning
Amber glasflaska, klass III, innehållande 30 ml hydroalkoholisk lösning, med införlivad dropp och förseglad med ett skruvlock försett med en tätningspackning, förpackad i en litograferad kartong.
30 ml injektionsflaska med dropp
5 mg / 2 ml injektionsvätska, lösning
Färglösa injektionsflaskor i neutralt glas, typ I, som uppfyller de tester som krävs av F.U. VIII Ed., Vol. I, sid. 457 för behållare avsedda att lagra injicerbara lösningar, förpackade i en litograferad kartong.
Låda med 6 injektionsflaskor à 2 ml
06.6 Anvisningar för användning och hantering
Inte relevant.
07.0 INNEHAVARE AV GODKÄNNANDE FÖR FÖRSÄLJNING
LUSOFARMACO
Luso Farmaco Institute of Italy S.p.A.
Via W. Tobagi, 8 - Peschiera Borromeo (MI)
Under licens från Nycomed Austria GmbH
08.0 NUMMER FÖR FÖRSÄLJNINGSTILLSTÅND
2,5 mg tabletter: 024519011
2,5 mg / ml orala droppar, lösning: 024519023
5 mg / 2 ml injektionsvätska, lösning: 024519035
09.0 DATUM FÖR FÖRSTA GODKÄNNANDE ELLER FÖRNYELSE AV GODKÄNNANDET
7.12.1981 / 1.06.2005
10.0 DATUM FÖR ÖVERSYN AV TEXTEN
Februari 2010