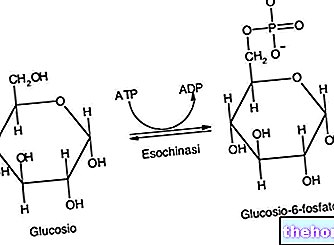
Aktiva ingredienser: Oxatomide
Tinset Adult 30 mg tabletter
Förpackningsinsatser finns i förpackningsstorlekar:- Tinset Adult 30 mg tabletter
- Tinset 25 mg / ml oral droppar suspension
- Tinset 5% gel
Varför används Tinset? Vad är det för?
FARMAKOTERAPEUTISK KATEGORI
Antihistamin för systemiskt bruk.
TERAPEUTISKA INDIKATIONER
Förebyggande och grundläggande behandling av allergiska sjukdomar, främst vid rinit, yttre astma, follikulär konjunktivit, kronisk urtikaria, atopisk dermatit, matallergi.Om det behövs kan TINSET kombineras med andra läkemedel som motsvarar dessa indikationer, förutsatt att deras verkningsmekanism skiljer sig från TINSETs TINSET är inte indicerat vid akut behandling av allergiska tillstånd såsom astmaanfall.
Kontraindikationer När Tinset inte ska användas
Överkänslighet mot den aktiva substansen, mot cinnarizin eller mot något hjälpämne, leversvikt.
Försiktighetsåtgärder vid användning Vad du behöver veta innan du tar Tinset
Konsumera inte alkoholhaltiga drycker och ta inte mediciner som innehåller alkohol medan du tar Tinset.
Oxatomid, liksom andra antihistaminer, kan störa hudallergitest och därför bör behandlingen avbrytas i minst 3 dagar före hudtestet.
Interaktioner Vilka läkemedel eller livsmedel kan ändra effekten av Tinset
Tala om för din läkare eller apotekspersonal om du nyligen har tagit andra läkemedel, även receptfria sådana.
Baserat på oxatomidmetabolismstudier kan det finnas en potentiell interaktion mellan Oxatomide och CYP450 -hämmare, såsom itrakonazol, ketokonazol och cimetidin. Tinset kan öka den lugnande effekten av CNS -depressiva medel, inklusive alkohol, barbiturater, hypnotika., Narkotiska analgetika, lugnande medel, ångestdämpande och antipsykotika. Biverkningar av antikolinerga läkemedel kan ökas genom samtidig administrering av Tinset. Samtidig användning av MAO -hämmare och Tinset rekommenderas inte.
Varningar Det är viktigt att veta att:
TINSET är inte indicerat vid akut behandling av allergiska tillstånd såsom astmaattack. När Tinset förskrivs till patienter med astma ska den nuvarande läkemedelsbehandlingen inte stoppas plötsligt, utan gradvis minska dosen. Detta gäller särskilt för patienter som behandlas med kortikosteroider. Fall av hepatit, leverskada, gulsot och onormal leverfunktion (måttlig till stor ökning av leverenzymer) har rapporterats, inklusive mycket sällsynta fall av dödligt leversvikt.
Patienterna bör observeras noggrant med avseende på leverbiverkningar.Vid onormal leverfunktion bör lämpliga åtgärder såsom avbrott av behandlingen vidtas och behandlingen med Tinset ska inte återupptas.
På grund av dess eliminering av levern bör försiktighet iakttas vid förskrivning av oxatomid till patienter med kända leversjukdomar. Vid behov bör behandlingen av dessa patienter helst börja med halva normal dos. Intervallet mellan administrationer kan bibehållas oförändrat.
Dyskinesi och extrapyramidala symptom har observerats hos både vuxna och barn. Extrapyramidala symtom var vanligare hos barn.
I den geriatriska populationen kan åldersrelaterade fysiologiska förändringar (såsom ökad permeabilitet av blod-hjärnbarriären och minskad levermetabolism) påverka aktiviteten hos H1-receptorantagonister. Hos äldre måste också en ökad risk för sedering beaktas .
Graviditet, amning och fertilitet
Fråga din läkare eller apotekspersonal om råd innan du tar något läkemedel.
Säkerheten för Tinset hos gravida kvinnor har inte fastställts. Om det är nödvändigt att administrera Tinset under graviditeten ska de potentiella riskerna noggrant vägas mot de förväntade terapeutiska fördelarna.
Det finns otillräcklig information om utsöndring av oxatomid i bröstmjölk, därför bör amning avbrytas vid behandling med Tinset.
Effekter på förmågan att framföra fordon och använda maskiner
Det rekommenderas inte att köra bil eller använda maskiner medan du tar Tinset på grund av eventuell trötthet och minskad vakenhet. Ett samtidigt intag av alkohol kan förstärka dessa effekter.
Viktig information om några av ingredienserna
Läkemedlet innehåller laktos, kontakta din läkare vid intolerans mot socker innan du tar medicinen.
Dosering och användningssätt Så här använder du Tinset: Dosering
Vuxna
För varje indikation, 1 tablett två gånger om dagen; efter frukost och efter middagen.
Uppmärksamhet
För att undvika oavsiktlig överdos, följ strikt de rekommenderade doserna.
Överdosering Vad du ska göra om du har tagit för mycket Tinset
De vanligaste symptomen efter överdosering är: somnolens, stupor och extrapyramidala symtom som dyskinesi, stel nacke, ofrivilliga ögonrörelser, dystoni och hypertoni.
Mindre vanligt är hyperexcitabilitet och agitation. Mer sällan har mydriasis och generaliserade muskelspasmer och koma rapporterats. Efter överdosering har medvetslöshet och QT -förlängning rapporterats.
Det finns inga specifika motgift. Behandlingen består av noggrann övervakning av vitala tecken och stödjande åtgärder. Ett EKG bör utföras för att utvärdera QT -segmentet. Om det anses lämpligt kan aktivt kol ges. Extrapyramidala symptom har behandlats framgångsrikt med antikolinerga medel.
Vid oavsiktlig förtäring / intag av en för hög dos Tinset, meddela din läkare omedelbart eller gå till närmaste sjukhus.
Om du har några tvivel om att använda tinset, kontakta din läkare eller apotek
Biverkningar Vilka är biverkningarna av Tinset
Liksom alla läkemedel kan TINSET orsaka biverkningar men alla användare behöver inte få dem.
De biverkningar som har rapporterats vid användning av Tinset i både kliniska prövningar och under marknadsföringen anges nedan.
I vanliga fall har följande rapporterats: Viktökning, dåsighet, trötthet, ökad aptit.
Mycket vanliga (kan drabba fler än 1 av 10 personer): sömnighet
Vanliga (kan förekomma hos upp till 1 av 10 personer): ökad aptit, trötthet, huvudvärk, sedering, muntorrhet, viktökning,)
Mindre vanliga (kan förekomma hos upp till 1 av 100 personer): aptitstörningar, nervositet, rastlöshet, irritabilitet, sömnlöshet, uppmärksamhetsstörning, yrsel, andnöd, illamående, kräkningar, buksmärtor, övre buksmärta, dyspepsi, förstoppning, obehag i bröstet, urinretention, utslag, urtikaria
Mycket sällsynta (kan förekomma hos upp till 1 av 1000 personer): hemolytisk anemi, trombocytopeni, leukopeni, agranulocytos, anafylaktisk chock, anafylaktiska reaktioner, anafylaktoida reaktioner, överkänslighet, minskad aptit, hallucinationer, agitation, apati, förvirring, desorientering, mardrömmar, sömnstörningar aggression, kramper, minskad medvetenhet, medvetslöshet, stupor, slöhet, afasi, parestesi, extrapyramidala störningar, onormal koordination, dyskinesi, dysartri, dysgeusi, hypertoni, hypotoni, opisthotonus, tremor, myoklonus, ataxi, dystoni, dåsighet, okulogisk kris, dimsyn, dubbelseende, onormal utvidgning av pupillerna, blickförlamning, tinnitus, hörselnedsättning, torsade de pointes, ventrikelflimmer, ventrikulär arytmi, ventrikulär extrasystole, arytmi, takykardi, bradykardi, hjärtklappning, rodnad, hypotension, chock, näsblod, bronkial spasm, torra slemhinnor na salter, svalgödem, gastroesofageal reflux, diarré, leversvikt (dödlig), fulminant hepatit, kolestatisk hepatit, hepatit, akut hepatit, hepatocellulär skada, hepatotoxicitet, leverskada, kolestatisk gulsot, gulsot, kolestas, onormal leverfunktion, fettlever, lever störningar, toxisk epidermal nekrolys, Stevens-Johnsons syndrom, toxiska utslag, erytem multiforme, erytem, angioödem, klåda, erytematösa utslag, ljuskänslighetsreaktioner, läkemedelsutbrott, eksem, överdriven svettning, muskelstelhet, muskelsvaghet, myalgi, stel nacke, trismus, dysuri, hematuri, kromaturi, gynekomasti, galaktorré, gångstörning, sjukdomskänsla, hyperpyrexi, pyrexi, kall känsla, ödem, onormala känslor, förlängning av QT -kanalen i elektrokardiogrammet, abnormitet i det elektrokardiografiska spåret, abnormitet i leverfunktionstestet, lever enzymer ökade, alaninaminotransferas ökade, ökade Ökning av aspartataminotransferas, förhöjt gammaglutamyltransferas, förhöjt bilirubin i blodet, förhöjt alkaliskt fosfatas i blodet, ökat kreatininfosfokinas i blodet, förhöjt laktatdehydrogenas i blodet, minskat blodtryck, ökad puls
Pediatriska patienter
De biverkningar som anges i detta avsnitt "biverkningar" kan också förekomma hos den pediatriska populationen.
Efterlevnaden av instruktionerna i bipacksedeln minskar risken för biverkningar.
Rapportering av biverkningar
Tala med din läkare eller apotekspersonal om du får några biverkningar. Detta inkluderar eventuella biverkningar som inte nämns i denna bipacksedel. Du kan också rapportera biverkningar direkt via det nationella rapporteringssystemet på https://www.aifa.gov.it/content/segnalazioni-reazioni-avverse. Genom att rapportera biverkningar kan du hjälpa till att ge mer information om säkerheten för detta läkemedel.
Giltighetstid och lagring
Utgångsdatum: se utgångsdatumet som står tryckt på förpackningen
Utgångsdatumet avser produkten i intakt förpackning, korrekt förvarad.
Varning: använd inte läkemedlet efter utgångsdatumet som anges på förpackningen
Läkemedel ska inte kastas i avloppsvatten eller hushållsavfall. Fråga din apotekare hur du ska kasta läkemedel som du inte använder längre. Detta hjälper till att skydda miljön.
HÅLL LÄKEMEDLET UTOM BARNENS SIKT OCH RÄCKLIGA.
Sammansättning och läkemedelsform
SAMMANSÄTTNING
En tablett innehåller:
aktiv ingrediens: oxatomid 30 mg; Hjälpämnen: laktos, majsstärkelse, mikrokristallin cellulosa, povidon, utfälld kiseldioxid, magnesiumstearat.
LÄKEMEDELSFORM OCH INNEHÅLL
30 tabletter om 30 mg.
Bipacksedel: AIFA (Italian Medicines Agency). Innehåll publicerat i januari 2016. Den information som finns finns kanske inte uppdaterad.
För att få tillgång till den senaste versionen är det lämpligt att gå till AIFA (Italian Medicines Agency) webbplats. Ansvarsfriskrivning och användbar information.
01.0 LÄKEMEDLETS NAMN
TINSET
02.0 KVALITATIV OCH KVANTITATIV SAMMANSÄTTNING
TINSET vuxna 30 mg tabletter
En tablett innehåller: aktiv ingrediens Oxatomide 30 mg.
Hjälpämnen: laktos 120,09 mg
TINSET 25 mg / ml oral droppar suspension
100 ml suspension innehåller: aktiv ingrediens Oxatomidehydrat 2,6 g (motsvarar 2,5 g oxatomid).
Hjälpämnen: metyl-p-hydroxibensoat 180 mg, propyl-p-hydroxibensoat 20 mg.
För fullständig förteckning över hjälpämnen, se avsnitt 6.1.
03.0 LÄKEMEDELSFORM
Tabletter:
vit, rund, platt graverad med "30" på ena sidan och poänglinjen på den andra.
Oral droppar suspension:
vit upphängning.
04.0 KLINISK INFORMATION
04.1 Terapeutiska indikationer
Förebyggande och grundläggande behandling av allergiska sjukdomar, främst vid rinit, yttre astma (exklusive astmaattacker), follikulär konjunktivit, kronisk urtikaria, atopisk dermatit, matallergi. Om det behövs kan TINSET kombineras med andra läkemedel som motsvarar dessa indikationer, förutsatt att deras verkningsmekanism skiljer sig från TINSET.
TINSET är inte indicerat för akut behandling av allergiska tillstånd såsom astmaattack.
04.2 Dosering och administreringssätt
TINSET vuxna 30 mg tabletter,
Vuxna: för varje indikation, 1 tablett, lika med 30 mg två gånger om dagen: efter frukost och efter middagen.
TINSET 25 mg / ml oral droppar suspension Vuxna: för varje indikation 30 droppar, lika med 30 mg två gånger om dagen: efter frukost och efter middagen.
BARN i åldern 1 år eller äldre: för varje indikation:
1 droppe för varje 2 kg kroppsvikt, två gånger om dagen.
För barn som är 1 år eller äldre och med en kroppsvikt på mindre än 12 kg, till exempel för barn med en kroppsvikt över 48 kg, bör läkaren rådfrågas.
Antalet droppar som ska ges till barnet bör beräknas utifrån barnets kroppsvikt.
VARNING: En överdos kan leda till allvarliga biverkningar, särskilt hos barn, därför måste den rekommenderade dosen följas strikt (se avsnitt 4.9). När det gäller användning av suspensionen till barn, särskilt för att undvika oavsiktlig överdos, bör doserna som ska administreras beräknas i droppar.
Produkten har ett liknande utseende som mjölk och kan därför locka uppmärksamhet hos barn, vilket kan öka risken för överdosering hos barn.
04.3 Kontraindikationer
Överkänslighet mot den aktiva substansen, mot cinnarizin eller mot något hjälpämne som anges i avsnitt 6.1.
Kontraindicerat för barn under 1 år. Patienter med nedsatt leverfunktion
04.4 Särskilda varningar och lämpliga försiktighetsåtgärder vid användning
TINSET är inte indicerat för akut behandling av allergiska tillstånd såsom astmaattack.
När Tinset förskrivs till patienter med astma ska pågående läkemedelsbehandling inte stoppas plötsligt, utan gradvis minskas. Detta gäller särskilt för patienter som behandlas med kortikosteroider.
Efter marknadsföring har det rapporterats om hepatit, leverskada, gulsot och förändringar i leverfunktionen (måttlig till stor ökning av leverenzymer), inklusive mycket sällsynta fall av dödligt leversvikt. Patienter bör övervakas noggrant. Observeras för lever Vid onormala levervärden bör lämpliga åtgärder vidtas, såsom att behandlingen avbryts och behandlingen med Tinset inte ska återupptas.
På grund av dess eliminering av levern bör försiktighet iakttas vid förskrivning av oxatomid till patienter med kända leversjukdomar. Vid behov bör behandlingen av dessa patienter helst börja med doser som är halva normaldosen. Intervallet mellan doseringen kan bibehållas oförändrat.
Dyskinesi och extrapyramidala symptom har observerats hos både vuxna och barn. Extrapyramidala symtom var vanligare hos barn. Barn är förmodligen mer mottagliga för effekter på centrala nervsystemet på grund av omogna blod-hjärnbarriär. Därför bör försiktighet iakttas hos barn mellan 1 och 6 år och särskilt barn mellan 12 och 24 månader. Tinset är kontraindicerat för barn under 1 år.
I den geriatriska populationen kan åldersrelaterade fysiologiska förändringar (såsom ökad permeabilitet av blod-hjärnbarriären och minskad levermetabolism) påverka aktiviteten hos H1-receptorantagonister.
Följ de rekommenderade doserna eftersom överdos av antihistaminer ibland kan ge allvarliga effekter, särskilt hos barn.
Tabletterna innehåller laktos, därför bör patienter med sällsynta ärftliga problem med galaktosintolerans, Lapp-laktasbrist eller glukos-galaktosmalabsorption inte ta detta läkemedel.
Suspensionen orala droppar innehåller para-hydroxibensoater som kan orsaka allergiska reaktioner (inklusive fördröjda).
Tinset ska administreras med försiktighet till äldre patienter på grund av ökad risk för sedering.
Drick inte alkohol och ta inte alkoholhaltiga läkemedel under behandling med Tinset (se avsnitt 4.5)
04.5 Interaktioner med andra läkemedel och andra former av interaktion
Oxatomid metaboliseras av cytokrom P450, särskilt till iso 3A4 och eventuellt 2D6, enligt in vitro -studier på humana levermikrosomer.Baserat på in vitro -studier kan det finnas en potentiell interaktion mellan oxatomid och CYP 450 -hämmare, såsom itrakonazol, ketokonazol och cimetidin.
Patienter bör informeras om att Tinset kan öka den lugnande effekten av depressiva medel i centrala nervsystemet, inklusive alkohol, barbiturater, hypnotika, narkotiska smärtstillande medel, lugnande medel, ångestdämpande och antipsykotika (se avsnitt 4.7). Biverkningar av antikolinerga läkemedel kan öka vid samtidig administrering av Samtidig användning av MAO -hämmare och Tinset rekommenderas inte.
Oxatomid, liksom andra antihistaminer, kan störa hudallergentest och därför bör behandlingen avbrytas i minst 3 dagar innan hudtest.
04.6 Graviditet och amning
Graviditet
Inga direkta embryotoxiska, peri- och postnatala toxiska effekter noterades hos djur. Det fanns inga direkta negativa effekter på fertiliteten, medan sekundära effekter endast registrerades vid maternellt toxiska doser. Djurförsöksdata visar begränsad passage av oxatomid över placentabarriären, men säkerheten för Tinset hos gravida kvinnor har inte fastställts. Om det är nödvändigt att administrera Tinset under graviditeten ska de potentiella riskerna noggrant vägas mot de förväntade terapeutiska fördelarna.
Matdags
Det finns otillräcklig information om utsöndringen av oxatomid / metaboliter i bröstmjölk, därför bör amning avbrytas vid behandling med Tinset.
04.7 Effekter på förmågan att framföra fordon och använda maskiner
Eftersom produkten kan orsaka dåsighet och försämra uppmärksamheten, bör de som måste köra fordon eller sköta operationer som kräver vaksamhet vara varnade för detta. Ett samtidigt intag av alkohol kan förstärka dessa effekter.
04.8 Biverkningar
Data från kliniska studier
Säkerheten för Tinset utvärderades hos 1188 patienter (674 vuxna och 514 barn), som deltog i 17 kliniska studier med Tinset (9 studier omfattade endast vuxna, endast 5 barn och 3 båda), med astma, flerårig allergi eller säsongsbunden inklusive rinit, konjunktivit, eksem, atopisk och kontaktdermatit, diabetes, kronisk urtikaria, läkemedelsallergi, matallergi, bronkit eller hudmastocytos.
Dessa patienter tog minst en dos Tinset och säkerhetsdata erhölls.
Patienter behandlades med Tinset under en planerad period på 1 vecka till 15 månader.
Biverkningsfrekvensen definieras med följande konvention:
Mycket vanliga (≥1 / 10)
Vanliga (≥1 / 100,
Mindre vanliga (≥1 / 1000 till
Sällsynta (≥1 / 10.000,
Mycket sällsynta (≤1 / 10 000)
Ingen känd frekvens kan inte uppskattas utifrån tillgängliga data.
Biverkningar som rapporterats för ≥ 1% av patienterna som behandlats med Tinset listas i tabell 1
Mindre vanliga biverkningar rapporterade av
Data efter marknadsföring
Förutom de biverkningar som rapporterats i kliniska prövningar och som listats ovan, har följande biverkningar rapporterats efter marknadsföring (tabell 3).
Rapportering av misstänkta biverkningar
Rapportering av misstänkta biverkningar som inträffar efter godkännande av läkemedlet är viktigt eftersom det möjliggör kontinuerlig övervakning av nytta / riskbalansen för läkemedlet. Vårdpersonal uppmanas att rapportera alla misstänkta biverkningar via det nationella rapporteringssystemet. "Italian Medicines Agency Webbplats: www.agenziafarmaco.gov.it/it/responsabili.
04.9 Överdosering
Symtom: De vanligast rapporterade symtomen efter en överdos är: somnolens, stupor och extrapyramidala symtom som dyskinesi, stel nacke, ofrivilliga ögonrörelser, dystoni och hypertoni. Mindre vanligt är hyperexcitabilitet och agitation. Mydriasis generaliserade muskelspasmer och koma har rapporterats mycket sällan. Mycket sällsynta fall av medvetslöshet och förlängning av QT -intervallet har rapporterats efter överdosering.
Behandling: det finns inga specifika motgift. Behandlingen består av noggrann övervakning av vitala tecken och stödjande åtgärder. Ett EKG bör utföras för att utvärdera QT -intervallet. Om det anses lämpligt kan aktivt kol ges. Extrapyramidala symptom har behandlats framgångsrikt med antikolinerga medel.
05.0 FARMAKOLOGISKA EGENSKAPER
05.1 Farmakodynamiska egenskaper
Farmakoterapeutisk grupp: antihistaminer för systemisk och topisk användning.
ATC -kod: R06AE06 (tabletter och droppar) Oxatomide.
Oxatomid är ett antiallergiskt läkemedel som verkar genom att hämma frisättning och effekter av olika mediatorer.
Blockering eller minskning av receptormedierade effekter för uthållighet (H1), serotonin (5-HT1), leukotriener (LTC3, LTC4) och trombocytaggregationsfaktor (PAF) är känd.Uppkomsten och intensiteten av allergiska reaktioner motverkas ytterligare med oxatomid genom minskning av frisättningen av mediatorer: Genom mobilisering av kalcium utsöndras mediatorerna för den allergiska reaktion som produceras och lagras av mastceller. Denna process hämmas av oxatomiden.
Vid kliniska doser utövar oxatomid inte andra farmakologiska åtgärder än antiallergiska.
05.2 Farmakokinetiska egenskaper
Hos människor absorberas produkten väl efter oral administrering och når en blodtopp inom 2 timmar. Halveringstiden är cirka 14 timmar och når plasmavärden vid steady state (cirka 35 ng / ml med doser på 30 mg två gånger per dag) ), efter 3 dagar. Plasmaproteinbindningen är cirka 98%. Det mesta av den orala dosen utsöndras och metaboliseras med avföring (60%), särskilt via gallan, inklusive via "urinen och mindre än 0,5%av dosen utsöndras oförändrat . De huvudsakliga metaboliska vägarna utförs av levern genom oxidativ N-dealkylering, konjugering och aromatisk hydroxylering.
05.3 Prekliniska säkerhetsdata
Oxatomidens toxicitet har bedömts i en serie prekliniska toxikologiska studier inklusive akut och kronisk toxicitet, reproduktionstoxicitet, gentoxicitet, cancerframkallande och lokala (dermala och okulära) tolerabilitetsstudier.
Oxatomiden visade inte genotoxisk eller cancerframkallande potential hos varken möss eller råttor.
Läkemedlet hade ingen effekt på fertiliteten hos råttor och visade inte teratogen potential hos råttor och kaniner. Vid administrering till råttor vid maternalt toxiska doser visade oxatomid embryofetotoxiska effekter.
06.0 LÄKEMEDELSINFORMATION
06.1 Hjälpämnen
30 mg tabletter: laktos, majsstärkelse, mikrokristallin cellulosa, povidon, utfälld kiseldioxid, magnesiumstearat.
25 mg / ml Oral droppar suspension: mikrogranulär och karmelloscellulosa, povidon, polysorbat 20, metylpara-hydroxibensoat, propylpara-hydroxibensoat, natriumsackarin, renat vatten.
06.2 Oförenlighet
Det finns inga kända kemisk-fysiska oförenligheter mellan oxatomiden och andra föreningar.
06.3 Giltighetstid
TINSET Vuxna 30 mg tabletter, TINSET 25 mg / ml orala droppar, suspension: 5 år.
TINSET 25 mg / ml orala droppar, suspension läkemedlet måste användas inom tre månader efter att flaskan öppnades; efter denna period måste det kvarvarande läkemedlet kasseras.
06.4 Särskilda förvaringsanvisningar
Detta läkemedel kräver inga särskilda förvaringsförhållanden.
06.5 Förpackningens innehåll och förpackningens innehåll
TINSET vuxna 30 mg tabletter
Blister av PVC och aluminium
förpackning: 30 tabletter
TINSET 25 mg / ml orala droppar, suspension:
gul glasflaska med dropp av polypropen och barnsäker stängning
förpackning: 30 ml flaska
06.6 Anvisningar för användning och hantering
För att undvika oavsiktlig överdos, följ strikt de rekommenderade doserna; När det gäller användning av orala suspensionsdroppar hos barn måste doserna som ska administreras beräknas i droppar och flaskan som innehåller suspensionen skakas kraftigt och noggrant före varje användning.
TINSET 25 mg / ml Orala droppar, suspension: barnsäker stängning:
denna typ av förslutning är utformad för att göra det svårt för ett barn att öppna flaskan. Kom ihåg att om vuxen inte stänger flaskan ordentligt enligt instruktionerna nedan, är locket inte längre barnsäkert.
• För att öppna, tryck ned plastlocket med dropparen ordentligt och skruva loss den.
• Stäng den igen efter provtagningen genom att trycka ned plastlocket med dropparen ordentligt och skruva fast den igen.
• För att säkerställa att säkerhetsmekanismen är korrekt aktiverad, vrid locket moturs utan att trycka på och kontrollera att flaskan inte kan öppnas.
Förvara detta läkemedel utom syn- och räckhåll för barn.
07.0 INNEHAVARE AV GODKÄNNANDE FÖR FÖRSÄLJNING
GRUNENTHAL ITALIA S.r.l. - Via Carlo Bo, 11 - 20143 Milano
08.0 NUMMER FÖR FÖRSÄLJNINGSTILLSTÅND
TINSET vuxna 30 mg tabletter, 30 tabletter - A.I.C. n. 025293010
TINSET 25 mg / ml oral droppar suspension, flaska 30 ml - A.I.C. n. 025293034
09.0 DATUM FÖR FÖRSTA GODKÄNNANDE ELLER FÖRNYELSE AV GODKÄNNANDET
Februari 2012
10.0 DATUM FÖR REVISION AV TEXTEN
3 februari 2015