Allmänhet
"Ge mig feber och jag kommer att bota alla sjukdomar": detta uttalande, tillskrivet den grekiska läkaren Hippokrates (400 f.Kr.), vittnar om hur människan länge har förstått värmens terapeutiska potential.
Det första dokumentativa beviset på den möjliga botande effekten av höga temperaturer vid behandling av tumörer går tillbaka till 1866, då den tyska läkaren Busch observerade fullständig remission av ett sarkom i ansiktet på en patient efter upprepade anfall av hög feber.

Idag, på grund av de potentiella terapeutiska fördelarna med denna teknik, erkänns hypertermi som den fjärde pelaren i onkologi.
Vad är onkologisk hypertermi?
Onkologisk hypertermi är en klinisk behandling för behandling av maligna tumörer, som kan användas ensam eller oftare i kombination med strålbehandling och kemoterapibehandlingar.För närvarande används faktiskt inte denna teknik så mycket som ett alternativ, utan som ett tillägg till andra behandlingar mot cancer, denna förening möjliggör erhållande av en ömsesidig förstärkning av den terapeutiska effekten. Dessutom möjliggör sambandet med hypertermi att minska doserna av kemoterapi och strålning, med en betydande minskning av biverkningarna relaterade till standardterapier.
Typer av hypertermi
Den terapeutiska effekten av hypertermi för behandling av tumörer kan utnyttjas med olika metoder och tekniker.
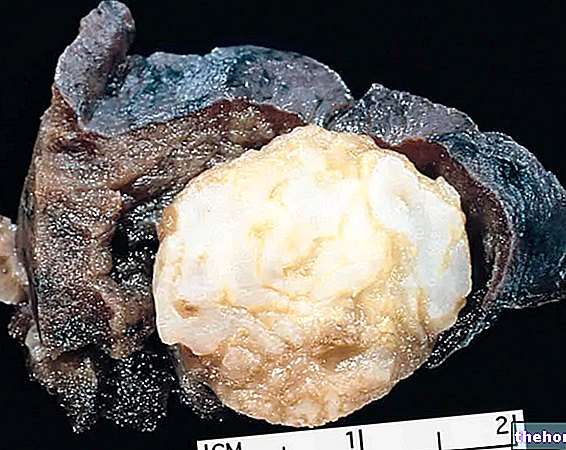
Tumörformer som har visat ett bra svar på hypertermi:
- Melanom och andra former av hudcancer
- Bröstcancer
- Mjukvävnadssarkom
- Blåscancer
- Huvud- och halscancer
- Livmoderhals- och äggstockscancer
- Prostatacancer
- Rektal cancer
- Axillära eller bröstväggscancer
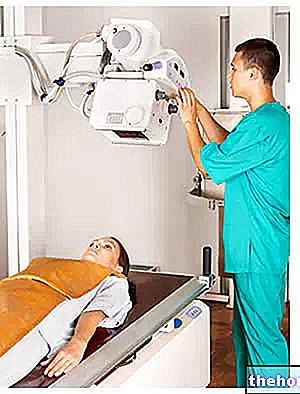
Temperaturen och varaktigheten av exponeringen för värme är de två grundläggande mängderna som ska kalibreras för att uppnå det önskade terapeutiska resultatet. Förutom omfattningen av temperaturen som uppnås och värmans appliceringstid är det dock mycket viktigt att utvärdera källan som genererar uppvärmningen och dess tillämpningsplats, till exempel mikrovågor, radiofrekvenser, nanopartiklar, ultraljud, lasrar kan användas etc. placeras externt eller internt i kroppen.
Alla dessa variabler väljs av onkologen utifrån egenskaperna hos de olika kliniska fallen.
Resultat
Inom onkologi beror chansen att läka från en malign tumör av många faktorer, såsom tumörens typ och stadium, dess storlek och plats, patientens ålder och allmänna hälsotillstånd.
Med tanke på allt detta har flera studier visat att hypertermi utgör ett utmärkt adjuvans för de klassiska behandlingsteknikerna för tumörer, vilket ger få kontraindikationer för patienter.
För vissa typer av tumörer, som associerar strålbehandling (och / eller kemoterapi) med hypertermi, erhölls en ökning med 30-100% av de fullständiga remissionsfrekvenserna och / eller överlevnadsfrekvensen efter 2 och 5 år, jämfört med användning av enbart strålbehandling (och / eller kemoterapi). För vissa cancerformer, såsom endetarmscancer, har behandlingsresultaten visat sig ännu mer uppmuntrande (upp till + 500% av den femåriga överlevnadsfrekvensen).
Klassisk hypertermi 41-45 ° C
Klassisk onkologisk hypertermi syftar till att värma cancerceller utan att skada de omgivande friska vävnaderna.
- Om temperaturen uppnås är mellan 41-43 ° C (mild hypertermi) huvudsyftet är att öka tumörens känslighet för strålbehandling och / eller kemoterapibehandlingar.
- Om de uppnådda temperaturerna ligger mellan 43 och 46 ° C blir värmens direkta effekt på dödandet av cancerceller viktigare.
Beroende på fallet varar den klassiska hypertermi -behandlingen i genomsnitt från 40 till 60 minuter och upprepas två till tre gånger i veckan. Mer frekventa behandlingar tenderar faktiskt att orsaka termoresistens (eller termotolerans om du föredrar det) i cancerceller, vilket gör att de bättre klarar höga temperaturer.
Beroende på fallet kan värmekällan ha olika storlekar och kan placeras på olika djup, i olika organ eller anatomiska delar av människokroppen. Till exempel, bland moderna hypertermi -tekniker finns det också möjlighet att implantera mikrovågsantenner direkt i subcutis.
Hur fungerar det
DIREKT SKADA TILL TUMÖRCELLER
Effekten av onkologisk hypertermi är baserad på tumörvävnadernas kaotiska angiogenes, i grunden presenterar tumormikromiljön nästan alltid en kaotisk och oorganiserad vaskulär ställning; som ett resultat får stora tumörområden (särskilt den centrala massan) otillräckliga mängder blod och syre. På grund av dessa förändringar av blodkärlen kan den neoplastiska massan inte avleda värme som vanliga vävnader; med andra ord, tumörer tenderar att lida mycket mer värme än friska vävnader, eftersom vissa av deras områden får lite blod (vilket fungerar som en riktig kylvätska); av samma anledning lider dessa områden redan av brist på syre och näringsämnen och överflöd av avfallsprodukter (hyperacidifiering).
Värmen som administreras av hypertermi orsakar skador på plasmamembranet, cellskelettet och kärnan; om hypertermiens omfattning och varaktighet är tillräcklig, leder denna skada direkt till tumörcellens död. Direkt skada blir betydande vid temperaturer> 43 ° C: indirekta skador, som vi kommer att se inom kort, är istället typiska för den så kallade "mild hypertermi" (42-43 ° C).
INDIREKT SKADA: ADJUVANT HYPERTERMI
Vår kropp reagerar på den lokala temperaturhöjningen genom att öka blodflödet till det drabbade området. På detta sätt "absorberar" större mängder cirkulerande blod värme, vilket bevarar vävnaderna från termisk skada. Detta svar förekommer också på tumörnivån, så - inom gränserna för den säregna vaskulära disorganiseringen - får tumörceller som utsätts för en liten temperaturökning högre mängder blod och syre:
- antitumörläkemedel kan finnas i blodet, som tack vare vasodilatation som induceras av hypertermi lättare kan nå de mindre vaskulariserade neoplastiska områdena; verkan av dessa läkemedel kan också underlättas av cellulär (ökad permeabilitet av plasmamembranet) och enzymatiska förändringar (proteindaturering) inducerade av värme.
När temperaturer i tumörmassan överstiger 43 ° C registreras å andra sidan en minskning av tumörblodflödet, med påföljande "infångning" av läkemedelsmolekylerna.
Fördelarna med kombinationen hypertermi-kemoterapi har bekräftats av flera studier. Antitumörläkemedel som Melphalan, Bleomycin, Adriamycin, Mitomycin C, Nitrosuree, Cisplatin är mer effektiva vid administrering under hypertermi. I detta avseende bör det dock betonas att inte alla kända kemoterapiläkemedel finner en förbättring av deras effektivitet om de används i en hypertermisk miljö. - Den större tillförseln av syre till tumörvävnaden förstärker effekterna av strålbehandling, som huvudsakligen baseras på DNA -skada som orsakas av reaktiva syrearter (fria radikaler) som genereras av strålning. cellulär kompromiss kopplad till skadan som tidigare orsakats av hypertermin.
Den ömsesidiga kompletteringen och förstärkningen av åtgärderna mellan hypertermi och strålbehandling beror på att:- skadan som orsakas av hypertermi är större i områden med låg vaskularisering (som inte effektivt kan sprida värme), såsom den neoplastiska nodulens hypoxiska centrala kärna;
- skadan som orsakas av strålterapi är istället större i områden med hög vaskularisering (syrerikare), såsom de perifera mantelområdena i tumörknölen;
- de två behandlingarna utför sin maximala skadliga effekt på tumören i olika faser av cellcykeln, och kompletterar också i denna mening.
Den maximala terapeutiska vinsten verkar uppnås genom att öva den hypertermiska behandlingen inom en eller två timmar efter strålterapipasset. När det gäller termokemoterapi kan dock de två behandlingarna också utföras samtidigt.
Onkologisk hypertermi kan bidra till minskning av tumörmassan med tanke på en kirurgisk avlägsnandeoperation. Det finns också fördelar när det gäller smärtstillande effekt (minskning av smärta som utlöses av vävnadens kompression av den neoplastiska massan).
Andra former av hypertermi
TOTAL KROPPSHYPERTERI
Som namnet antyder tillhandahåller denna form av hypertermi uppvärmning av hela organismen. Syftet är i detta fall inte att direkt förstöra tumörmassan, utan att bestämma dess indirekta remission med hjälp av ett immunförstärkning. Quest " Den senare har faktiskt en inneboende förmåga att förstöra cancerceller, och denna förmåga ökar enormt under förhållanden med hög kroppstemperatur.
Syftet med totalkroppshyperteri är att framkalla en artificiell feber, som simulerar en feberattack runt 39-41 ° C. I detta avseende kan termiska eller vattentäckta kammare användas.
Användningen av totalkroppen är mestadels begränsad till den experimentella inställningen för behandling av diffusa metastaser. Tekniken kräver noggrann övervakning av patienten för att undvika skador från hypertermi, vilket också kan vara mycket allvarligt. Det är också en adjuvant behandling, från ska därför användas tillsammans med andra behandlingar mot cancer.
INTERSTIZIAL HYPERTERI
Såsom framgår av brachyterapi - där små radioaktiva källor implanteras i målvävnaden - "innebär interstitiell hypertermi implantation av anordningar som kan generera" lokal hypertermi. Antenner används i detta avseende som värmer tack vare tillförsel av mikrovågsugn.
INFUSIONELL HYPERTERI och PERFUSIONSHYPERTERI
Intraperitoneal infusionshypertermi är baserad på användning av peritonealtvättar med medicinska lösningar vid höga temperaturer. Det används i fall av peritoneala neoplasmer som är svåra att behandla, såsom peritonealt mesoteliom och magcancer. Andra tekniker för hypertermi är baserade på samma princip, som inbegriper infusion av terapeutiska lösningar som värms upp i andra hålrum, såsom pleural eller urinblåsa.
Vid perfusionshyperteri används extrakorporeal cirkulation, med uppvärmning av en del av blodet och återinförande av detta med tillsats av kemoterapeutiska läkemedel, för att erhålla höga läkemedelskoncentrationer i den perfunderade vävnaden.
ABLATIV HYPERTERI
I detta fall är temperaturerna mycket högre (50-100 ° C), men de appliceras bara i några minuter. Sådana temperaturer kan producera en omedelbar och total nekros av de behandlade vävnaderna. Värmen genereras genom applicering av en växelström genom elektroder eller genom användning av laser eller elektromagnetisk strålning, applicerad direkt på tumörmassan (invasiv behandling). Den största svårigheten ligger i att bevara de friska vävnaderna som omger tumören.
Även om denna teknik utnyttjar värmens terapeutiska effekt, går den för verkningsmekanismen utöver vad som är det traditionella begreppet hypertermi.
NYA UTVECKLINGAR I "HYPERTERMIENS OMRÅDE"
Vetenskapen om hypertermi utvecklas ständigt för att utveckla alltmer selektiva behandlingar för att förstöra cancerceller utan att skada friska.
Den senaste utvecklingen gäller den icke-invasiva termometri med användning av magnetiska resonansskannrar (för att utvärdera temperaturen i de olika tumörområdena), hypertermi magneto-vätska och användning av värmekänsliga liposomer. De senare är läkemedel inneslutna i lipidvesiklar, stabila vid normala kroppstemperaturer men som kan släppa ut innehållet vid temperaturer av cirka 40-43 ° C; dessa läkemedel representerar därför den perfekta kombinationen med regionala behandlingar med hypertermi.
Gränser
Att förstå hypertermins verkningsmekanismer och de följaktliga potentiella fördelarna vid behandling av tumörer kan leda till överdriven entusiasm hos läsaren inför denna typ av behandling.
Även om det stöds av rättvisa bevis på effekt, behåller tillämpningen av hypertermi i onkologi några kritiska frågor. För det första, i klinisk praxis kan det finnas kontraindikationer eller gränser som gör ingreppet opraktiskt; vissa tekniker, till exempel, möjliggör verkliga mer eller mindre invasiva kirurgiska ingrepp; andra är fortfarande begränsade mest till experimentmiljön. Det är också nödvändigt för att övervinna gränser. tekniker relaterade till värmeemission, penetrationsdjup, termogenens homogenitet och behovet av en korrekt termisk dos för att undvika skador på friska vävnader. I detta avseende är ytterligare studier och teknisk utveckling önskvärd för att utveckla effektiva protokoll och standardiserade för att antas i olika kliniska situationer.