Aktiva ingredienser: Brinzolamid, Timolol
AZARGA 10 mg / ml + 5 mg / ml ögondroppar, suspension
Varför används Azarga? Vad är det för?
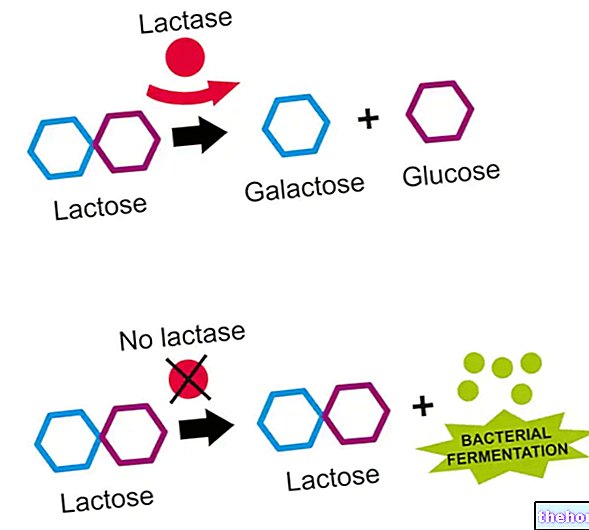
AZARGA innehåller två aktiva ingredienser, brinzolamie och timolol, som arbetar tillsammans för att minska trycket i ögat.
AZARGA används för att behandla högt tryck i ögat, även kallat glaukom eller okulär hypertoni, hos patienter över 18 år och vars högt tryck i ögat inte effektivt kan kontrolleras av ett läkemedel ensamt.
Kontraindikationer När Azarga inte ska användas
Använd inte AZARGA
- om du är allergisk mot brinzolamid, mot läkemedel som kallas sulfonamider (till exempel läkemedel som används för att behandla diabetes och infektioner och även diuretika (tabletter för att främja diures), mot timolol, betablockerare (läkemedel som används för att sänka blodtrycket eller för att behandla hjärtsjukdomar) eller något annat innehållsämne i detta läkemedel (anges i avsnitt 6)
- om du har eller har haft andningsproblem som astma, svår kronisk obstruktiv bronkit (svår lungsjukdom som kan orsaka väsande andning, andningssvårigheter och / eller långvarig hosta) eller andra typer av andningsproblem.
- vid svår hösnuva
- om du har långsamma hjärtslag, hjärtsvikt eller hjärtrytmstörningar (oregelbunden hjärtslag).
- om du har för mycket surhet i ditt blod (ett tillstånd som kallas hyperkloremisk acidos).
- om du har allvarliga njurproblem.
Försiktighetsåtgärder vid användning Vad du behöver veta innan du tar Azarga
Sätt bara AZARGA -droppar i ögonen.
Tala med din läkare eller apotekspersonal innan du använder AZARGA om du lider av eller tidigare har lidit av
- kranskärlssjukdom (symtom kan vara bröstsmärta eller täthet, väsande andning eller kvävning), hjärtsvikt, lågt blodtryck.
- förändringar i hjärtfrekvensen såsom långsam puls.
- andningssvårigheter, astma eller kronisk obstruktiv lungsjukdom.
- dålig cirkulationssjukdom (som Raynaulds sjukdom eller Raynaulds syndrom)
- diabetes, eftersom timolol kan dölja tecken och symtom på lågt blodsocker
- överaktiv sköldkörtel, eftersom timolol kan dölja tecken och symtom på sköldkörtelsjukdom
- muskelsvaghet (myasthenia gravis)
- Innan en operation, tala om för din läkare att du använder AZARGA, eftersom timolol kan förändra effekterna av vissa läkemedel som används under anestesi.
- om du tidigare har haft atopi (en tendens att utveckla en allergisk reaktion) och allvarliga allergiska reaktioner kan det vara mer troligt att du får en allergisk reaktion med användning av AZARGA och adrenalinbehandling kanske inte är tillräckligt effektiv för att behandla reaktionen. har någon annan behandling, tala om för din läkare eller sjuksköterska att du tar AZARGA.
- om du har leverproblem.
- om du har torra ögon eller problem med hornhinnan.
- om du har njurproblem.
Barn och ungdomar
AZARGA rekommenderas inte för barn och ungdomar under 18 år.
Interaktioner Vilka läkemedel eller livsmedel kan förändra effekten av Azarga
Tala om för din läkare eller apotekspersonal om du använder, nyligen har använt eller kan tänkas använda andra läkemedel.
AZARGA kan interagera med andra läkemedel du tar, inklusive andra ögondroppar för att behandla glaukom. Tala om för din läkare om du tar eller har för avsikt att ta läkemedel för att sänka blodtrycket, såsom parasympatomimetika och guanetidin eller andra hjärtmediciner inklusive kinidin (används för att behandla hjärtproblem och vissa typer av malaria), amiodaron eller andra läkemedel för att behandla hjärtrytmstörningar och glykosider för hjärtsvikt.
Tala också om för din läkare om du tar eller tänker ta läkemedel för att behandla diabetes, eller för att behandla magsår eller svampdödande medel, antivirala läkemedel eller antibiotika eller antidepressiva medel som kallas fluoxetin och paroxetin.
Tala om för din läkare om du tar en annan kolsyraanhydrashämmare (acetazolamid eller dorzolamid).
Varningar Det är viktigt att veta att:
Graviditet och amning
Du ska inte använda AZARGA om du är gravid eller blir gravid om inte din läkare anser det nödvändigt. Tala med din läkare innan du använder AZARGA.
Använd inte AZARGA medan du ammar, timolol kan utsöndras i bröstmjölk. Rådfråga din läkare innan du använder något läkemedel under amning.
Köra och använda maskiner
Kör inte eller använd maskiner förrän din syn är klar. Din syn kan vara suddig en stund direkt efter att du har använt AZARGA.
En av de aktiva ingredienserna kan minska förmågan att utföra operationer som kräver mental uppmärksamhet och / eller fysisk koordination. Om du upplever detta symptom, var försiktig när du kör fordon eller använder maskiner.
AZARGA innehåller bensalkoniumklorid
AZARGA innehåller ett konserveringsmedel (bensalkoniumklorid) som kan missfärga mjuka kontaktlinser och kan orsaka ögonirritation. Bär därför inte kontaktlinser medan du tar AZARGA. Vänta 15 minuter efter att du har använt AZARGA innan du sätter tillbaka dina kontaktlinser.
Dos, metod och administreringstid Hur man använder Azarga: Dosering
Använd alltid detta läkemedel enligt läkarens eller apotekspersonalens anvisningar. Kontakta din läkare eller apotekspersonal om du är osäker.
Om du byter ögondroppar som tidigare använts för behandling av glaukom med AZARGA, ska du sluta använda det andra läkemedlet och börja använda AZARGA dagen efter. Kontakta din läkare eller apotekspersonal om du är osäker.
Följande är användbart för att begränsa mängden medicin som kommer in i blodet efter applicering av ögondropparna:
- Håll ögonlocket stängt och applicera samtidigt ett försiktigt tryck med ett finger på ögonets inre hörn nära näsan i minst 2 minuter.
Den rekommenderade dosen är en droppe i det / de drabbade ögat, två gånger om dagen.
Använd endast AZARGA i båda ögonen om din läkare säger till dig det. Använd läkemedlet under den tid som din läkare rekommenderar.
Hur man använder det
- Ta flaskan och en spegel.
- Tvätta händerna.
- Skaka väl innan användning.
- Skruva loss flasklocket. Ta bort locket efter att locket har lossnat, ta bort det innan du använder produkten.
- Ta flaskan, vänd den upp och ner och håll den mellan tummen och pekfingret.
- Du lutar huvudet bakåt. Dra ned det nedre locket med ett rent finger, så att en "ficka" bildas mellan locket och ögat, droppen kommer att gå dit (figur 1).
- Håll flaskans spets nära ögat. Använd spegeln om det hjälper.
- Rör inte ögat eller ögonlocket, omgivande områden eller andra ytor med flaskans spets. Det kan infektera ögondropparna.
- Pressa försiktigt på flaskans botten för att släppa en droppe AZARGA i taget.
- Tryck inte hårt på flaskan: den är konstruerad för att fungera med lågt tryck på botten (figur 2).
- Efter att ha använt AZARGA, tryck på ögonvrån nära näsan med fingret i 2 minuter (figur 3). Detta hjälper till att förhindra att AZARGA sprider sig till resten av kroppen.
- Om du behöver lägga dropparna i båda ögonen, upprepa stegen för det andra ögat.
- Skruva tillbaka locket direkt efter användning.
- Avsluta en flaska innan du öppnar nästa.
Om en droppe saknar ditt öga, försök igen.
Om du använder andra ögondroppar eller ögonsalvor, låt det gå minst 5 minuter mellan varje läkemedels instillation. Oftalmiska salvor ska ges sist.
Om du har glömt att ta AZARGA, fortsätt med nästa dos enligt schemat. Ta inte en dubbel dos för att kompensera för en glömd dos. Använd inte mer än en droppe i de drabbade ögonen två gånger om dagen.
Om du slutar att ta AZARGA utan att tala med din läkare kommer ditt intraokulära tryck inte att kontrolleras med eventuell synförlust.
Fråga din läkare eller apotekspersonal om du har ytterligare frågor om användningen av detta läkemedel.
Överdosering Vad du ska göra om du har tagit för mycket Azarga
Om du har tagit mer AZARGA än du borde, tvätta genast ögat med ljummet vatten. Använd inte dropparna förrän det är dags för nästa dos.
Du kan uppleva minskad puls, minskat blodtryck, hjärtsvikt, andningssvårigheter och ditt nervsystem kan påverkas.
Biverkningar Vilka är biverkningarna av Azarga
Liksom alla läkemedel kan detta läkemedel orsaka biverkningar men alla användare behöver inte få dem.
Sluta använda detta läkemedel och kontakta din läkare omedelbart om du får utslag, allvarliga hudreaktioner eller intensiv rodnad eller klåda i ögat. Dessa kan vara tecken på en allergisk reaktion (frekvensen är inte känd).
Du kan vanligtvis fortsätta att använda dropparna, såvida inte effekterna är allvarliga. Om du är orolig, tala med din läkare eller apotekspersonal. Sluta inte använda AZARGA utan att först tala med din läkare.
Vanliga biverkningar (kan förekomma hos upp till 1 av 10 användare)
- Effekter i ögat: dimsyn, tecken och symptom på ögonirritation (t.ex. brännande, irritation, klåda, rivning, rodnad), ögonsmärta.
- Allmänna biverkningar: smakstörning
Mindre vanliga biverkningar (kan förekomma hos upp till 1 av 100 användare)
- Effekter i ögat: erosion av hornhinnan (skada på ögonglobens främre yta), intraokulär inflammation, ljuskänslighet, onormal ögonkänslighet, okulär urladdning, torra ögon, trötta ögon, ögonlock.
- Allmänna biverkningar: lågt blodtryck, hosta, sömnsvårigheter (sömnlöshet).
Ingen känd frekvens (kan inte beräknas utifrån tillgängliga data)
- Effekter i ögat: synstörning, skada på synnerven, ökat ögontryck, avlagringar på ögonytan, störningar i hornhinnan, minskad ögonkänslighet, inflammation eller infektion i konjunktiva, onormal, dubbel eller nedsatt syn, ökad ögonpigmentering, tillväxt på ögats yta, ökad rivning, ögonsvullnad, ljuskänslighet, minskad tillväxt eller antal ögonfransar, hängande övre ögonlock (ögat förblir halvstängt), inflammation i ögonlocken och ögonlockskörtlar, inflammation i hornhinnan och lossning av skiktet under näthinnan som innehåller blodkärlen efter filteroperationer som kan orsaka synstörningar, minskad hornhinnekänslighet.
- Hjärta och cirkulation: förändringar i rytm eller puls, långsam puls, hjärtklappning, en typ av hjärtrytmstörning, bröstsmärta, nedsatt hjärtfunktion, hjärtinfarkt, ökat blodtryck, minskad blodtillförsel till hjärnan, stroke, ödem (vätska uppbyggnad), kongestivt hjärtsvikt (hjärtsjukdom med andfåddhet och svullnad i fötter och ben på grund av vätskeansamling), svullnad i extremiteterna, lågt blodtryck, förändring i färg på fingrar och fötter och ibland andra områden i kropp (Raynauds fenomen), kalla händer och fötter.
- Andningsvägar: sammandragning av luftvägarna i lungorna (främst hos patienter med redan befintlig sjukdom), andfåddhet eller andningssvårigheter, kalla symtom, bröststockning, infektion i näsgångar, nysningar, täppt näsa, torr näsa, rinnande näsa, blödning näsa, astma, halsirritation.
- Nervsystemet och allmänna störningar: depression, mardrömmar, minnesförlust, huvudvärk, nervositet, irritabilitet, trötthet, tremor, onormal känsla, svimning, yrsel, sömnighet, generaliserad eller svår svaghet, ovanliga känslor som nålar.
- Mage: illamående, kräkningar, diarré, tarmgas eller buksmärtor, inflammation i halsen, känsla av torr eller onormal mun, matsmältningsbesvär, magont
- Blod: blodprov som visar onormala leverfunktionsvärden, ökade klorhalter i blodet, minskat antal röda blodkroppar
- Allergi: ökade allergisymtom, generaliserade allergiska reaktioner inklusive svullnad under huden som kan förekomma i områden som ansikte och lemmar och som kan hindra luftvägarna och orsaka svårigheter att svälja eller andas, nässelutslag, lokaliserade och generaliserade utslag, klåda, allvarligt plötsligt liv -hotande allergiska reaktioner.
- Öra: ringningar i öronen, yrsel eller yrsel
- Hud: hudutslag, rodnad eller inflammation i huden, minskad eller onormal hudkänslighet, håravfall, silverfärgade hudutslag (psorasiforma utslag) eller försämring av psoriasis.
- Muskel: generaliserad rygg-, led- eller muskelsmärta som inte orsakas av träning, muskelspasmer, extremitetsvärk, muskelsvaghet / svaghet, ökade tecken och symtom på myasthenia gravis (muskelsjukdom).
- Njurar: ryggontliknande njursmärta i nedre delen av ryggen, ofta urinering
- Reproduktion: sexuell dysfunktion, minskad libido, manlig sexuell svårighet.
- Metabolism: låga blodsockernivåer
Rapportering av biverkningar
Tala med din läkare eller apotekspersonal om du får några biverkningar. Detta gäller även biverkningar som inte anges i denna bipacksedel. Du kan också rapportera biverkningar direkt via det nationella rapporteringssystemet som anges i bilaga V. Genom att rapportera biverkningar kan du hjälpa till att ge mer information om läkemedlets säkerhet.
Giltighetstid och lagring
Förvara detta läkemedel utom syn- och räckhåll för barn.
Använd inte detta läkemedel efter utgångsdatum som anges på flaskan och kartongen efter EXP. Utgångsdatumet avser den sista dagen i månaden.
Detta läkemedel kräver inga särskilda förvaringsförhållanden.
För att förhindra infektioner, kassera flaskan 4 veckor efter första öppnandet och använd en ny flaska. Skriv öppningsdatumet i utrymmet på flaskan och kartongen.
Kasta inga läkemedel i avloppsvatten eller hushållsavfall. Fråga din apotekare om hur du ska kasta läkemedel som du inte använder längre. Detta skyddar miljön.
Deadline "> Annan information
Vad AZARGA innehåller
- De aktiva ingredienserna är brinzolamid och timolol. En ml suspension innehåller 10 mg brinzolamid och 5 mg timolol (som maleat).
- Övriga innehållsämnen är bensalkoniumklorid (se avsnitt 2 "AZARGA innehåller bensalkoniumklorid"), karbopol 974P, dinatriumedetat, mannitol (E421), renat vatten, natriumklorid, tyloxapol, saltsyra och / eller natriumhydroxid. Små mängder saltsyra och / eller natriumhydroxid tillsätts för att bibehålla normala surhetsnivåer (pH -nivåer).
Hur AZARGA ser ut och förpackningens innehåll
AZARGA är en vätska (vit till benvit enhetlig suspension) som levereras i en förpackning som innehåller en 5 ml plastflaska med ett skruvlock eller i en förpackning som innehåller tre 5 ml flaskor.
Alla förpackningsstorlekar kanske inte marknadsförs.
Bipacksedel: AIFA (Italian Medicines Agency). Innehåll publicerat i januari 2016. Den information som finns finns kanske inte uppdaterad.
För att få tillgång till den senaste versionen är det lämpligt att gå till AIFA (Italian Medicines Agency) webbplats. Ansvarsfriskrivning och användbar information.
01.0 LÄKEMEDLETS NAMN -
AZARGA 10 mg / ml + 5 mg / ml ögondroppar, upphängning
02.0 KVALITATIV OCH KVANTITATIV SAMMANSÄTTNING -
En ml suspension innehåller 10 mg brinzolamid och 5 mg timolol (som timololmaleat).
Hjälpämne med känd effekt:
En ml suspension innehåller 0,10 mg bensalkoniumklorid.
För fullständig förteckning över hjälpämnen, se avsnitt 6.1.
03.0 LÄKEMEDELSFORM -
Ögondroppar, suspension (ögondroppar).
Vit till benvit enhetlig suspension, pH 7,2 (ungefär).
04.0 KLINISK INFORMATION -
04.1 Terapeutiska indikationer -
Minskning av intraokulärt tryck (IOP) hos vuxna patienter med öppenvinkelglaukom eller okulär hypertoni för vilka monoterapi ger otillräcklig IOP -reduktion (se avsnitt 5.1).
04.2 Dosering och administreringssätt -
Dosering
Användning till vuxna, inklusive äldre
Dosen är en droppe AZARGA i konjunktivsäcken i det / de drabbade ögat två gånger om dagen.
Systemisk absorption reduceras genom att nasolakrimalkanalen stängs eller ögonlocket sänks i 2 minuter. På så sätt kan minskningen av systemiska biverkningar och ökad lokal aktivitet uppnås (se avsnitt 4.4).
Om du missar en dos, fortsätt behandlingen med nästa dos enligt schemat. Dosen bör inte överstiga en droppe två gånger om dagen per påverkat öga.
När AZARGA används som ersättning för ett annat antiglaukommedicin ska det andra läkemedlet avbrytas och AZARGA -behandlingen startas dagen efter.
Särskilda populationer
Pediatrisk population
Säkerhet och effekt för AZARGA hos barn och ungdomar i åldern 0 till 18 år har ännu inte fastställts.
Inga data finns tillgängliga.
Nedsatt lever- och njurfunktion
Studier med AZARGA eller ögondroppar som innehåller timolol 5 mg / ml har inte utförts på patienter med nedsatt lever- eller njurfunktion. Ingen dosjustering krävs hos patienter med nedsatt leverfunktion eller hos patienter med nedsatt njurfunktion.
AZARGA har inte studerats hos patienter med allvarligt nedsatt njurfunktion (kreatininclearance hyperkloremisk acidos (se avsnitt 4.3). Eftersom brinzolamid och dess huvudsakliga metabolit övervägs utsöndras av njurarna, är AZARGA kontraindicerat hos patienter med allvarligt nedsatt njurfunktion (se avsnitt 4.3).
AZARGA ska användas med försiktighet till patienter med allvarligt nedsatt leverfunktion (se avsnitt 4.4).
Administreringssätt
För oftalmisk användning.
Patienter bör uppmanas att skaka flaskan väl före användning. När säkerhetsringen har lossnat, ta bort den innan produkten används.
För att förhindra kontaminering av droppflaskans spets och lösning, var försiktig så att du inte vidrör ögonlocken, omgivande områden eller andra ytor med flaskans droppspets. Instruera patienter att hålla flaskan tätt stängd när den inte används.
Vid samtidig användning av mer än ett aktuellt oftalmiskt läkemedel ska läkemedlet administreras med ett intervall på minst 5 minuter.
Oftalmiska salvor ska administreras sist.
04.3 Kontraindikationer -
• Överkänslighet mot de aktiva substanserna eller mot något hjälpämne.
• Överkänslighet mot andra betablockerare
• Överkänslighet mot sulfonamider (se avsnitt 4.4.)
• Reaktiv luftvägssjukdom, inklusive bronkial astma och en "historia av bronkial astma, svår kronisk obstruktiv lungsjukdom."
• Sinusbradykardi, sjuk sinus syndrom, sino-förmaksblock, andra eller tredje gradens atrioventrikulära block som inte kontrolleras med en pacemaker. Manifest hjärtsvikt eller kardiogen chock.
• Allvarlig allergisk rinit
• Hyperkloremisk acidos (se avsnitt 4.2).
• allvarligt nedsatt njurfunktion.
04.4 Varningar och lämpliga försiktighetsåtgärder vid användning -
Systemiska effekter
• Brinzolamid och timolol absorberas systemiskt. På grund av den beta-adrenerga komponenten i timolol kan samma typer av kardiovaskulära, lung- och andra biverkningar som ses med betasubstanser uppstå.-adrenerga blockerare administreras systemiskt. Förekomsten av systemiska biverkningar efter topikal oftalmisk administrering är lägre än vad som ses efter systemisk administrering För att minska systemisk absorption se avsnitt 4.2.
• Överkänslighetsreaktioner som är gemensamma för alla sulfonamidderivat kan förekomma hos patienter som behandlas med AZARGA, eftersom läkemedlet absorberas systemiskt.
Hjärtpatologier
Hos patienter med kardiovaskulär sjukdom (t.ex. kranskärlssjukdom, Prinzmetals angina och hjärtsvikt) och hypotoni bör betablockerare utvärderas kritiskt och behandling med andra aktiva substanser bör övervägas. Tecken på förvärring av dessa sjukdomar och oönskade reaktioner bör övervakas hos patienter med hjärt -kärlsjukdom.
På grund av den negativa effekten på ledningstiden bör betablockerare administreras med försiktighet till patienter med första gradens hjärtblock.
Kärlsjukdomar
Patienter med allvarliga perifera cirkulationsstörningar / störningar (t.ex. allvarliga former av Raynaulds sjukdom eller Raynaulds syndrom) bör behandlas med försiktighet.
Hypertyreos
Betablockerare kan också dölja tecknen på hypertyreoidism.
Muskelsvaghet
Beta-adrenergblockerande läkemedel har rapporterats öka muskelsvaghet relaterade till vissa symptom på myastheni (t.ex. diplopi, ptos och generaliserad svaghet).
Andningspatologier
Andningsreaktioner, inklusive död på grund av bronkospasm hos patienter med astma, har rapporterats efter administrering av vissa oftalmiska betablockerare.
Hos patienter med mild till måttlig kronisk obstruktiv lungsjukdom ska AZARGA användas med försiktighet och endast om den potentiella nyttan överväger den potentiella risken.
Hypoglykemi / diabetes
Betablockerare ska administreras med försiktighet till patienter med spontan hypoglykemi eller till patienter med labil diabetes, eftersom betablockerare kan dölja tecken och symtom på akut hypoglykemi.
Störningar i syra / basbalansen
AZARGA innehåller brinzolamid, en sulfonamid. Samma typer av biverkningar som kan hänföras till sulfonamider kan uppstå vid topisk administrering. Syra / basstörningar har rapporterats vid oral användning av kolsyraanhydrashämmare.Detta läkemedel ska användas med försiktighet hos patienter som riskerar nedsatt njurfunktion på grund av den möjliga risken för metabolisk acidos.Sluta använda detta läkemedel om tecken på allvarliga reaktioner eller överkänslighet observeras.
Mental vakenhet
Orala kolsyraanhydrashämmare kan försämra förmågan att utföra uppgifter som kräver mental vakenhet eller fysisk koordination.AZARGA absorberas systemiskt och därför kan detta inträffa efter topisk administrering.
Anafylaktiska reaktioner
När du tar beta-blockerare, patienter med tidigare atopi eller allvarlig anafylaktisk reaktion på ett flertal allergener kan vara mer reaktiva vid upprepad kontakt med sådana allergener och kanske inte svara på de vanliga doserna av adrenalin som används för att behandla anafylaktiska reaktioner.
Frigörelse av choroid
Choroidavlossning har rapporterats efter administrering av terapi för minskning av vattenhaltig humorproduktion (t.ex. timolol, acetazolamid) efter filtreringsprocedurer.
Kirurgisk anestesi
Betablockerande oftalmologiska preparat kan blockera de systemiska beta-agonisteffekterna av t.ex. adrenalin.Narkosläkaren bör informeras när patienten tar timolol.
Samtidig behandling
Effekten på intraokulärt tryck eller kända systemiska effekter av betablockerare kan förstärkas när timolol administreras till patienter som redan får ett systemiskt beta-blockerande medel. Sådana patienters respons bör övervakas noggrant. Aktuellt om två beta-adrenerga blockeringar medel eller två kolsyraanhydrashämmare rekommenderas inte (se avsnitt 4.5).
Additiva effekter på de kända systemiska effekterna av kolsyraanhydrashämmare kan förekomma hos patienter som får AZARGA och en oral kolsyraanhydrashämmare. Samtidig administrering av AZARGA och orala kolsyraanhydrashämmare har inte studerats och rekommenderas inte (se avsnitt 4.5).
Okulära effekter
Det finns begränsad erfarenhet av AZARGA vid behandling av patienter med pseudoexfoliativt eller pigmentärt glaukom. Försiktighet bör iakttas vid behandling av dessa patienter och noggrann övervakning av IOP rekommenderas.
AZARGA har inte studerats hos patienter med trångvinkelglaukom och dess användning rekommenderas inte till dessa patienter.
Oftalmiska betablockerare kan orsaka torra ögon. Patienter med hornhinnesjukdom bör behandlas med försiktighet.
Brinzolamidens möjliga roll för hornhinnans endotelfunktion hos patienter med nedsatt hornhinna (särskilt hos patienter med låga endotelceller) har inte studerats. Patienter med kontaktlinser har inte studerats specifikt och för dessa patienter rekommenderas noggrann övervakning under användning av brinzolamid, eftersom kolsyraanhydrashämmare kan försämra hornhinnans hydratisering och kontaktlinsförslitning kan öka risken för hornhinnan. Noggrann övervakning av patienter med hornhinnor rekommenderas. nedsatt, liksom patienter med diabetes mellitus eller hornhinnedystrofier.
AZARGA kan användas när du använder kontaktlinser under noggrann observation (se under "Benzalkoniumklorid")
Bensalkoniumklorid
AZARGA innehåller bensalkoniumklorid som kan orsaka ögonirritation och är känt för att missfärga mjuka kontaktlinser. Kontakt med mjuka kontaktlinser bör undvikas. Patienter bör rådas att ta bort kontaktlinser före användning. Applicering av AZARGA och vänta 15 minuter efter dosering sätta in dem igen.
Bensalkoniumklorid har också rapporterats orsaka punkterad keratopati och / eller toxisk ulcerös keratopati. Noggrann övervakning krävs vid frekvent eller långvarig användning.
Nedsatt leverfunktion
AZARGA ska användas med försiktighet till patienter med allvarligt nedsatt leverfunktion.
04.5 Interaktioner med andra läkemedel och andra former av interaktion -
Inga läkemedelsinteraktionsstudier har utförts med AZARGA.
AZARGA innehåller brinzolamid, en kolsyraanhydrashämmare och absorberas systemiskt även om den administreras lokalt.Syra / basstörningar har rapporterats vid oral användning av kolsyraanhydrashämmare. Möjligheten till interaktion bör övervägas hos patienter som får AZARGA.
Potentialen för en additiv effekt på de kända systemiska effekterna av kolsyraanhydrashämning finns hos patienter som behandlas med orala kolsyraanhydrashämmare och ögondroppar som innehåller brinzolamid. Samtidig administrering av ögondroppar som innehåller brinzolamid och orala kolsyraanhydrashämmare rekommenderas inte.
Cytokrom P -isoenzymer-450 ansvariga för metabolismen av brinzolamid inkluderar CYP3A4 (den huvudsakliga), CYP2A6, CYP2B6, CYP2C8 och CYP2C9. CYP3A4 -hämmare som ketokonazol, itrakonazol, klotrimazol, ritonavir och troleandomycin förväntas hämma metabolismen av brinzolamid via CYP3A4. Försiktighet bör iakttas om CYP3A4 -hämmare används samtidigt. Eftersom eliminering främst sker via njuren är det dock osannolikt att ackumulering av brinzolamid uppstår. Brinzolamid är inte en hämmare av cytokrom P -isoenzymer-450.
Additiva effekter som hypotoni och / eller markerad bradykardi kan uppstå när en oftalmisk lösning av betablockerare administreras samtidigt med orala kalciumkanalblockerare, beta-adrenerga blockerande medel, antiarytmika (inklusive amiodaron), digitalisglykosider, parasympatomimetika, guanetidin.
Betablockerare kan minska responsen på adrenalin som används för att behandla anafylaktiska reaktioner. Särskild försiktighet bör iakttas hos patienter som tidigare haft atopi eller anafylaksi (se avsnitt 4.4).
Den hypertensiva reaktionen vid plötslig utsättning av klonidin kan förstärkas när du tar betablockerare. Försiktighet iakttas vid samtidig användning av detta läkemedel med klonidin.
Potentiering av beta har rapporterats under kombinerad behandling med CYP2D6 -hämmare (t.ex. kinidin, fluoxetin, paroxetin) och timolol.-systemiskt block (t.ex. minskad hjärtfrekvens, depression). Försiktighet rekommenderas.
Betorna-blockerare kan förstärka den hypoglykemiska effekten av antidiabetika-blockerare kan dölja tecken och symtom på hypoglykemi (se avsnitt 4.4).
Mydriasis har ibland rapporterats efter samtidig användning av oftalmiska betablockerare och adrenalin (adrenalin).
04.6 Graviditet och amning -
Graviditet
Det finns inga adekvata data om oftalmisk användning av brinzolamid och timolol hos gravida djurstudier med brinzolamid har visat reproduktionstoxicitet efter systemisk administrering, se avsnitt 5.3 AZARGA ska inte användas under graviditet om det inte är absolut nödvändigt. systemisk absorption se avsnitt 4.2.
Epidemiologiska studier har inte visat missbildande effekter men visar risk för intra-uterin tillväxthämning när betablockerare ges oralt. Dessutom har tecken och symtom på betablockerare effekter (t.ex. bradykardi, hypotoni, andningssvårigheter och hypoglykemi) observerats hos nyfödda när betablockerare har administrerats fram till tidpunkten för förlossningen. Om AZARGA administreras fram till förlossningen bör det nyfödda barnet övervakas noggrant under de första dagarna i livet.
Matdags
Det är inte känt om oftalmisk brinzolamid utsöndras i bröstmjölk hos människa. Djurstudier har visat att brinzolamid utsöndras i bröstmjölk efter oral administrering, se avsnitt 5.3.
Betablockerare utsöndras i bröstmjölk. Vid terapeutiska doser av timolol i ögondroppar är det dock osannolikt att tillräckliga mängder finns i bröstmjölk för att ge kliniska symptom på betablockerare hos spädbarnet. För att minska systemisk absorption, se avsnitt 4.2.
En risk för spädbarn kan dock inte uteslutas. Beslutet att avbryta amning eller AZARGA -behandling bör fattas med hänsyn till fördelarna med amning för barnet och nyttan med terapi för kvinnan.
Fertilitet
Prekliniska data visar ingen effekt av brinzolamid eller timolol på manlig eller kvinnlig fertilitet. Inga effekter på manlig eller kvinnlig fertilitet förväntas med användning av AZARGA.
04.7 Effekter på förmågan att framföra fordon och använda maskiner -
AZARGA har försumbar påverkan på förmågan att framföra fordon och använda maskiner.
Övergående dimsyn, liksom andra synstörningar, kan försämra förmågan att framföra fordon eller använda maskiner.
Kolsyraanhydrashämmare kan försämra förmågan att utföra operationer som kräver mental uppmärksamhet och / eller fysisk koordination (se avsnitt 4.4).
04.8 Biverkningar -
Sammanfattning av säkerhetsprofilen
I kliniska studier var de vanligaste biverkningarna suddig syn, ögonirritation och ögonsmärta, som inträffade hos cirka 2% till 7% av patienterna.
Tabell över biverkningar
Följande biverkningar har rapporterats under kliniska studier och övervakning efter marknadsföring med AZARGA och de enskilda komponenterna brinzolamid och timolol.De klassificeras enligt följande konvention: mycket vanliga (> 1/10), vanliga (> 1/100 till 1/1000 till 1/10 000 till
1 biverkningar observerade för Azarga
Ytterligare två biverkningar observerade med enbart timolol
3 ytterligare biverkningar observerade med enbart brinzolamid
Beskrivning av utvalda biverkningar
Dysgeusi (bitter eller ovanlig smak i munnen efter instillation) var en ofta systemiskt förekommande biverkning i samband med användning av AZARGA under kliniska prövningar. Detta beror troligen på att ögondropparna passerar in i näsofarynxen genom nasolakrimalkanalen och kan tillskrivas brinzolamid. Nasolakrimal ocklusion eller lätt stängning av ögonlocket efter instillation kan bidra till att minska förekomsten av denna effekt (se avsnitt 4.2).
AZARGA innehåller brinzolamid, en sulfonamidhämmare av kolsyraanhydras med systemisk absorption. Magtarmkanalen, nervsystemet, hematologiska, njur- och metaboliska effekter är i allmänhet associerade med systemiska kolsyraanhydrashämmare. Samma typ av biverkningar som kan hänföras till orala kolsyraanhydrashämmare är möjliga med topisk administrering.
Timolol absorberas i systemcirkulationen. Detta kan orsaka biverkningar liknande de som ses med systemiska betablockerande läkemedel. De listade oönskade reaktionerna inkluderar reaktioner som finns i klassen oftalmiska betablockerare. Ytterligare biverkningar förknippade med användningen av de enskilda komponenterna som kan förekomma med AZARGA finns i tabellen ovan. Se avsnitt 4.2 för att minska systemisk absorption.
Pediatrisk population
AZARGA rekommenderas inte för barn och ungdomar under 18 år på grund av brist på data om säkerhet och effekt.
Rapportering av misstänkta biverkningar
Rapportering av misstänkta biverkningar som inträffar efter godkännande av läkemedlet är viktigt eftersom det möjliggör kontinuerlig övervakning av läkemedlets nytta / riskbalans.Hälso- och sjukvårdspersonal uppmanas att rapportera alla misstänkta biverkningar via det nationella rapporteringssystemet. I bilaga V.
04.9 Överdosering -
Vid oavsiktligt intag kan symptom på överdosering av betablockerare innefatta bradykardi, hypotoni, hjärtsvikt och bronkospasm.
Vid överdosering med AZARGA ögondroppar bör behandlingen vara symptomatisk och stödjande. På grund av brinzolamid kan elektrolytobalans, utveckling av ett tillstånd av acidos och möjliga effekter på det centrala nervsystemet uppstå. Serumelektrolytnivåer (särskilt kalium) och blodets pH -nivåer bör övervakas. Studier har visat att timolol inte lätt dialyserar.
05.0 FARMAKOLOGISKA EGENSKAPER -
05.1 "Farmakodynamiska egenskaper -
Farmakoterapeutisk grupp: oftalmologer, antiglaukompreparat och miotika.
ATC -kod: S01ED51.
Handlingsmekanism
AZARGA innehåller två aktiva ingredienser: brinzolamid och timololmaleat. Dessa två komponenter minskar förhöjt intraokulärt tryck (IOP) främst genom att minska utsöndringen av vattenhaltig humor, men genom olika verkningsmekanismer. Den kombinerade effekten av dessa två aktiva ingredienser bestämmer en ytterligare minskning av IOP jämfört med det enda intaget av varje komponent.
Brinzolamid är en potent hämmare av humant kolsyraanhydras II (CA-II), det dominerande isoenzymet i ögat. Inhiberingen av kolsyraanhydras vid nivån av ögonets ciliära processer minskar utsöndringen av vattenhaltig humor, förmodligen på grund av en avmattning i bildandet av bikarbonatjoner med en följd av minskad transport av natrium och vätska.
Timolol är ett icke-selektivt adrenergt blockerande medel som inte har inneboende sympatomimetisk aktivitet, direkt myokardial depressiv aktivitet eller membranstabiliserande aktivitet. Tonografi- och fluorofotometri -studier på människor indikerar att dess dominerande verkan är relaterad till en minskning av bildandet av vattenhaltig humor och en liten ökning av utflödets lätthet.
Farmakodynamiska effekter
Kliniska effekter:
I en tolv månaders kontrollerad klinisk studie på patienter med öppenvinkelglaukom eller okulär hypertoni som enligt utredarens mening skulle kunna dra nytta av kombinationsbehandling och som hade ett genomsnittligt baslinjärt intraokulärt tryck mellan 25 och 27 mmHg, den genomsnittliga intraokulära trycksänkande effekten av AZARGA administrerat två gånger dagligen varierade från 7 till 9 mmHg. AZARGAs inferioritet gentemot dorzolamid 20 mg / ml + timolol 5 mg / ml i genomsnittlig IOP-minskning visades vid alla tidpunkter vid alla besök.
I en sex månaders kontrollerad klinisk studie på patienter med öppenvinkelglaukom eller okulär hypertoni och genomsnittligt intraokulärt tryck mellan 25 och 27 mmHg inkluderades den genomsnittliga intraokulära tryckreducerande effekten av AZARGA administrerad två gånger dagligen mellan 7 och 9 mmHg och upp till 3 mmHg högre än brinzolamid 10 mg / ml administrerat två gånger dagligen och upp till 2 mmHg högre än timolol 5 mg / ml administrerat två gånger dagligen. Statistiskt större minskning av genomsnittlig IOP jämfört med både brinzolamid och timolol observerades vid alla tidpunkter vid alla besök.
I tre kontrollerade kliniska prövningar var okulärt obehag efter instillation av AZARGA signifikant mindre än obehag som känns efter instillation av 20 mg / ml dorzolamid + 5 mg / ml timolol.
05.2 "Farmakokinetiska egenskaper -
Absorption
Efter lokal okulär administrering absorberas brinzolamid och timolol genom hornhinnan och in i den systemiska cirkulationen. I en farmakokinetisk studie fick friska försökspersoner oral brinzolamid (1 mg) två gånger dagligen i 2 veckor för att förkorta tiden till steady state innan AZARGA startades. Efter administrering av AZARGA två gånger dagligen i 13 veckor var de genomsnittliga koncentrationerna av röda blodkroppar (RBC) för brinzolamid 18,8 ± 3,29 mcM, 18,1 ± 2,68 mcM och 18, 4 ± 3,01 μM vid 4, 10 respektive 15 veckor, vilket visar att steady-state-koncentrationer av brinzolamid i RBC upprätthölls.
Vid steady state efter administrering av AZARGA, medelvärdet av Cmax och AUC0-12 timmar i plasma av timolol var 27% respektive 28% lägre (Cmax: 0,824 ± 0,453 ng / ml; AUC0-12h: 4,71 ± 4,29 ng h / ml), jämfört med administrering av 5 mg / ml timolol (Cmax: 1,13 ± 0,494 ng / ml; AUC0-12 timmar: 6,58 ± 3,18 ng h / ml). Den lägre systemiska exponeringen för timolol efter administrering av AZARGA är inte kliniskt relevant.Efter administrering av AZARGA uppnåddes medelvärdet för Cmax för timolol vid 0,79 ± 0,45 timmar.
Distribution
Plasmaproteinbindningen av brinzolamid är måttlig (cirka 60%). Brinzolamid utsöndras i röda blodkroppar på grund av dess höga affinitetsbindning till CA-II och i mindre utsträckning till CA-I. Dess metabolit N-Aktiv desetyl-brinzolamid ackumuleras i röda blodkroppar genom att huvudsakligen binda till CA-I. Affiniteten för brinzolamid och metaboliten till CA i de röda blodkropparna och vävnaden resulterar i låga plasmakoncentrationer.
Distributionsdata i kaninernas ögonvävnad visade att timolol kan mätas i vattenhaltig humor i upp till 48 timmar efter administrering av AZARGA. Vid steady state detekteras timolol i human plasma i upp till 12 timmar efter administrering. Av AZARGA
Biotransformation
De metaboliska vägarna för brinzolamid innefattar N.-dealkylation, O-dealkylering och oxidation av dess N -sidokedja-propyl. N-desetyl-brinzolamid är en viktig metabolit av brinzolamid som bildas hos människor, som också kan binda till CA-I i närvaro av brinzolamid och ackumuleras i röda blodkroppar.n vitro visade att metabolismen av brinzolamid huvudsakligen involverar CYP3A4 -isoenzymet samt minst fyra andra isoenzymer (CYP2A6, CYP2B6, CYP2C8 och CYP2C9).
Timolol metaboliseras på två sätt. Den ena vägen producerar en etanolamin -sidokedja på tiadiazolringen och den andra producerar en etanol -sidokedja på morfolin -kväveatomen och en andra liknande sidokedja med en karbonylgrupp intill kvävet. Metabolismen av timolol medieras huvudsakligen av CYP2D6 -isoenzymet.
Eliminering
Brinzolamid elimineras främst via njurutsöndring (cirka 60%). Ungefär 20% av dosen återvinns i urinen som en metabolit. Brinzolamid och N-desetyl-brinzolamid är huvudkomponenterna i urinen, tillsammans med spår (-desmetyl .
Timolol och dess metaboliter utsöndras huvudsakligen genom njurarna. Ungefär 20% av en dos timolol utsöndras oförändrat i urinen och resten utsöndras i urinen som metaboliter. T1 / 2 av timolol i plasma är 4,8 timmar efter okulär administrering av AZARGA.
05.3 Prekliniska säkerhetsdata -
Brinzolamid
Icke-kliniska data avslöjar ingen särskild fara för människor med brinzolamid baserat på konventionella studier av säkerhetsfarmakologi, toxicitet vid upprepade doser, gentoxicitet och cancerframkallande potential.
Utvecklingstoxicitetsstudier på kaniner med orala doser av brinzolamid upp till 6 mg / kg / dag (214 gånger den rekommenderade kliniska dagliga dosen på 28 mcg / kg / dag) visade ingen effekt på fostrets utveckling trots betydande toxicitet. Liknande studier på råttor visade något minskad benbildning av skallen och bröstbenet hos foster från mödrar som fick brinzolamid i doser på 18 mg / kg / dag (642 gånger den rekommenderade kliniska dagliga dosen), men inte vid doser på 6 mg / kg / dag . Dessa resultat inträffade vid doser som orsakade metabolisk acidos med en minskning av moderns kroppsviktstillväxt och fostervikt.
En minskning av fosterdosens vikt-beroende observerades hos valpar till mödrar som fick brinzolamid oralt med variabel läsbar minskning (cirka 5-6%) med 2 mg / kg / dag upp till cirka 14% med 18 mg / kg / dag. Under amning var halten av inga negativa effekter hos avkomman 5 mg / kg / dag.
Timolol
Icke-kliniska data avslöjar ingen särskild fara för människor med timolol baserat på konventionella studier av säkerhetsfarmakologi, toxicitet vid upprepade doser, genotoxicitet och cancerframkallande potential.Reproduktionstoxicitetsstudier med timolol har visat fördröjd fostring i fostret hos råttor. Utan några negativa effekter på postnatal utveckling ( vid 50 mg / kg / dag eller 3500 gånger den dagliga kliniska dosen på 14 mcg / kg / dag) och en ökning av fostrets resorptioner hos kaniner (vid 90 mg / kg / dag eller 6400 gånger den dagliga kliniska dosen).
06.0 LÄKEMEDELSINFORMATION -
06.1 Hjälpämnen -
Bensalkoniumklorid
Mannitol (E421)
Carbopol 974P
Tyloxapol
Dinatriumedetat
Natriumklorid
Saltsyra och / eller natriumhydroxid (för pH -justering)
Renat vatten
06.2 Inkompatibilitet "-
Inte relevant.
06.3 Giltighetstid "-
2 år.
4 veckor efter första öppnandet.
06.4 Särskilda förvaringsanvisningar -
Detta läkemedel kräver inga särskilda förvaringsförhållanden.
06.5 Förpackningens innehåll och förpackningens innehåll -
5 ml ogenomskinliga lågdensitetspolyetenrunda flaskor, med droppare och vitt skruvlock av polypropylen (DROP-TAINER) innehållande 5 ml suspension.
Kartonger innehållande 1 eller 3 flaskor. Alla förpackningsstorlekar kanske inte marknadsförs.
06.6 Anvisningar för användning och hantering -
Inga speciella instruktioner.
07.0 INNEHAVARE AV "MARKNADSFÖRINGANDE GODKÄNNANDE" -
Alcon Laboratories (UK) Ltd.
Frimley Business Park
Frimley
Camberley
Surrey, GU16 7SR
08.0 NUMMER FÖR FÖRSÄLJNINGSTILLSTÅND -
EU / 1/08/482 / 001-002
038837011
038837023
09.0 DATUM FÖR FÖRSTA GODKÄNNANDE ELLER FÖRNYELSE AV GODKÄNNANDE -
Datum för första godkännandet: 25 november 2008
Datum för senaste förnyelse: 26 augusti 2013
10.0 DATUM FÖR REVISION AV TEXTEN -
D.CCE mars 2015