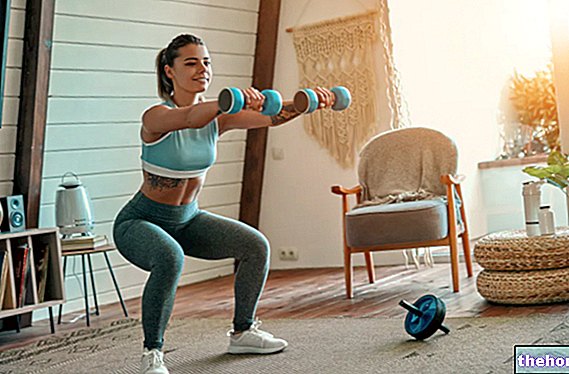Aktiva ingredienser: Degarelix
FIRMAGON 80 mg pulver och vätska till injektionsvätska, lösning
Firmagon -förpackningsinsatser är tillgängliga för förpackningsstorlekar:- FIRMAGON 80 mg pulver och vätska till injektionsvätska, lösning
- FIRMAGON 120 mg pulver och vätska till injektionsvätska, lösning
Varför används Firmagon? Vad är det för?
FIRMAGON innehåller degarelix. Degarelix är en kemiskt syntetiserad hormonblockerare som används vid behandling av prostatacancer hos vuxna manliga patienter. Degarelix efterliknar ett naturligt hormon (gonadotropinfrisättande hormon, GnRH) och blockerar dess effekt direkt. Genom att göra detta minskar degarelix omedelbart nivån av det manliga hormonet testosteron som stimulerar prostatacancer.
Kontraindikationer När Firmagon inte ska användas
Använd inte FIRMAGON - om du är allergisk mot degarelix eller något annat innehållsämne i detta läkemedel.
Försiktighetsåtgärder för användning Vad du behöver veta innan du tar Firmagon
Tala om för din läkare om du har följande tillstånd:
- Du har hjärt- eller hjärtrytmproblem (arytmi) eller använder läkemedel för att behandla detta problem. Hjärtrytmproblem kan förvärras med användning av FIRMAGON.
- Du lider av diabetes mellitus. Förvärring eller början av diabetes kan förekomma. Om du är diabetiker måste du mäta ditt blodsocker oftare.
- Lider av leverproblem. Du kan behöva kontrollera din leverfunktion.
- Du lider av njursjukdom. Användningen av FIRMAGON har inte studerats hos patienter med svår njursjukdom.
- Du har osteoporos eller något annat tillstånd som påverkar styrkan i dina ben. Minskade testosteronnivåer kan orsaka en minskning av kalcium i benen (gallring av benen).
- Lider av svår överkänslighet. Användningen av FIRMAGON har inte studerats hos patienter med allvarliga överkänslighetsreaktioner.
Barn och ungdomar
Ge inte detta läkemedel till barn eller ungdomar.
Interaktioner Vilka läkemedel eller livsmedel kan ändra effekten av Firmagon
FIRMAGON kan störa vissa läkemedel som används för hjärtrytmproblem (t.ex. kinidin, prokainamid, amiodaron och sotalol) eller andra läkemedel som kan påverka hjärtrytmen (t.ex. ett antibiotikum), antipsykotika).
Tala om för din läkare om du tar eller nyligen har tagit eller kan tänkas ta andra läkemedel, även receptfria sådana.
Varningar Det är viktigt att veta att:
För dig som bedriver sportaktiviteter
Användningen av läkemedlet utan terapeutisk nödvändighet utgör dopning och kan i alla fall avgöra positiva antidopningstester.
Köra och använda maskiner
Trötthet och yrsel är vanliga biverkningar som kan påverka förmågan att framföra fordon och använda maskiner. Dessa effekter kan bero på behandlingen eller själva sjukdomen.
Dos, metod och administreringstid Hur man använder Firmagon: Dosering
Detta läkemedel måste vanligtvis administreras av en läkare eller sjuksköterska.
Den rekommenderade startdosen är två på varandra följande 120 mg injektioner. Du får sedan en injektion på 80 mg per månad. Den injicerade vätskan bildar en gel som frigör degarelix under en period av en månad.
FIRMAGON ska ENDAST injiceras under huden (subkutant). FIRMAGON får INTE injiceras i ett blodkärl (intravenöst). Försiktighetsåtgärder bör vidtas för att undvika oavsiktlig injektion i en ven. Injektionspunkten måste varieras inom bukområdet.
Om du har glömt att använda FIRMAGON
Om du tror att du har glömt din månatliga dos FIRMAGON, informera din läkare. Fråga din läkare om du har ytterligare frågor om användningen av detta läkemedel.
Instruktioner för korrekt användning
NOTERA:
SKAKA INTE VIKLARNA
Förpackningen innehåller en injektionsflaska med pulver och en förfylld spruta med vätska som måste förberedas för subkutan injektion.
- Ta bort locket från förpackningen på flaskans adapter. Fäst adaptern på pulverflaskan genom att trycka ned tills spetsen passerar genom gummiproppen och adaptern klickar på plats.
- Förbered den förfyllda sprutan genom att sätta i kolven
- Ta bort den förfyllda sprutlocket. Fäst sprutan på injektionsflaskan med pulver genom att skruva fast den på adaptern. Överför allt lösningsmedel till pulverflaskan.
- Håll sprutan insatt i adaptern, virvla försiktigt tills vätskan är klar och fri från oupplösta partiklar eller pulver. Om pulvret fäster vid injektionsflaskan ovanför vätskans yta kan flaskan lutas något. Skaka för att förhindra skumning. en ring av små luftbubblor på vätskeytan är acceptabel. Beredningsförfarandet tar vanligtvis några minuter, men i vissa fall kan det ta upp till 15 minuter.
- Vänd flaskan upp och ner och dra upp till injektionssprutans markeringslinje. Se alltid till att aspirera den exakta volymen och justera för eventuella bubblor.
- Lossa sprutan från adaptern och sätt in den djupa subkutana injektionsnålen i sprutan.
- Ge en djup subkutan injektion. För att göra detta: ta tag i buken, lyft den subkutana vävnaden och sätt in nålen djupt i en vinkel på inte mindre än 45 grader. Injicera långsamt 4 ml FIRMAGON 80 mg omedelbart efter beredning. *
- Injektioner ska inte ges i områden där patienten kan utsättas för tryck, till exempel i bältesområdet, där det finns band eller nära revbenen. Injicera inte direkt i en ven. Dra försiktigt tillbaka sprutkolven för att kontrollera om blod har sugits upp. Om det finns blod i sprutan får medicinen inte längre användas, stoppa proceduren och kasta sprutan och nålen (rekonstituera en ny dos för patienten).
* Kemisk-fysisk stabilitet har visats under användning i 2 timmar vid 25 ° C. Ur mikrobiologisk synvinkel, om inte rekonstitutionsmetoden utesluter risken för bakteriell kontaminering, ska produkten användas omedelbart. Om den inte används omedelbart är användarens tid och tid för användningen.
Biverkningar Vilka är biverkningarna av Firmagon
Liksom alla läkemedel kan detta läkemedel orsaka biverkningar men alla användare behöver inte få dem.
Allvarliga allergiska reaktioner mot detta läkemedel är sällsynta. Kontakta din läkare omedelbart om du utvecklar allvarliga utslag, klåda eller andnöd eller svårigheter. Dessa kan vara symptom på en allvarlig allergisk reaktion.
Mycket vanliga (kan drabba fler än 1 av 10 användare)
Spolning, smärta och rodnad på injektionsstället. Biverkningar på injektionsstället är vanligare med startdosen och mindre vanliga med underhållsdosen.
Vanliga (kan drabba upp till 1 av 10 användare)
- svullnad, knölar och härdning på injektionsstället
- frossa, feber eller influensaliknande syndrom efter injektion
- sömnstörningar, trötthet, yrsel, huvudvärk
- viktökning, illamående, diarré, höga nivåer av vissa leverenzymer
- överdriven svettning (inklusive nattsvett), utslag
- anemi
- smärta och muskuloskeletala störningar
- minskning av testikelvolym, bröstsvullnad, impotens.
Mindre vanliga (kan drabba upp till 1 av 100 användare)
- förlust av sexlust, testikelsmärta, bäckensmärta, ejakulatoriskt misslyckande, könsirritation, bröstsmärta
- depression, psykiska förändringar
- hudrodnad, håravfall, hudknölar, domningar
- allergiska reaktioner, nässelfeber, klåda
- minskad aptit, förstoppning, kräkningar, muntorrhet, buksmärtor och obehag, ökat blodsocker / diabetes mellitus, ökat kolesterol, förändringar i kalcium i blodet, minskad vikt
- ökat blodtryck, hjärtrytmförändringar, EKG -förändringar (QT -förlängning), känsla av onormalt hjärtslag, dyspné, perifert ödem
- muskelsvaghet, muskelspasmer, ledsvullnad / stelhet, osteoporos / osteopeni, ledvärk
- frekvent lust att urinera, urinträngning, svårighet eller smärta vid urinering, urinering på natten, nedsatt njurfunktion, inkontinens
- suddig syn
- obehag på injektionsstället inklusive minskat blodtryck och hjärtfrekvens (vasovagal reaktion)
- obehag
Sällsynta (kan förekomma hos upp till 1 av 1000 användare)
- Febril neutropeni (mycket lågt antal vita blodkroppar i kombination med feber) hjärtinfarkt, hjärtsvikt.
Mycket sällsynta (kan förekomma hos upp till 1 av 10 000 användare)
- Infektion, abscess och nekros vid injektionsstället
Rapportering av biverkningar
Tala med din läkare om du får några biverkningar. Detta inkluderar eventuella biverkningar som inte nämns i denna bipacksedel. Du kan också rapportera biverkningar direkt via det nationella rapporteringssystemet.
Genom att rapportera biverkningar kan du hjälpa till att ge mer information om läkemedlets säkerhet.
Giltighetstid och lagring
Förvara detta läkemedel utom syn- och räckhåll för barn.
Använd inte detta läkemedel efter utgångsdatum som anges på injektionsflaskor, sprutor och kartong. Utgångsdatumet avser den sista dagen i den månaden.
Detta läkemedel kräver inga särskilda förvaringsanvisningar.
Efter rekonstituering
Detta läkemedel är stabilt i 2 timmar vid 25 ° C.
På grund av risken för mikrobiell kontaminering bör detta läkemedel användas omedelbart. Om det inte används omedelbart är användningen av detta läkemedel användarens ansvar.
Kasta inga läkemedel i avloppsvatten eller hushållsavfall. Fråga din apotekare om hur du ska kasta läkemedel som du inte använder längre. Detta skyddar miljön.
Annan information
Vad FIRMAGON innehåller
- Den aktiva substansen är degarelix. Varje injektionsflaska innehåller 80 mg degarelix (som acetat). Efter beredning innehåller 1 ml av den beredda lösningen 20 mg degarelix
- Den andra ingrediensen i pulvret är mannitol (E421).
- Lösningsmedlet är vatten för injektionsvätskor.
Hur FIRMAGON -lådan ser ut och vad den innehåller
FIRMAGON är pulver och vätska till injektionsvätska, lösning. Pulvret har ett vitt till benvitt utseende. Lösningsmedlet är en klar, färglös lösning.
FIRMAGON finns i två förpackningar.
Förpackning med 1 bricka innehållande: 1 injektionsflaska med pulver innehållande 80 mg degarelix och 1 förfylld spruta innehållande 4,2 ml lösningsmedel, 1 kolv, 1 ampulladapter och 1 injektionsnål.
Förpackning med 3 brickor innehållande: 3 injektionsflaskor med pulver innehållande 80 mg degarelix och 3 förfyllda sprutor innehållande 4,2 ml lösningsmedel, 3 kolvar, 3 ampuller och 3 injektionsnålar.
Alla förpackningar kanske inte är till salu.
Bipacksedel: AIFA (Italian Medicines Agency). Innehåll publicerat i januari 2016. Den information som finns finns kanske inte uppdaterad.
För att få tillgång till den senaste versionen är det lämpligt att gå till AIFA (Italian Medicines Agency) webbplats. Ansvarsfriskrivning och användbar information.
01.0 LÄKEMEDLETS NAMN
FIRMAGON 80 mg pulver och lösningsmedel för injicerbar lösning
02.0 KVALITATIV OCH KVANTITATIV SAMMANSÄTTNING
Varje injektionsflaska innehåller 80 mg degarelix (i acetatform).
Efter beredning innehåller varje ml lösning 20 mg degarelix.
För fullständig förteckning över hjälpämnen, se avsnitt 6.1.
03.0 LÄKEMEDELSFORM
Pulver och vätska till injektionsvätska, lösning.
Pulver: Vitt till benvitt pulver.
Lösningsmedel: Klar, färglös lösning.
04.0 KLINISK INFORMATION
04.1 Terapeutiska indikationer
FIRMAGON är en gonadotropinfrisättande hormon (GnRH) -antagonist indikerad för behandling av vuxna manliga patienter med avancerad hormonberoende prostatacancer.
04.2 Dosering och administreringssätt
Dosering
Den första underhållsdosen ska ges en månad efter startdosen.
Den terapeutiska effekten av degarelix bör övervakas med hjälp av kliniska parametrar och serumprostataspecifika antigennivåer (PSA). Kliniska studier har visat att undertryckande av testosteronnivåer (T) sker omedelbart efter administrering av initialdosen, med serumtestosteronnivåer som motsvarar nivåerna för medicinsk kastration (Ttestosteron (T
För patienter med suboptimalt svar måste det bekräftas att serumtestosteronnivåerna förblir tillräckligt undertryckta.
Eftersom degarelix inte inducerar testosteronhöjningar är det inte nödvändigt att kombinera ett antiandrogen som skydd mot ökningen i början av behandlingen.
Särskilda populationer
Äldre, patienter med nedsatt lever- eller njurfunktion:
Ingen dosjustering är nödvändig hos äldre eller hos patienter med lätt till måttligt nedsatt lever- eller njurfunktion (se avsnitt 5.2). Inga studier har utförts på patienter med allvarligt nedsatt lever- eller njurfunktion och därför rekommenderas försiktighet vid behandling (se avsnitt 4.4).
Pediatrisk population
Det finns ingen specifik användning av FIRMAGON hos barn och ungdomar vid behandling av manliga vuxna med hormonberoende prostatacancer.
Administreringssätt
FIRMAGON måste rekonstitueras före administrering. Se avsnitt 6.6 för rekonstituerings- och administrationsanvisningar.
FIRMAGON är endast för subkutan användning, administreras inte intravenöst.
Intramuskulär administrering rekommenderas inte eftersom den inte har studerats.
FIRMAGON administreras genom subkutan injektion i bukområdet. Injektionsstället bör bytas regelbundet. Injektioner ska ges i områden utan tryck, till exempel bort från bälten eller elastiska band och inte nära revbenen.
04.3 Kontraindikationer
Överkänslighet mot den aktiva substansen eller mot något hjälpämne, listad i avsnitt 6.
04.4 Särskilda varningar och lämpliga försiktighetsåtgärder vid användning
Effekter på QT / QTc -intervallet
Långvarig androgenbristbehandling kan förlänga QT-intervallet. Periodiska (månatliga) uppföljningselektrokardiogram (EKG) utfördes i den bekräftande studien där FIRMAGON jämfördes med leuprorelin; ett intervall observerades med båda terapierna. QT / QTc större än 450 msek i cirka 20% av patienterna och mer än 500 msek hos 1% och 2% av patienterna i degarelix- respektive leuprorelingrupperna (se avsnitt 5.1).
FIRMAGON har inte studerats hos patienter med tidigare korrigerat QT -intervall över 450 msek, hos patienter med historia eller riskfaktorer för torsades de pointes och hos patienter som samtidigt behandlas med läkemedel som kan förlänga QT -intervallet. nytta / risk -förhållande vid behandling med FIRMAGON bör övervägas noggrant hos sådana patienter (se avsnitt 4.5 och 4.8).
En grundlig QT -studie visade att det inte fanns någon inneboende effekt av degarelix på QT / QTc -intervallet (se avsnitt 4.8).
Nedsatt leverfunktion
Patienter med kända eller misstänkta leverproblem ingick inte i långvariga kliniska studier med degarelix. Måttliga, övergående förhöjningar av ALAT och ASAT observerades, inte åtföljda av förhöjningar av bilirubin eller kliniska symptom. Övervakning av leverfunktion rekommenderas hos patienter med kända eller misstänkta leversjukdomar under behandlingen. Farmakokinetiken för degarelix studerades efter intravenös engångsadministration hos patienter med lätt till måttligt nedsatt leverfunktion (se avsnitt 5.2).
Nedsatt njurfunktion
Degarelix har inte studerats hos patienter med allvarligt nedsatt njurfunktion, därför rekommenderas försiktighet hos sådana patienter.
Överkänslighet
Degarelix har inte studerats hos patienter med en historia av svår obehandlad astma, anafylaktiska reaktioner eller svår urtikaria eller angioödem.
Förändringar i bentäthet
Fall av minskad bentäthet har rapporterats i den medicinska litteraturen hos män som genomgår orkiektomi eller behandlas med GnRH -agonister. Det kan antas att långa perioder av undertryckande av testosteronnivåer hos människor kan ha effekter på bentätheten, bentäthet har inte mätts under behandling med degarelix.
Glukostolerans
En minskning av glukostolerans observerades hos män som genomgick orchiektomi eller behandlades med GnRH -agonister. Utvecklingen eller försämringen av diabetes kan observeras, därför bör diabetespatienter underkastas mer frekvent övervakning av blodsockernivåer när de genomgår androgenbristbehandling.Effekten av degarelix på insulin och glukosnivåer har inte studerats.
Hjärt-kärlsjukdomar
Hos patienter som genomgår androgenberövningsbehandling har kardiovaskulära sjukdomar såsom stroke och hjärtinfarkt rapporterats i litteraturen. Därför måste alla kardiovaskulära riskfaktorer beaktas.
04.5 Interaktioner med andra läkemedel och andra former av interaktion
Inga formella läkemedelsinteraktionsstudier har utförts.
Eftersom behandling med androgenbrist kan förlänga QTc -intervallet bör samtidig användning av degarelix med läkemedel som är kända för att förlänga QTc -intervallet eller läkemedel som kan inducera torsade de pointes, såsom klass IA -antiarytmika, noga övervägas, t.ex. kinidin, disopyramid) eller klass III (t.ex. amiodaron, sotalol, dofetilide, ibutilide), metadon, moxifloxacin, antipsykotika, etc. (se avsnitt 4.4).
Degarelix är inte ett substrat för det mänskliga CYP450 -systemet och har inte visat någon induktion eller hämning in vitro av CYP1A2, CYP2C8, CYP2C9, CYP2C19, CYP2D6, CYP2E1 eller CYP3A4 / 5. Därför är kliniskt signifikanta farmakokinetiska interaktioner mellan läkemedel kopplade till de ovan nämnda isoenzymerna osannolika.
04.6 Graviditet och amning
Graviditet och amning
Det finns inga indikationer för användning av FIRMAGON hos kvinnor.
Fertilitet
FIRMAGON kan hämma manlig fertilitet så länge testosteron undertrycks.
04.7 Effekter på förmågan att framföra fordon och använda maskiner
FIRMAGON har ingen eller försumbar påverkan på förmågan att framföra fordon och använda maskiner. Trötthet och vingling är vanliga biverkningar som kan påverka förmågan att framföra fordon eller använda maskiner.
04.8 Biverkningar
Sammanfattning av säkerhetsprofilen
De vanligast observerade biverkningarna under behandling med degarelix i bekräftande fas III -studier (N = 409) beror på de förväntade fysiologiska effekterna av testosteronsuppression, och inkluderar rodnad och viktökning (observerad hos 25% respektive 7% av de behandlade patienterna under ett år) eller biverkningar på injektionsstället. Övergående debut av frossa, feber eller influensaliknande symptom har rapporterats (hos 3%, 2% respektive 1% av patienterna) inom timmar efter administrering.
Biverkningar på injektionsstället rapporterades huvudsakligen smärta och erytem, rapporterade hos 28%respektive 17%av patienterna, svullnad (6%), induration (4%) och klumpbildning (3) rapporterades mindre ofta.%). Dessa händelser inträffade huvudsakligen med startdosen medan under underhållsbehandling vid 80 mg -dosen förekom dessa händelser per 100 injektioner: 3 för smärta och abscess på injektionsstället eller nekros på injektionsstället som kan kräva kirurgisk behandling / dränering.
Tabell över biverkningar
Frekvensen av de biverkningar som anges nedan definieras enligt följande konventioner:
Mycket vanliga (≥ 1/10); vanligt (≥ 1/100 e
Tabell 1: Frekvens av biverkningar rapporterade hos 1259 patienter som behandlats för totalt 1781 patienter under ett år (fas II- och III-studier) och från rapporter efter marknadsföring
* Känd fysiologisk konsekvens av testosteronsuppression
Beskrivning av utvalda biverkningar
Variationer i laboratorieparametrar
Förändringar i laboratorieparametrar som observerades under ett behandlingsår i den bekräftande fas III -studien (N = 409) låg inom samma intervall i både degarelix- och GnRH -agonist (leuprorelin) komparatorgruppen. Markant onormala värden (> 3 * ULN) av levertransaminaser (ALAT, ASAT och GGT) observerades hos 2-6% av patienterna med normala värden i början av behandlingen efter behandling med båda läkemedlen. värden före behandling, markanta minskningar av hematologiska värden, hematokrit (≤0,37) och hemoglobin (≤115 g / l) observerades hos 40% respektive 13-15% efter behandling med båda läkemedlen. Det är inte känt i som mäter denna minskning av hematologiska värden kan hänföras till den underliggande patologin eller är en följd av androgen deprivationsterapi. Markant onormala kaliumvärden
(≥5,8 mmol / L), kreatinin (≥177 μmol / L) och BUN (≥10,7 mmol / L) hos patienter med normala förbehandlingsvärden observerades hos 6%, 2%respektive 15%. av patienter som behandlats med degarelix och in
3%, 2% och 14% av patienterna som behandlats med leuprorelin.
Förändringar i EKG -värden
Förändringar i EKG -mätningar som observerades under ett års behandling i den bekräftande fas III -studien (N = 409) låg inom samma intervall i både degarelix och
behandlas med en GnRH -agonist (leuprorelin) som komparator. Tre patienter (500 ms. Från baslinjen till slutet av studien, genomsnittliga QTcF -förändringar var 12,0 msek i degarelix -gruppen och 16,7 msek i leuprorelin -gruppen.
Bristen på inneboende effekt av degarelix på hjärtrepolarisering (QTcF), hjärtfrekvens, AV -ledning, hjärtdepolarisering eller T- eller U -vågmorfologi bekräftades av en grundlig QT -studie hos friska försökspersoner (N = 80) som fick en "IV -infusion av degarelix under 60 minuter och uppnår en genomsnittlig Cmax på 222 ng / ml, ungefär 3-4 gånger Cmax som erhållits vid behandling av prostatacancer.
Rapportering av misstänkta biverkningar
Det är viktigt att rapportera misstänkta biverkningar efter godkännande av läkemedlet, eftersom det möjliggör kontinuerlig övervakning av nytta / riskbalansen för läkemedlet. Vårdpersonal uppmanas att rapportera alla misstänkta biverkningar via det nationella rapporteringssystemet. "Bilaga V .
04.9 Överdosering
Det finns ingen klinisk erfarenhet av effekterna av akut degarelix -överdosering. Vid överdosering ska patienten övervakas noggrant och vid behov ges stödjande behandling.
05.0 FARMAKOLOGISKA EGENSKAPER
05.1 Farmakodynamiska egenskaper
Farmakoterapeutisk grupp: endokrin terapi, andra hormonantagonister och relaterade ämnen.
ATC -kod: L02BX02.
Handlingsmekanism
Degarelix är en selektiv gonadotropinfrisättande hormon (GnRH) -antagonist som binder konkurrenskraftigt och reversibelt till hypofysen GnRH -receptorer, vilket snabbt reducerar frisättningen av gonadotropiner, luteiniserande hormon (LH) och follikelstimulerande hormon (FSH), vilket resulterar i minskad utsöndring av testosteron (T) av testiklarna. Det är känt att prostatacancer är känslig och reagerar på behandlingar som tar bort källan till androgener. Till skillnad från GnRH -agonister inducerar GnRH -antagonister inte en ökning av LH vilket resulterar i ökad testosteron / tumörstimulering och potentiell symptomatisk blossar upp efter behandlingens början.
En enda dos på 240 mg degarelix, följt av en månatlig underhållsdos på 80 mg, orsakar en snabb minskning av LH- och FSH -koncentrationerna och följaktligen testosteron. Serumkoncentrationerna av dihydrotestosteron (DHT) minskar på samma sätt som för testosteron. Degarelix är effektivt för att uppnå och bibehålla testosteronsuppression långt under medicinska kastrationsnivåer på 0,5 ng / ml. Den månatliga underhållsdosen på 80 mg gör det möjligt att bibehålla testosteronsuppression hos 97% av patienterna i minst ett år. Inga testosterontoppar observerades efter injektioner efter den första under behandling med degarelix. Median testosteronnivåer efter ett års behandling var 0,087 ng / ml (interkvartilintervall 0,06-0,15) N = 167.
Resultat av den bekräftande fas III -studien
Effekten och säkerheten för degarelix utvärderades i en öppen, multicenter, randomiserad, aktiv kontroll, parallell gruppstudie. Studien utvärderade effekten och säkerheten för två månadsvisa degarelix doseringsregimer med en startdos på 240 mg (40 mg / ml) följt med en månatlig subkutan dos på 160 mg (40 mg / ml) eller 80 mg (20 mg / ml), jämfört med en månatlig intramuskulär administrering av 7,5 mg leuprorelin till patienter med prostatacancer som kräver androgenberövningsbehandling. Totalt 620 patienter randomiserades till de tre behandlingsgrupperna, varav 504 (81%) patienter slutförde studien. I gruppen degarelix 240/80 mg avbröt 41 (20%) patienter studien, mot 32 (16%) patienter i leuprorelin -gruppen.
Av de 610 patienter som behandlats:
• 31% hade lokaliserad prostatacancer
• 29% hade lokalt avancerad prostatacancer
• 20% hade metastatisk prostatacancer
• 7% hade okänd metastatisk status
• 13% hade tidigare behandlats med kirurgi eller strålning eller hade ökat PSA.
Den grundläggande demografin är likadan för alla grupper. Medelåldern var 74 år (intervall 47 till 98 år). Det primära målet var att visa effekten av degarelix för att uppnå och bibehålla testosteronsuppression under 0,5 ng / ml under 12 månaders behandling: Den lägsta effektiva underhållsdosen på 80 mg degarelix valdes.
Uppnåendet av serumtestosteron (T) -nivåer ≤0,5 ng / ml
FIRMAGON är effektivt för att uppnå snabb testosteronundertryckning, se tabell 2.
Tabell 2: Andel patienter som uppnådde T≤0,5 ng / ml efter behandlingens början.
Undvik plötsliga ökningar av testosteron
En plötslig ökning definieras som att överskrida baslinjetestosteronnivån på ≥15% under de första två veckorna.
En plötslig ökning av testosteron observerades inte hos någon av de degarelixbehandlade patienterna; det var en genomsnittlig minskning av testosteron med 94% på dag 3. De flesta patienter som behandlades med leuprorelin upplevde förhöjningar av testosteron, med en genomsnittlig ökning av testosteronnivåer med 65% på dag 3. Dessa skillnader var statistiskt signifikanta (p
Studiens primära slutpunkt var graden av testosteronsuppression efter ett års behandling med degarelix eller leuprorelin.Den kliniska nyttan av degarelix jämfört med antiandrogen-associerad leuprorelin vid tidig behandling visades inte.
Återställande av testosteronnivåer
I en studie med patienter med PSA-förhöjning efter lokal behandling (främst radikal prostatektomi och strålbehandling) administrerades FIRMAGON under en sju månaders period följt av en sju månaders övervakningsperiod. Mediantiden för återhämtning av testosteronnivåer (> 0,5 ng / ml, bortom kastrationsnivåer) efter avslutad behandling var 112 dagar (beräknat från början av övervakningsperioden, dvs 28 dagar efter den sista injektionen.). Mediantiden för att nå testosteronnivåer> 1,5 ng / ml (över normalgränsens nedre gräns) var 168 dagar.
Långsiktig effekt
Terapeutisk framgång definierades i studien som att uppnå medicinska kastreringsnivåer på dag 28 och bibehålla testosteronkoncentrationer som inte överstiger 0,5 ng / ml på någon av de 364 behandlingsdagarna.
Tabell 3: Kumulativ sannolikhet för testosteron ≤0,5 ng / ml från dag 28 till dag 364.
* Kaplan Meier uppskattningar för grupper
Uppnåendet av minskning av prostata specifikt antigen (PSA)
Tumörstorleken mättes inte direkt under den kliniska studien men det fanns ett indirekt positivt tumörsvar som kunde påvisas som 95% median PSA -minskning med degarelix efter 12 månader.
Median PSA -värdena i basstudien var:
• 19,8 ng / ml (interkvartilintervall: P25 9,4 ng / ml, P75 46,4 ng / ml) i gruppen degarelix 240/80 mg
• 17,4 ng / ml (interkvartilintervall: P25 8,4 ng / ml, P75 56,5 ng / ml) i 7,5 mg leuprorelin -gruppen.
Skillnaderna är statistiskt signifikanta (s
Prostataspecifika antigen (PSA) -nivåer reducerades med 64% efter två veckors administrering av degarelix, med 85% efter en månad och med 95% efter tre månader, förblev undertryckta (cirka 97%) under en behandlingsperiod. Ett år.
Från dag 56 till dag 364 fanns det inga signifikanta skillnader i förändringstakten från baslinjen mellan degarelix och jämföraren.
Effekter på prostatavolymen
Tre månaders degarelix-behandling (240/80 mg dosbehandling) resulterade i en minskning av prostatavolymen med 37% mätt med trans-rektal ultraljud hos patienter som behövde hormonbehandling före strålbehandling och hos patienter som var kandidater för medicinsk kastration. Minskningen i prostatavolymen liknade den som uppnåddes med goserelin plus anti-androgen skydd.
Effekter på QT / QTc -intervall
Kontrollelektrokardiogram utfördes regelbundet i den bekräftande studien där FIRMAGON jämfördes med leuprorelin. Med båda terapierna observerades ett QT / QTc -intervall större än 450 msek hos cirka 20% av patienterna. Från baslinjen till studiens slut var medianförändringar uppmätta med FIRMAGON 12,0 msek och med leuprorelin 16,7 msek.
Anti-degarelix antikroppar
Utvecklingen av anti-degarelix-antikroppar observerades hos 10% av patienterna efter ett års behandling med FIRMAGON och hos 29% av patienterna efter behandling med FIRMAGON i upp till 5,5 år. Det finns inga indikationer på att bildandet av dessa antikroppar påverkar effekten och säkerheten för FIRMAGON upp till 5,5 års behandling.
Pediatrisk population
Europeiska läkemedelsmyndigheten har befriat FIRMAGON från sin skyldighet att lämna in studieresultat för alla undergrupper av den pediatriska populationen (se avsnitt 4.2 för information om pediatrisk användning).
05.2 Farmakokinetiska egenskaper
Absorption
Efter subkutan administrering av 240 mg degarelix i en koncentration av 40 mg / ml till patienter med prostatacancer i den centrala studien CS21 var AUC0-28 dagar 635 (602-668) dag * ng / ml, Cmax var 66,0 (61,0- 71,0) ng / ml och nåddes vid Tmax 40 (37-42) timmar. Medelvärden var cirka 11-12 ng / ml efter startdos och 11-16 ng / ml efter underhållsdosen på 80 mg vid koncentrationer av 20 mg / ml. Efter Cmax minskar plasmakoncentrationen av degarelix bifasiskt med en genomsnittlig slutlig halveringstid (t½) på 29 dagar med underhållsdosen. För subkutan administrering är en följd av en mycket långsam frigöring av degarelix från deponeringen som bildas vid injektionsstället. Läkemedlets farmakokinetiska beteende påverkas av dess koncentration i injektionslösningen. Därför tenderar Cmax och biotillgänglighet att minska med ökad doskoncentration medan halveringstiden tenderar att d öka. Därför ska inga andra styrkor än de rekommenderade användas.
Distribution
Distributionsvolymen hos friska äldre män är cirka 1 l / kg. Plasmaproteinbindning uppskattas till cirka 90%.
Biotransformation
Degarelix genomgår vanlig peptidnedbrytning under passage genom lever-gallsystemet och utsöndras huvudsakligen som peptidfragment i avföringen. Inga signifikanta metaboliter detekterades i plasmaprover efter subkutan administrering. Utbildning in vitro visat att degarelix inte är ett substrat för det mänskliga CYP450 -systemet.
Eliminering
Hos friska män utsöndras cirka 20-30% av en enda intravenös dos i urinen, vilket tyder på att 70-80% utsöndras via lever-gallvägarna. Clearance av degarelix som en enda intravenös dos (0,864-49,4 mcg / kg) hos friska äldre män var 35-50 ml / h / kg.
Särskilda populationer:
Patienter med nedsatt njurfunktion
Farmakokinetiska studier har inte utförts på patienter med nedsatt njurfunktion. Endast cirka 20-30% av den administrerade dosen degarelix utsöndras oförändrat av njurarna. En populationsfarmakokinetisk analys av fas III -konfirmeringsstudien visade att clearance av degarelix hos patienter med lätt eller måttligt nedsatt njurfunktion reduceras med cirka 23%; därför rekommenderas ingen dosjustering för sådana patienter.Data om patienter med allvarligt nedsatt njurfunktion är knappa. och därför rekommenderas försiktighet hos dessa patienter.
Patienter med nedsatt leverfunktion
Degarelix utvärderades i en farmakokinetisk studie på patienter med lätt till måttligt nedsatt leverfunktion. Inga tecken på överexponering observerades hos patienter med nedsatt leverfunktion jämfört med friska försökspersoner. Inga dosjusteringar krävs hos patienter med mild till måttlig nedsatt leverfunktion. Patienter med svår leversvikt har inte studerats, därför rekommenderas försiktighet i denna grupp.
05.3 Prekliniska säkerhetsdata
Djurreproduktionsstudier har visat att degarelix orsakar infertilitet hos hanar. Detta beror på den farmakologiska effekten som är reversibel.
I studier av reproduktionstoxicitet hos kvinnor gav degarelix förväntade resultat på grund av dess farmakologiska egenskaper. Det orsakar en dosberoende förlängning av parningstiden och graviditeten, ett litet antal corpora lutea, och en ökning av förluster före och efter implantation, aborter, tidiga embryo- / fosterdöd, för tidiga födslar och leveranslängd.
Prekliniska farmakologiska säkerhetsstudier, studier av upprepad toxicitet, genotoxicitet och cancerframkallande potential visade inga särskilda risker för den mänskliga arten. I synnerhet båda studierna in vitro den där in vivo visade ingen QT -förlängning.
Ingen organspecifik toxicitet observerades i akuta, subakuta eller kroniska studier på råttor och apor efter subkutan administrering av degarelix. Läkemedelsrelaterad lokal irritation noterades när degarelix administrerades subkutant vid höga doser till djur.
06.0 LÄKEMEDELSINFORMATION
06.1 Hjälpämnen
Damm
Mannitol (E421)
Lösningsmedel
Vatten för injektionsvätskor
06.2 Oförenlighet
I avsaknad av kompatibilitetsstudier, blanda inte denna produkt med andra läkemedel.
06.3 Giltighetstid
3 år.
Efter rekonstituering
Kemisk-fysikalisk stabilitet har visats vid användning i 2 timmar vid 25 ° C. Ur mikrobiologisk synvinkel, om inte rekonstitutionsmetoden utesluter risken för bakteriell kontaminering, ska produkten användas omedelbart. Om den inte används. tid och användningsvillkor är användarens ansvar.
06.4 Särskilda förvaringsanvisningar
Inga särskilda försiktighetsåtgärder.
För förvaringsförhållanden för den färdigberedda produkten, se avsnitt 6.3.
06.5 Förpackningens innehåll och förpackningens innehåll
Injektionsflaska av glas (typ I) med brombutylgummipropp och aluminiumförslutningstätning innehållande 80 mg pulver till injektionsvätska, lösning
Förfylld glasspruta (typ I) med elastomerkolv, lock och 4 ml märkningslinje innehållande 4,2 ml lösningsmedel
Kolv
Adapter på flaska
Injektionsnål (25G 0,5 x 25mm)
Förpackning FIRMAGON finns i två paket:
Förpackning med 1 bricka innehållande: 1 injektionsflaska med pulver, 1 förfylld spruta med lösningsmedel, 1 kolv, 1 flaskaadapter och 1 nål.
Förpackning med 3 brickor innehållande: 3 injektionsflaskor med pulver, 3 förfyllda sprutor med lösningsmedel, 3 kolvar, 3 ampuller och 3 nålar.
Alla förpackningsstorlekar kanske inte finns på marknaden.
06.6 Anvisningar för användning och hantering
Följ instruktionerna för beredning noggrant.
Administrering av olika koncentrationer rekommenderas inte eftersom bildandet av gelavlagringar påverkas av koncentrationen. Den beredda lösningen ska vara en klar vätska, fri från oupplösta partiklar.
NOTERA:
• SKAKA INTE HALKORNA
Förpackningen innehåller en injektionsflaska med pulver och en förfylld spruta med lösningsmedel som ska beredas för subkutan injektion.
1. Ta bort locket från förpackningen på flaskans adapter. Fäst adaptern på pulverflaskan genom att trycka ned den tills spetsen passerar genom gummiproppen och adaptern klickar på plats.
2. Förbered den förfyllda sprutan genom att sätta i kolven
3. Ta bort det förfyllda sprutlocket. Fäst sprutan på injektionsflaskan med pulver genom att skruva fast den på adaptern. Överför allt lösningsmedel till pulverflaskan.
4. Håll sprutan insatt i adaptern, virvla försiktigt tills vätskan är klar och fri från olösta partiklar eller pulver. Om pulvret fäster vid injektionsflaskan ovanför vätskans yta kan flaskan lutas något. Undvik skakningar för att förhindra att skummande.
Bildandet av en ring med små luftbubblor på vätskans yta är acceptabelt, rekonstitueringsförfarandet tar vanligtvis några minuter men i vissa fall kan det ta upp till 15 minuter.
5. Vänd injektionsflaskan upp och ner och dra upp till injektionssprutans markeringslinje.
Se alltid till att aspirera den exakta volymen och justera för eventuella luftbubblor.
6. Lossa sprutan från adaptern och sätt in nålen för djup subkutan injektion i sprutan.
7. Ge en djup subkutan injektion. För att göra detta: ta tag i buken, lyft den subkutana vävnaden och sätt in nålen djupt i en vinkel på inte mindre än 45 grader.
Injicera långsamt 4 ml FIRMAGON 80 mg omedelbart efter beredning.
Injektioner ska inte ges i områden där patienten kan utsättas för tryck, till exempel i bältesområdet, där det finns band eller nära revbenen.
Injicera inte direkt i en ven. Dra försiktigt tillbaka sprutkolven för att kontrollera om blod har sugits upp. Om det finns blod i sprutan får medicinen inte längre användas, stoppa proceduren och kasta sprutan och nålen (rekonstituera en ny dos för patienten).
Inga särskilda bestämmelser krävs för eliminering.
07.0 INNEHAVARE AV GODKÄNNANDE FÖR FÖRSÄLJNING
Ferring Pharmaceuticals A / S
Kay Fiskers Plads 11
DK-2300 Köpenhamn S
Danmark
08.0 NUMMER FÖR FÖRSÄLJNINGSTILLSTÅND
EU/1/08/504/001
039232018
EU/1/08/504/003
09.0 DATUM FÖR FÖRSTA GODKÄNNANDE ELLER FÖRNYELSE AV GODKÄNNANDET
Datum för första godkännandet: 17/02/2009
Datum för den senaste förnyelsen: 19/09/2013
10.0 DATUM FÖR REVISION AV TEXTEN
D.CCE november 2014