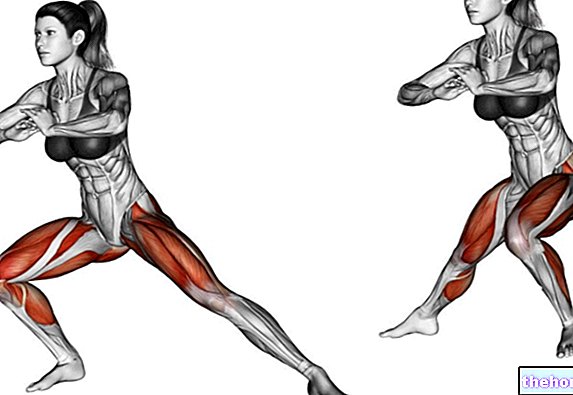
Aktiva ingredienser: Ezetimibe, Simvastatin
INEGY 10 mg / 10 mg
INEGY 10 mg / 20 mg
INEGY 10 mg / 40 mg
INEGY 10 mg / 80 mg tabletter
Indikationer Varför används Inegy? Vad är det för?
INEGY innehåller de aktiva substanserna ezetemibe och simvastatin. INEGY är ett läkemedel som används för att minska nivåerna av totalt kolesterol, "dåligt" kolesterol (LDL -kolesterol) och fettsubstanser som kallas triglycerider i blodet. Dessutom ökar INEGY nivåerna av "bra" kolesterol (HDL -kolesterol).
INEGY fungerar på två sätt för att sänka kolesterolet. Den aktiva substansen ezetimibe minskar kolesterolet som absorberas i matsmältningskanalen. Den aktiva ingrediensen simvastatin som tillhör klassen "statiner" hämmar produktionen av kolesterol som syntetiseras av kroppen.
Kolesterol är en av flera fettämnen som finns i blodomloppet. Totalt kolesterol består huvudsakligen av LDL -kolesterol och HDL -kolesterol.
LDL -kolesterol kallas ofta "dåligt" kolesterol eftersom det kan byggas upp i artärväggarna och bilda plack. Med tiden kan denna plackuppbyggnad leda till förträngning av artärerna. Denna förträngning kan bromsa eller blockera blodflödet till vitala organ som hjärta och hjärna. Denna blockering av blodflödet kan orsaka hjärtinfarkt eller stroke.
HDL -kolesterol kallas ofta "bra" kolesterol eftersom det hjälper till att förhindra att dåligt kolesterol byggs upp i artärerna och skyddar mot hjärtsjukdomar.
Triglycerider är en annan form av fett i blodet som kan öka risken för hjärtsjukdomar.
INEGY används för patienter som inte kan kontrollera sina kolesterolnivåer med enbart kost. När du tar detta läkemedel bör du fortfarande följa en kolesterolsänkande diet
. INEGY används som tillägg till kosten för att sänka kolesterolet om du har:
- förhöjda kolesterolnivåer i blodet (primär hyperkolesterolemi) [familjär och icke-familjär heterozygot] eller förhöjda blodfettnivåer (blandad hyperlipidemi):
- som inte kontrolleras väl av en statin ensam;
- för vilken du har tagit behandling med statin och ezetimibe som separata tabletter;
- en ärftlig sjukdom (homozygot familjär hyperkolesterolemi) som ökar kolesterolhalten i blodet. Det är möjligt att du också behandlas med andra behandlingar.
INEGY hjälper dig inte att gå ner i vikt.
Kontraindikationer När Inegy inte ska användas
Ta inte INEGY om:
- du är allergisk (överkänslig) mot "ezetimibe, simvastatin eller något annat innehållsämne i detta läkemedel (anges i avsnitt 6: Förpackningens innehåll och annan information)
- har för närvarande leverproblem
- du är gravid eller ammar
- du tar medicin med en eller flera av följande aktiva substanser:
- itrakonazol, ketokonazol, posakonazol eller vorikonazol (används för att behandla svampinfektioner)
-erytromycin, klaritromycin eller telitromycin (används för att behandla infektioner)
- HIV -proteashämmare såsom indinavir, nelfinavir, ritonavir och saquinavir (HIV -proteashämmare används för att behandla HIV -infektioner)
- boceprevir eller telaprevir (används för att behandla hepatit C -virusinfektioner)
nefazodon (används för att behandla depression)
- kobicistat
- gemfibrozil (används för att sänka kolesterolet)
- ciklosporin (används ofta hos organtransplanterade patienter)
- danazol (ett mänskligt hormon som används för att behandla endometrios, ett tillstånd där livmoderslemhinnan växer utanför livmodern).
- du tar eller under de senaste sju dagarna har tagit eller har fått ett läkemedel som kallas fusidinsyra (används för att behandla bakteriell infektion).
Ta inte mer än 10 mg / 40 mg INEGY om du tar lomitapid (används för att behandla ett allvarligt och sällsynt genetiskt kolesteroltillstånd)
Fråga din läkare om du är osäker på om medicinen du använder är en av de som anges ovan.
Försiktighetsåtgärder vid användning Vad du behöver veta innan du tar Inegy
Tala om för din läkare:
- av alla dina medicinska tillstånd, inklusive allergier.
- om du dricker stora mängder alkohol eller om du någonsin har haft leversjukdom. I det här fallet kanske INEGY inte passar dig.
- om du ska opereras. Du kan behöva sluta ta INEGY under en kort tid.
- om du är asiatisk, eftersom en annan dos kan vara lämplig för dig.
Din läkare måste göra ett blodprov innan du tar INEGY och om du har symtom på leverproblem medan du tar INEGY. Denna analys görs för att veta om levern fungerar korrekt.
Din läkare kan också beställa blodprov för att kontrollera leverfunktionen efter att du har startat INEGY -behandling.
Medan du behandlas med detta läkemedel kommer din läkare noggrant att kontrollera att du inte har diabetes eller att du inte riskerar att utveckla diabetes. Du riskerar att utveckla diabetes om du har högt blodsocker och fett, om du är överviktig och har högt blodtryck.
Tala om för din läkare om du har allvarlig lungsjukdom.
Administrering av INEGY med fibrater (vissa typer av kolesterolsänkande läkemedel) bör undvikas eftersom användning av INEGY med fibrater inte har studerats.
Kontakta din läkare omedelbart om du har muskelsmärta, muskelsårighet och muskelsvaghet av obestämda orsaker, eftersom muskelproblem sällan kan vara allvarliga och leda till att muskelvävnadsskada orsakar njurskador och mycket sällan dödsfall har inträffat.
Risken för muskelskada är större vid högre doser INEGY, särskilt med 10 mg / 80 mg dosen. Risken för muskelskada är också större hos vissa patienter. Tala om för din läkare om något av följande gäller dig:
- har njurproblem
- har sköldkörtelproblem
- är 65 år eller äldre
- är kvinna
- har någonsin haft muskelproblem medan du tog kolesterolsänkande läkemedel som kallas "statiner" (t.ex. simvastatin, atorvastatin och rosuvastatin) eller fibrater (t.ex. gemfibrozil och bezafibrat)
- du eller din närmaste familj har en ärftlig muskelsjukdom.
Tala också om för din läkare eller apotekspersonal om du har konstant muskelsvaghet. Ytterligare tester och läkemedel kan behövas för att diagnostisera och behandla detta tillstånd.
Barn och ungdomar
Användning av INEGY rekommenderas inte till barn under 10 år.
Interaktioner Vilka droger eller livsmedel kan förändra effekten av Inegy
Tala om för din läkare om du tar, nyligen har tagit eller kanske tar andra läkemedel med något av följande aktiva ämnen. Att ta INEGY med något av följande läkemedel kan öka risken för muskelproblem (några har redan nämnts ovan i avsnittet "Ta inte INEGY om"):
- cyklosporin (används ofta hos patienter som får organtransplantation)
- danazol (ett konstgjord hormon som används för att behandla endometrios, ett tillstånd där livmoderslemhinnan växer utanför livmodern)
- läkemedel med en aktiv substans som itrakonazol, ketokonazol, flukonazol, posakonazol eller vorikonazol (används för att behandla svampinfektioner)
- fibrerar med aktiva ingredienser som gemfibrozil och bezafibrat (används för att sänka kolesterolet)
- erytromycin, klaritromycin, telitromycin eller fusidinsyra (används för att behandla bakteriella infektioner). Ta inte fusidinsyra medan du använder detta läkemedel. Se även punkt 4 i denna bipacksedel.
- HIV -proteashämmare såsom indinavir, nelfinavir, ritonavir och saquinavir (används för att behandla AIDS)
- boceprevir eller telaprevir (används för att behandla hepatit C -virusinfektioner)
- nefazodon (används för att behandla depression)
- läkemedel med den aktiva substansen kobicistat
- amiodaron (används för att behandla oregelbunden hjärtslag)
- verapamil, diltiazem eller amlodipin (används för att behandla högt blodtryck, bröstsmärta i samband med hjärtsjukdom eller annan hjärtsjukdom)
- lomitapid (används för att behandla ett allvarligt och sällsynt genetiskt kolesteroltillstånd
- höga doser (1 g eller mer per dag) av niacin eller nikotinsyra (används också för att sänka kolesterolet)
- kolkicin (används för att behandla gikt).
Utöver de ovan nämnda läkemedlen, berätta för din läkare eller apotekspersonal om du tar eller nyligen har tagit andra läkemedel, även receptfria sådana. Tala särskilt om för din läkare om du tar något av följande:
- läkemedel med en aktiv ingrediens för att förhindra blodproppar, såsom warfarin, fluindion, fenprocoumon eller acenocoumarol (antikoagulantia)
- kolestyramin (används också för att sänka kolesterolet) eftersom det påverkar hur INEGY fungerar
- fenofibrat (används också för att sänka kolesterolet)
- rifampicin (används för att behandla tuberkulos).
Du bör också berätta för alla läkare som förskriver ett nytt läkemedel att du tar INEGY.
INEGY med mat och dryck
Grapefruktjuice innehåller ett eller flera ämnen som förändrar metabolismen av vissa läkemedel, inklusive INEGY. Konsumtion av grapefruktjuice bör undvikas eftersom det kan öka risken för muskelproblem.
Varningar Det är viktigt att veta att:
Graviditet och amning
Använd inte INEGY om du är gravid, tänker bli gravid eller misstänker graviditet. Om du blir gravid när du tar INEGY, sluta ta det omedelbart och kontakta din läkare. INEGY ska inte användas under amning eftersom det inte är känt om läkemedlet passerar i bröstmjölk.
Fråga din läkare eller apotekspersonal om råd innan du tar något läkemedel.
Köra och använda maskiner
INEGY förväntas inte störa din förmåga att köra bil eller använda maskiner. Det bör dock komma ihåg att vissa människor har känt sig yr efter att ha tagit INEGY.
INEGY innehåller laktos
INEGY tabletter innehåller socker, laktos. Om din läkare har fått veta att du har "intolerans mot vissa sockerarter, kontakta din läkare innan du tar detta läkemedel.
Dosering och användningssätt Hur man använder Inegy: Dosering
Din läkare kommer att avgöra vilken tablettstyrka som är lämplig för dig, baserat på din nuvarande behandling och din riskprofil.
Tabletterna är inte trasiga och ska inte delas.
Ta alltid detta läkemedel enligt läkarens eller apotekspersonalens anvisningar. Kontakta din läkare eller apotekspersonal om du är osäker
- Innan du börjar ta INEGY måste du redan ha följt en diet för att sänka kolesterolnivåerna.
- Under behandling med INEGY bör du fortsätta att följa denna diet för att sänka ditt kolesterol.
Vuxna: dosen är 1 INEGY tablett oralt en gång om dagen.
Användning för ungdomar (10 till 17 år): Dosen är 1 tablett INEGY oralt en gång om dagen (en maximal dos på 10 mg / 40 mg en gång om dagen bör inte överskridas). INEGY -dosen på 10 mg / 80 mg rekommenderas endast till vuxna patienter med mycket höga kolesterolnivåer och hög risk för hjärtsjukdomar som inte har nått sin ideala kolesterolnivå med de lägsta doserna.
Ta INEGY på kvällen. Du kan ta den med eller utan mat.
Om din läkare har ordinerat INEGY med ett annat kolesterolsänkande läkemedel som innehåller den aktiva substansen kolestyramin eller något annat gallsyrasekvestreringsmedel, ska du ta INEGY minst 2 timmar före eller 4 timmar efter att du har tagit gallsyrabindande medel.
Överdosering Vad du ska göra om du har tagit för mycket Inegy
Om du har tagit mer INEGY än du borde:
- kontakta din läkare eller apotekspersonal.
Om du har glömt att ta INEGY:
- ta inte en dubbel dos för att kompensera för en glömd tablett, ta bara din normala dos INEGY nästa dag vid vanlig tid.
Om du slutar att ta INEGY:
- tala med din läkare eller apotekspersonal eftersom ditt kolesterol kan stiga igen.
Fråga din läkare eller apotekspersonal om du har ytterligare frågor om användningen av detta läkemedel.
Biverkningar Vilka är biverkningarna av Inegy
Liksom alla läkemedel kan INEGY orsaka biverkningar, men inte alla får dem (se avsnitt Vad du behöver veta innan du tar INEGY).
Följande vanliga biverkningar har rapporterats (kan förekomma hos upp till 1 av 10 personer):
- muskelvärk
- ökningar i blodlaboratorietestvärden för lever (transaminas) och / eller muskelfunktion (CK)
Följande ovanliga biverkningar har rapporterats (kan förekomma hos upp till 1 av 100 personer):
- ökning av blodprovsvärden relaterade till leverfunktion; ökning av urinsyravärdena i blodet, ökad tid det tar för blod att koagulera, närvaro av protein i urinen, minskad kroppsvikt
- yrsel huvudvärk; kittlande känsla
- buksmärtor; dålig matsmältning; flatulens; illamående; Han retched; uppblåsthet i buken; diarre; torr mun; magont
- utslag; klia; urtikaria
- ledvärk; muskelsmärta; känslighet; svaghet eller spasmer; nacksmärta; smärta i armar eller ben; ryggont
- ovanlig trötthet eller svaghet känner mig trött; bröstsmärta; svullnad, särskilt i händer och fötter
- sömnstörning; svårt att somna
Dessutom har följande biverkningar rapporterats hos personer som tar INEGY eller läkemedel som innehåller de aktiva substanserna ezetimibe eller simvastatin:
- lågt antal röda blodkroppar (anemi); minskat antal blodceller, vilket kan orsaka blåmärken / blödningar (trombocytopeni)
- förlust av känsla eller svaghet i armar och ben; dåligt minne; minnesförlust; förvirring
- andningsproblem, inklusive ihållande hosta och / eller andnöd eller feber
- förstoppning
- inflammation i bukspottkörteln ofta med svår buksmärta
- leverinflammation med följande symtom: gulning av hud och ögon; klia; mörkfärgad urin eller ljusfärgad avföring; känner sig trött eller svag; aptitlöshet; leversvikt; gallblåsstenar eller inflammation i gallblåsan (som kan orsaka buksmärtor, illamående och kräkningar)
- håravfall; förhöjda röda utslag, ibland med målformade lesioner (erythema multiforme)
- en överkänslighetsreaktion som har inkluderat några av följande egenskaper: överkänslighet (allergiska reaktioner inklusive svullnad i ansikte, läppar, tunga och / eller svalg som kan orsaka andningssvårigheter eller sväljningar och kräver omedelbar behandling, smärta eller inflammation i lederna, inflammation i blodet kärl, onormala blåmärken, utslag och svullnad, nässelfeber, hudkänslighet för solen, feber, rodnad, andfåddhet och illamående, lupusliknande symptom (som inkluderar utslag, hudproblem) leder och effekter på vita blodkroppar).
- muskelsmärta; känslighet; muskelsvaghet eller kramper; muskelskador; senproblem, ibland komplicerade av senbrott.
- minskad aptit
- värmevallningar; högt blodtryck
- värk
- erektil dysfunktion
- depression
- förändringar i vissa blodprovsvärden relaterade till leverfunktion
Ytterligare möjliga biverkningar rapporterade med vissa statiner:
- sömnstörningar, inklusive mardrömmar
- sexuella svårigheter
- diabetes. Det är mer troligt om du har högt blodsocker och fett, är överviktig och har högt blodtryck.Din läkare kommer att övervaka dig under behandling med detta läkemedel.
- muskelsmärta, ömhet eller svaghet som är konstant som kanske inte försvinner efter att INEGY har stoppats (frekvensen är inte känd).
Kontakta din läkare omedelbart om du har muskelsmärta, muskelsårighet och muskelsvaghet av obestämda orsaker, eftersom muskelproblem sällan kan vara allvarliga och leda till att muskelvävnadsskada orsakar njurskador och mycket sällan dödsfall har inträffat.
Rapportering av biverkningar
Tala med din läkare eller apotekspersonal om du får några biverkningar. Detta inkluderar eventuella biverkningar som inte nämns i denna bipacksedel. Du kan också rapportera biverkningar direkt via det nationella rapporteringssystemet på: https://www.aifa.gov.it/content/segnalazioni-reazioni-avverse
Giltighetstid och lagring
- Förvara detta läkemedel utom syn- och räckhåll för barn.
- Använd inte detta läkemedel efter utgångsdatum som anges på förpackningen efter "EXP".
- Förvara INEGY -tabletter vid temperaturer över 30 ° C.
Blister: Förvaras i originalförpackningen för att skydda läkemedlet från ljus och fukt.
Flaskor: Håll flaskorna väl tillslutna för att skydda läkemedlet från ljus och fukt.
Kasta inga läkemedel i avloppsvatten eller hushållsavfall. Fråga din apotekare om hur du ska kasta läkemedel som du inte längre använder. Detta hjälper till att skydda miljön.
Vad gör INEGY
De aktiva substanserna i INEGY är ezetimibe och simvastatin. Varje tablett innehåller 10 mg ezetimibe och 10 mg, 20 mg, 40 mg eller 80 mg simvastatin.
Övriga innehållsämnen är: butylerad hydroxianisol, citronsyramonohydrat, kroskarmellosnatrium, hypromellos, laktosmonohydrat, magnesiumstearat, mikrokristallin cellulosa, propylgallat.
Beskrivning av hur INEGY ser ut och förpackningens innehåll
INEGY finns som vita till benvita kapselformade tabletter med koden "311", "312", "313" eller "315" på ena sidan. Tabletterna är inte trasiga och ska inte delas.
INEGY finns i förpackningar med 7, 10, 14, 28, 30, 50, 56, 84, 90, 98, flerförpackningar innehållande 98 (2 förpackningar med 49), 100 eller 300 tabletter.
Alla förpackningsstorlekar kanske inte marknadsförs.
Bipacksedel: AIFA (Italian Medicines Agency). Innehåll publicerat i januari 2016. Den information som finns finns kanske inte uppdaterad.
För att få tillgång till den senaste versionen är det lämpligt att gå till AIFA (Italian Medicines Agency) webbplats. Ansvarsfriskrivning och användbar information.
01.0 LÄKEMEDLETS NAMN
INEGY 10 MG / 10 MG, 10 MG / 20 MG, 10 MG / 40 MG, 10 MG / 80 MG TABLETTER
02.0 KVALITATIV OCH KVANTITATIV SAMMANSÄTTNING
Varje tablett innehåller 10 mg ezetimibe och 10, 20, 40 eller 80 mg simvastatin.
Hjälpämne med känd effekt:
Varje 10 mg / 10 mg tablett innehåller 58,2 mg laktosmonohydrat.
Varje 10 mg / 20 mg tablett innehåller 126,5 mg laktosmonohydrat.
Varje 10 mg / 40 mg tablett innehåller 262,9 mg laktosmonohydrat.
Varje 10 mg / 80 mg tablett innehåller 535,8 mg laktosmonohydrat.
För fullständig förteckning över hjälpämnen, se avsnitt 6.1.
03.0 LÄKEMEDELSFORM
Läsplatta.
Vita till benvita kapselformade tabletter med koden "311", "312", "313" eller "315" på ena sidan.
04.0 KLINISK INFORMATION
04.1 Terapeutiska indikationer
Hyperkolesterolemi
INEGY indikeras som tillägg till kost hos patienter med primär hyperkolesterolemi (familjär och icke-familjär heterozygot) eller med blandad hyperlipidemi där användning av en kombinationsprodukt indikeras:
• patienter som inte är tillräckligt kontrollerade på enbart statin;
• patienter som redan behandlats med statin och ezetimibe.
INEGY innehåller ezetimibe och simvastatin. Simvastatin (20-40 mg) har visat sig minska frekvensen av kardiovaskulära händelser (se avsnitt 5.1). En fördelaktig effekt av ezetimib på kardiovaskulär morbiditet och dödlighet har ännu inte påvisats.
Homozygot familjär hyperkolesterolemi (homozygot IF)
INEGY indikeras som tillägg till kost hos patienter med homozygot familjär hyperkolesterolemi. Patienter kan också genomgå ytterligare terapeutiska åtgärder (till exempel lågdensitetslipoprotein [LDL] -aferes).
04.2 Dosering och administreringssätt
Dosering
Hyperkolesterolemi
Patienten bör följa en adekvat fettsnål diet och fortsätta kosten under behandling med INEGY.
Läkemedlet ska administreras oralt. Dosintervallet för INEGY är 10 mg / 10 mg / dag till 10 mg / 80 mg / dag på kvällen. Doser är kanske inte alla tillgängliga i alla medlemsstater. Vanlig dos är 10 mg / 20 mg / dag. O 10 mg / 40 mg / dag administreras på kvällen som en enda dos. Dosen på 10 mg / 80 mg rekommenderas endast till patienter med svår hyperkolesterolemi och med hög risk för kardiovaskulära komplikationer som inte har uppnått terapeutiska mål med lägre doser och när fördelarna förväntas uppväga de potentiella riskerna (se avsnitt 4.4 och 5.1).
Lågdensitetslipoproteinkolesterol (LDL-C), risken för kranskärlssjukdom och patientens svar på aktuell kolesterolsänkande behandling bör övervägas i början av behandlingen eller när dosen ändras.
Dosen INEGY bör individualiseras baserat på den erkända effekten av de olika INEGY-styrkorna (se avsnitt 5.1, tabell 1) och svaret på pågående kolesterolsänkande behandling. Dosjusteringar, om det behövs, bör göras med intervall. Inte mindre. än 4 veckor INEGY kan administreras med eller utan måltider Tabletten ska inte delas.
Homozygot familjär hyperkolesterolemi
Den rekommenderade startdosen för patienter med homozygot familjär hyperkolesterolemi är INEGY 10 mg / 40 mg / dag på kvällen. Dosen 10 mg / 80 mg rekommenderas endast när fördelarna förväntas överväga de potentiella riskerna (se ovan; avsnitt 4.3 och 4.4). INEGY kan användas hos dessa patienter som ett adjuvans till andra lipidsänkande behandlingar (t.ex. LDL-aferes) eller om sådana behandlingar inte är tillgängliga.
Hos patienter som tar lomitapid samtidigt med INEGY ska INEGY -dosen inte överstiga 10 mg / 40 mg / dag (se avsnitt 4.3, 4.4 och 4.5).
Samtidig administrering med andra läkemedel
Administrering av INEGY måste ske antingen ≥2 timmar före eller ≥4 timmar efter administrering av ett gallsyrabindande medel.
Hos patienter som tar amiodaron, amlodipin, verapamil eller diltiazem samtidigt med INEGY ska INEGY -dosen inte överstiga 10 mg / 20 mg / dag (se avsnitt 4.4 och 4.5).
Hos patienter som får lipidsänkande doser av niacin (≥1 g / dag) samtidigt med INEGY, ska INEGY-dosen inte överstiga 10 mg / 20 mg / dag (se avsnitt 4.4 och 4.5).
Pensionärer
Ingen dosjustering krävs hos äldre patienter (se avsnitt 5.2).
Pediatrisk population
Behandlingsstart måste utföras under överinseende av en specialist.
Ungdomar ≥10 år (pubertetsstatus: pojkar i Tanner steg II och högre och flickor som har varit postmenarche i minst ett år): Klinisk erfarenhet av barn och ungdomar (10 till 17 år) är begränsad. Vanlig rekommenderad start dosen är 10 mg / 10 mg en gång dagligen på kvällen Det rekommenderade dosintervallet är 10 mg / 10 mg upp till maximalt 10 mg / 40 mg / dag (se avsnitt 4.4 och 5.2).
Barn
Patienter med nedsatt leverfunktion
Ingen dosjustering krävs hos patienter med lätt nedsatt leverfunktion (Child-Pugh poäng 5 till 6). Behandling med INEGY rekommenderas inte till patienter med måttlig (Child-Pugh poäng 7 till 9) eller svår (Child-Pugh poäng> 9) nedsatt leverfunktion. (Se avsnitt 4.4 och 5.2).
Patienter med njurskada
Ingen dosjustering krävs hos patienter med lätt nedsatt njurfunktion (uppskattad glomerulär filtrationshastighet ≥60 ml / min / 1,73 m2). Hos patienter med kronisk njursjukdom och uppskattad glomerulär filtrationshastighet 2 är den rekommenderade dosen INEGY 10 mg / 20 mg en gång dagligen på kvällen (se avsnitt 4.4, 5.1 och 5.2). Högre doser ska administreras med försiktighet.
Administreringssätt
Inegy ska administreras oralt. Inegy kan ges som en enda dos på kvällen.
04.3 Kontraindikationer
Överkänslighet mot den eller de aktiva substanserna eller mot något hjälpämne som anges i avsnitt 6.1.
Graviditet och amning (se avsnitt 4.6).
Aktiv leversjukdom eller förhöjda, ihållande och obestämda värden på serumtransaminaser.
Samtidig administrering av potenta CYP3A4-hämmare (medel som ökar AUC cirka fem gånger eller mer) (t.ex. itrakonazol, ketokonazol, posakonazol, vorikonazol, erytromycin, klaritromycin, telitromycin, HIV-proteashämmare (t.ex. nelfinavir), boceprevir, telaprevir, nefazod produkter som innehåller kobicistat) (se avsnitt 4.4 och 4.5).
Samtidig administrering av gemfibrozil, cyklosporin eller danazol (se avsnitt 4.4 och 4.5).
Hos patienter med homozygot IF, samtidig administrering av lomitapid med doser av INEGY 10 mg / 40 mg (se avsnitt 4.2, 4.4 och 4.5).
04.4 Särskilda varningar och lämpliga försiktighetsåtgärder vid användning
Myopati / rabdomyolys
Fall av myopati och rabdomyolys har rapporterats efter marknadsföring med ezetimib.De flesta patienter som utvecklat rabdomyolys behandlades samtidigt med ezetimib och ett statin, men rabdomyolys har rapporterats mycket sällan med ezetimib och monoterapi. Mycket sällan med tillägg av ezetimibe till andra läkemedel som är kända för att vara förknippade med en ökad risk för rabdomyolys.
INEGY innehåller simvastatin. Simvastatin, liksom andra HMG-CoA-reduktashämmare, orsakar ibland myopati, som uppträder som muskelsmärta, ömhet eller svaghet i samband med förhöjningar i kreatinkinas (CK) nivåer över 10 gånger den övre gränsen för det normala. Myopati manifesteras ibland som rabdomyolys med eller utan akut njursvikt sekundärt till myoglobinuri och mycket sällan dödliga utfall har inträffat Risken för myopati ökar med höga nivåer av HMG-CoA-reduktashämmande aktivitet i plasma.
Precis som med andra HMG-CoA-reduktashämmare är risken för myopati / rabdomyolys dosrelaterad till simvastatin.I en klinisk prövningsdatabas där 41 413 patienter behandlades med simvastatin varav 24 747 (cirka 60%) inskrivna i studier med en median efter minst 4 års uppföljning var förekomsten av myopati cirka 0,03%, 0,08% och 0,61% vid 20, 40 respektive 80 mg / dag.I dessa studier övervakades patienter noga och vissa interagerande läkemedel uteslöts.
I en klinisk studie där patienter med en historia av hjärtinfarkt behandlades med simvastatin 80 mg / dag (genomsnittlig uppföljning på 6,7 år) var förekomsten av myopati cirka 1,0% jämfört med en incidens på 0,02% som ses hos patienter behandlades med 20 mg / dag. Ungefär hälften av dessa fall av myopati inträffade under det första behandlingsåret. Incidensen av myopati under varje påföljande behandlingsår var cirka 0,1% (se avsnitt 4.8 och 5.1).
Risken för myopati är högre hos patienter som behandlas med INEGY 10 mg / 80 mg än med andra statinbaserade behandlingar med liknande effekt för att sänka LDL-C. Därför ska INEGY 10 mg / 80 mg dosen endast användas till patienter med svår hyperkolesterolemi och hög risk för kardiovaskulära komplikationer som inte har uppfyllt behandlingsmålen med lägre doser och när fördelarna förväntas vara större potentiella risker. Hos patienter som behandlas med INEGY 10 mg / 80 mg för vilka ett interaktionsmedel krävs, bör en lägre dos INEGY eller en alternativ statinbehandling med lägre potential för läkemedelsinteraktioner användas (se nedan. Åtgärder för att minska risken för myopati orsakad av läkemedelsinteraktioner och punkterna 4.2, 4.3 och 4.5).
I en klinisk studie där över 9 000 patienter med kronisk njursjukdom randomiserades för att få INEGY 10 mg / 20 mg dagligen (n = 4650) eller placebo (n = 4620) (medianuppföljning på 4,9 år), förekomst av myopati var 0,2% för INEGY och 0,1% för placebo (se avsnitt 4.8).
I en klinisk studie där patienter med hög risk för kardiovaskulär sjukdom behandlades med simvastatin 40 mg / dag (medianuppföljning på 3,9 år) var förekomsten av myopati cirka 0,05% för patienter. Icke-kinesiska (n = 7367) kontra 0,24% för kinesiska patienter (n = 5 468). Även om den enda asiatiska befolkningen som utvärderades i denna kliniska studie var kinesisk, bör försiktighet iakttas vid förskrivning av INEGY till asiatiska patienter och den lägsta dosen måste nödvändigtvis användas.
Minskad funktionalitet hos transportproteiner
Minskad funktion av levertransportproteiner OATP kan öka systemisk exponering för simvastatinsyra och öka risken för myopati och rabdomyolys. Nedsatt funktion kan uppstå både som ett resultat av inhibering av interagerande läkemedel (t.ex. cyklosporin) och hos patienter som bär SLCO1B1 -genotyp c. 521T> C.
Patienter som bär SLCO1B1 -genallelen (c.521T> C) som kodar för ett mindre aktivt OATP1B1 -protein har ökad systemisk exponering för simvastatinsyra och ökad risk för myopati. Risken för myopati relaterad till en hög dos (80 mg) av simvastatin är totalt cirka 1%, utan genetisk testning. Baserat på resultaten från SEARCH -studien har bärare av den homozygota C -allelen (även kallad CC) behandlade med 80 mg en 15% risk att utveckla myopati inom ett år, medan risken för heterozygota bärare av C -allelen (CT) är 1,5%. Den relativa risken är 0,3% hos patienter med den vanligaste genotypen (TT) (se avsnitt 5.2). Om det är tillgängligt bör genotypning för förekomst av C-allelen övervägas som en del av nytta-riskbedömningen innan simvastatin förskrivs till enskilda patienter och höga doser, i de där det finns. CC-genotyp, bör undvikas. Frånvaron av denna gen vid genotypning utesluter dock inte möjligheten att myopati utvecklas.
Mätning av kreatinkinasnivåer
CK -nivåer bör inte mätas efter ansträngande träning eller i närvaro av någon annan orsak till CK -ökning eftersom detta kan göra data svåra att tolka. Om CK-nivåerna är signifikant förhöjda vid baslinjen (större än 5 gånger den övre gränsen för det normala) bör dessa mätas om inom 5-7 dagar för att resultaten ska bekräftas.
Innan behandlingen
Alla patienter som börjar med INEGY -behandling eller ökar dosen av INEGY bör informeras om risken för myopati och instrueras att rapportera om oförklarlig muskelsmärta, ömhet och svaghet omedelbart.
Försiktighet bör iakttas hos patienter med predisponerande faktorer för rabdomyolys. För att fastställa ett referensvärde för baslinjen bör CK -nivån mätas innan behandling påbörjas i följande fall:
• äldre (ålder ≥ 65 år)
• kvinnligt kön
• njurskada
• okontrollerad hypotyreos
• personlig eller familjehistoria av ärftliga muskelsjukdomar
• historia av tidigare episoder av muskeltoxicitet med statin eller fibrat
• alkoholmissbruk.
I ovanstående fall måste risken som behandlingen innebär vägas mot den möjliga nyttan, och noggrannare övervakning av patienten rekommenderas vid behandling. Om patienten tidigare har upplevt muskelsjukdomar under behandling med ett fibrat eller ett statin, bör behandling med en statinhaltig produkt (t.ex. INEGY) endast påbörjas med försiktighet. Om CK -nivåerna är signifikant förhöjda vid baslinjen (större än 5 gånger den övre gränsen för det normala), ska behandling inte påbörjas.
Under behandlingen
Om patienten rapporterar muskelsmärta, svaghet eller kramper under behandling med INEGY ska CK -nivåerna mätas. Vid signifikant förhöjda CK -nivåer (större än 5 gånger den övre gränsen för det normala), i avsaknad av ansträngande träning, ska behandlingen avbrytas. Avbrytande av behandlingen kan övervägas vid allvarliga muskelsymtom som orsakar dagligt obehag, även om CK -värdena förblir under 5 gånger normalgränsen. Behandlingen bör avbrytas om det finns misstanke om myopati av någon annan anledning.
Det har varit mycket sällsynta rapporter om immunförmedlad nekrotiserande myopati (IMNM) under eller efter behandling med vissa statiner. IMNM kännetecknas kliniskt av ihållande proximal muskelsvaghet och förhöjt serumkreatinkinas, som kvarstår trots avbrott av statinbehandling (se avsnitt 4.8).
Om symtomen avtar och CK -nivåerna återgår till det normala kan återinförande av INEGY eller annan produkt som innehåller ett annat statin övervägas vid lägsta dos och under noggrann övervakning.
En högre förekomst av myopati har observerats hos patienter som titrerats till simvastatin 80 mg (se avsnitt 5.1) Det rekommenderas att CK -nivåer mätas regelbundet eftersom de kan vara användbara för att identifiera subkliniska fall av myopati. Det finns dock ingen säkerhet sådan övervakning kommer att förhindra myopati.
INEGY -behandlingen bör tillfälligt avbrytas några dagar innan större elektiv kirurgi och om något större medicinskt eller kirurgiskt tillstånd utvecklas.
Åtgärder för att minska risken för myopati orsakad av läkemedelsinteraktioner (se även avsnitt 4.5)
Risken för myopati och rabdomyolys ökar signifikant genom samtidig användning av INEGY med kraftfulla CYP3A4 -hämmare (såsom itrakonazol, ketokonazol, posakonazol, vorikonazol, erytromycin, klaritromycin, telitromycin, HIV -proteashämmare (t.ex. nelfinavir), nelfinavir), nelfinavir) nefazodon och läkemedel som innehåller kobicistat), som med cyklosporin, danazol och gemfibrozil. Användningen av dessa läkemedel är kontraindicerad (se avsnitt 4.3).
På grund av förekomsten av simvastatin i INEGY ökar också risken för myopati och rabdomyolys genom samtidig användning av andra fibrater, niacin vid lipidsänkande doser (≥ 1 g / dag) eller samtidig användning av amiodaron, amlodipin, verapamil eller diltiazem med vissa doser INEGY (se avsnitt 4.2 och 4.5). Risken för myopati, inklusive rabdomyolys, kan öka när INEGY administreras samtidigt med fusidinsyra. Hos patienter med homozygot IF kan denna risk ökas genom samtidig användning av lomitapid och INEGY (se avsnitt 4.5).
När det gäller CYP3A4 -hämmare är samtidig användning av INEGY med itrakonazol, ketokonazol, posakonazol, vorikonazol, hiv -proteashämmare (t.ex. nelfinavir), boceprevir, telaprevir, erytromycin, klaritromycin, telitromycin och nefitromicin och 4.5). Om behandling med potenta CYP3A4-hämmare (medel som ökar AUC cirka fem gånger eller mer) inte kan undvikas, ska INEGY-behandlingen avbrytas (och användningen av ett annat statin bör övervägas) under behandlingen. Dessutom bör man vara försiktig när man kombination av INEGY med några andra mindre potenta CYP3A4 -hämmare: flukonazol, verapamil, diltiazem (se avsnitt 4.2 och 4.5). Samtidig intag av grapefruktjuice och INEGY bör undvikas.
Simvastatin ska inte ges samtidigt med fusidinsyra. Det har rapporterats om rabdomyolys (inklusive vissa dödsfall) hos patienter som får denna kombination (se avsnitt 4.5). Hos patienter där användning av systemisk fusidinsyra anses vara väsentlig, bör statinbehandling avbrytas under behandling med fusidinsyra.Patienter bör rådas att omedelbart söka läkarvård om symtom utvecklas: muskelsvaghet, smärta eller ömhet.
Statinbehandling kan återinföras sju dagar efter den sista dosen av fusidinsyra.I undantagsfall där långvarig systemisk användning av fusidinsyra krävs, till exempel för att behandla allvarliga infektioner, bör behovet av samtidig administrering av INEGY och fusidinsyra endast utvärderas från fall till fall under strikt medicinsk övervakning.
Samtidig användning av INEGY vid doser över 10 mg / 20 mg per dag och niacin vid lipidsänkande doser (≥1 g / dag) bör undvikas om inte den kliniska nyttan sannolikt överväger den ökade risken för myopati (se avsnitt 4.2 och 4.5).
Sällsynta fall av myopati / rabdomyolys har associerats med samtidig administrering av HMG-CoA-reduktashämmare och lipidmodifierande doser av niacin (nikotinsyra) (≥ 1 g / dag), som båda kan orsaka myopati ensam.
I en klinisk studie (medianuppföljning på 3,9 år) med patienter med hög risk för kardiovaskulär sjukdom och med välkontrollerade LDL-C-nivåer på simvastatin 40 mg / dag med eller utan ezetimibe 10 mg, fanns det ingen ytterligare fördel med kardiovaskulära utfall med tillägg av lipidmodifierande doser av niacin (nikotinsyra) (≥1 g / dag). Därför överväger läkare kombinationsbehandling med simvastatin och lipidmodifierande niacin (nikotinsyra) (≥ 1 g / dag) eller niacin -innehållande produkter bör noggrant väga de potentiella fördelarna och riskerna och bör noggrant övervaka patienterna för tecken eller symtom på muskelsmärta, känslighet eller svaghet, särskilt under de första månaderna av behandlingen och när doserna av det ena eller det andra läkemedlet ökas.
Dessutom var förekomsten av myopati i denna studie cirka 0,24% för kinesiska patienter som behandlats med simvastatin 40 mg eller ezetimibe / simvastatin 10 mg / 40 mg jämfört med 1,24% för kinesiska patienter som behandlats med simvastatin 40 mg eller ezetimibe / simvastatin 10 mg / 40 mg administreras samtidigt med nikotinsyra / laropiprant 2000 mg / 40 mg modifierad frisättning. Även om den enda asiatiska befolkningen som utvärderades i denna kliniska studie var den kinesiska, eftersom förekomsten av myopati är högre hos kinesiska patienter än hos icke-kinesiska patienter, kan samtidig administrering av INEGY med doser av niacin (nikotinsyra) ändra lipidprofilen ( ≥ 1 g / dag) rekommenderas inte till asiatiska patienter.
Acipimox är strukturellt relaterat till niacin. Även om acipimox inte har studerats kan risken för muskelrelaterade toxiska effekter vara liknande den för niacin.
Samtidig användning av INEGY vid doser över 10 mg / 20 mg per dag och amiodaron, amlodipin, verapamil eller diltiazem bör undvikas.Patienter med homozygot IF ska kombinerad användning av INEGY i doser över 10 mg / 40 mg per dag med lomitapid bör undvikas. (Se avsnitt 4.2, 4.3 och 4.5)
Patienter som tar andra läkemedel som är kända för att ha en måttlig hämmande effekt på CYP3A4 vid terapeutiska doser vid samtidig användning med INEGY, särskilt med högre doser INEGY, kan ha ökad risk för myopati. Vid samtidig administrering av INEGY med en måttlig CYP3A4-hämmare (medel som ökar AUC cirka 2-5 gånger) kan en dosjustering vara nödvändig. För vissa måttliga CYP3A4 -hämmare, t.ex. diltiazem, rekommenderas en maximal dos på 10 mg / 20 mg INEGY (se avsnitt 4.2).
Säkerhet och effekt för INEGY administrerat med fibrater har inte studerats. Det finns en ökad risk för myopati vid samtidig användning av simvastatin och fibrater (särskilt gemfibrozil). Därför är samtidig användning av INEGY och gemfibrozil kontraindicerat (se avsnitt 4.3) och samtidig användning med andra fibrater rekommenderas inte (se avsnitt 4.5).
Leverenzymer
I kontrollerade kombinationsdoseringsstudier där patienter behandlades med ezetimibe och simvastatin observerades på varandra följande förhöjningar i transaminaser (≥3 gånger övre gräns för normal [ULN]) (se avsnitt 4.8).
I en kontrollerad klinisk prövning där över 9 000 patienter med kronisk njursjukdom randomiserades till att få INEGY 10 mg / 20 mg dagligen (n = 4650) eller placebo (n = 4620) (median uppföljningsperiod på 4,9 år), förekom incidensen av på varandra följande transaminashöjningar (> 3 gånger ULN) var 0,7% för INEGY och 0,6% för placebo (se avsnitt 4.8).
Det rekommenderas att leverfunktionstester utförs innan behandling påbörjas med INEGY och därefter vid klinisk indikation. Patienter som titreras till 10 mg / 80 mg dosen ska genomgå ett ytterligare test före titrering, 3 månader efter titrering till 10 mg / 80 mg dosen och regelbundet därefter (t.ex. var sjätte månad) under det första behandlingsåret. Särskild uppmärksamhet bör ägnas patienter som utvecklar förhöjningar av serumtransaminaser och hos dessa patienter bör blodprov upprepas omedelbart och utföras oftare därefter. Om transaminasnivåer visar tecken på progression, särskilt om de stiger till 3 gånger ULN och är ihållande, ska läkemedelsbehandling avbrytas. Observera att ALAT kan uppstå från muskler, därför kan en ökning av ALAT och CK indikera myopati (se ovan Myopati / rabdomyolys).
Det har förekommit sällsynta rapporter efter marknadsföring om dödligt och icke-dödligt leversvikt hos patienter som tar statiner, inklusive simvastatin. Om allvarlig leverskada med kliniska symptom och / eller hyperbilirubinemi eller gulsot uppstår under behandling med INEGY, avbryt behandlingen omedelbart. Om det inte finns någon alternativ etiologi, starta inte om behandlingen med INEGY.
INEGY ska användas med försiktighet hos patienter som konsumerar betydande mängder alkohol.
Nedsatt leverfunktion
På grund av de okända effekterna av den ökade exponeringen för ezetimib hos patienter med måttligt eller svårt nedsatt leverfunktion rekommenderas INEGY inte (se avsnitt 5.2).
Diabetes mellitus
Vissa bevis tyder på att statiner, som en klasseffekt, ökar blodsockret och hos vissa patienter med hög risk att utveckla diabetes kan orsaka en nivå av hyperglykemi så att antidiabetisk behandling är lämplig.
Denna risk uppvägs dock av minskningen av kärlrisken med användning av statiner och bör därför inte vara en anledning till att behandlingen med statiner avbryts.
Riskpatienter (fastande glukos 5,6 till 6,9 mmol / L, BMI> 30 kg / m2, förhöjda triglyceridnivåer, hypertoni) bör övervakas både kliniskt och biokemiskt i enlighet med nationella riktlinjer.
Pediatrisk population
Säkerheten och effekten av ezetimib som administreras samtidigt med simvastatin hos patienter i åldern 10 till 17 år med heterozygot familjär hyperkolesterolemi utvärderades i en kontrollerad klinisk studie på ungdomar (Tanner stadium II eller högre) och flickor. minst ett år.
I denna begränsade kontrollerade studie hade det i allmänhet ingen effekt på sexuell tillväxt eller mognad hos unga pojkar eller flickor, eller någon effekt på menstruationscykellängden hos flickor. Effekterna av ezetimib under en behandlingsperiod> 33 veckor på sexuell tillväxt och mognad har dock inte studerats (se avsnitt 4.2 och 4.8).
Säkerhet och effekt för ezetimib som ges samtidigt med simvastatindoser över 40 mg dagligen har inte studerats hos barn mellan 10 och 17 år.
Ezetimibe har inte studerats hos patienter yngre än 10 år eller hos flickor före menarche (se avsnitt 4.2 och 4.8).
Den långsiktiga effekten av ezetimibterapi hos patienter under 17 år för att minska vuxens sjuklighet och dödlighet har inte studerats.
Buntar
Säkerhet och effekt för ezetimib administrerat med fibrater har inte fastställts (se ovan och avsnitt 4.3 och 4.5).
Antikoagulantia
Om INEGY tillsätts till warfarin, ett annat kumarinantikoagulantia eller fluindion, bör International Normalized Ratio övervakas tillräckligt (se avsnitt 4.5).
Interstitiell lungsjukdom
Fall av interstitiell lungsjukdom har rapporterats med vissa statiner, inklusive simvastatin, särskilt med långtidsbehandling (se avsnitt 4.8). Symtomen kan vara dyspné, icke-produktiv hosta och försämring av allmän hälsa (trötthet, viktminskning och feber). Om det misstänks att en patient har utvecklat interstitiell lungsjukdom ska INEGY -behandlingen avbrytas.
Hjälpämne
Patienter med sällsynta ärftliga problem med galaktosintolerans, Lapp-laktasbrist eller glukos-galaktosmalabsorption bör inte ta detta läkemedel.
04.5 Interaktioner med andra läkemedel och andra former av interaktion
Farmakodynamiska interaktioner
Interaktioner med lipidsänkande läkemedel som kan orsaka myopati när de ges ensamma
Risken för myopati, inklusive rabdomyolys, ökar vid samtidig administrering av simvastatin med fibrater. Dessutom orsakar en "farmakokinetisk interaktion mellan simvastatin och gemfibrozil en ökning av plasmanivåerna av simvastatin (se nedan, Farmakokinetiska interaktioner och avsnitt 4.3 och 4.4). Sällsynta fall av myopati / rabdomyolys har associerats med samtidig administrering av simvastatin och lipidmodifierande doser av niacin (≥ 1 g / dag) (se avsnitt 4.4).
Fibrater kan öka utsöndringen av kolesterol i gallan, vilket leder till kolelithiasis.I en preklinisk studie på hundar ökade ezetimibe kolesterolet i gallblåsan (se avsnitt 5.3). Även om relevansen av dessa prekliniska data för människor är okänd, rekommenderas inte samtidig administrering av INEGY med fibrater (se avsnitt 4.4).
Farmakokinetiska interaktioner
Förskrivningsrekommendationer för interagerande medel sammanfattas i följande tabell (ytterligare detaljer finns i texten; se även avsnitt 4.2, 4.3 och 4.4).
Interaktionsmedicin i samband med ökad risk för myopati / rabdomyolys
av myopati / rabdomyolys
Andra läkemedels effekter på INEGY
INEGY
Niacin: I en studie med 15 friska vuxna gav samtidig användning av INEGY (10 mg / 20 mg dagligen i 7 dagar) en liten ökning av medelvärdena AUC för niacin (22%) och nikotinursyra (19%).), ges som NIASPAN depottabletter (1000 mg i 2 dagar och 2000 mg i 5 dagar efter en fettsnål frukost). I samma studie resulterade samtidig användning av NIASPAN i en liten ökning av de genomsnittliga AUC -värdena för ezetimib (9%), totalt ezetimib (26%), simvastatin (20%) och simvastatinsyra (35%). (Se avsnitt 4.2 och 4.4).
Inga läkemedelsinteraktionsstudier har utförts med högre doser av simvastatin.
Ezetimibe
Antacida: Samtidig administrering av antacida minskade absorptionshastigheten för ezetimib men hade ingen effekt på biotillgängligheten av ezetimib. Denna minskning av absorptionshastigheten anses inte vara kliniskt signifikant.
Kolestyramin: samtidig administrering av kolestyramin minskade medelarean under kurvan (AUC) för totalt ezetimib (ezetimibe + ezetimibe-glukuronid) med cirka 55%. Den ytterligare minskningen av lågdensitetslipoproteinkolesterol (LDL-C) på grund av tillsatsen av INEGY till kolestyramin kan minskas genom denna interaktion (se avsnitt 4.2).
Ciklosporin: I en studie med åtta post-njurtransplanterade patienter med kreatininclearance> 50 ml / min vid stabila doser av cyklosporin resulterade administrering av en enda 10 mg dos ezetimib i en 3,4-faldig ökning (intervallet 2,3-7,9 gånger) av genomsnittlig AUC för totalt ezetimib jämfört med en frisk kontrollpopulation från en annan studie som behandlats med ezetimibe ensam (n = 17.) I en annan studie visade en transplanterad patient med allvarligt nedsatt njurfunktion som tog cyklosporin och flera andra läkemedel 12 gånger högre "total exponering för" ezetimib jämfört med relaterade kontroller som behandlats med ezetimibe enbart. I en crossoverstudie med två perioder, av tolv friska försökspersoner, resulterade daglig administrering av ezetimibe 20 mg i 8 dagar med cyklosporin 100 mg engångsdos dag 7 i en genomsnittlig 15% ökning av cyklosporin AUC (intervall mellan en minskning av med 10% och en ökning med 51%) jämfört med en engångsdos på 100 mg enbart cyklosporin. Inga kontrollerade studier har utförts på effekten av samtidig administrering av ezetimib på exponering för cyklosporin hos njurtransplanterade patienter. Samtidig administrering av INEGY och cyklosporin är kontraindicerad (se avsnitt 4.3).
Buntar: Samtidig administrering av fenofibrat eller gemfibrozil ökade de totala koncentrationerna av ezetimib med cirka 1,5 respektive 1,7 gånger. Även om dessa ökningar inte anses vara kliniskt signifikanta, är samtidig administrering av INEGY och gemfibrozil kontraindicerat och med andra fibrater rekommenderas inte (se avsnitt 4.3 och 4.4).
Simvastatin
Simvastatin är ett substrat för cytokrom P450 3A4. Kraftiga hämmare av cytokrom P450 3A4 ökar risken för myopati och rabdomyolys genom att öka koncentrationen av HMG-CoA-reduktashämmande aktivitet i plasma under simvastatinbehandling. Sådana hämmare inkluderar itrakonazol, ketokonazol, posakonazol, vorikonazol, erytromycin, klaritromycin, telitromycin, hiv-proteashämmare (t.ex. nelfinavir), boceprevir, telaprevir, nefazodon och läkemedel som innehåller kobicistat. Mer än 10-faldig ökning av exponeringen av simvastatinsyra beta-hydroxisyrametabolit). Telitromycin orsakade en 11-faldig ökning av exponeringen av simvastatinsyra.
Kombinationen med itrakonazol, ketokonazol, posakonazol, vorikonazol, hiv -proteashämmare (t.ex. nelfinavir), boceprevir, telaprevir, erytromycin, klaritromycin, telitromycin, nefazodon och läkemedel som innehåller kobicistat, är kontraindicerad, liksom avsnitt ciclospibro . Om behandling med potenta CYP3A4-hämmare (medel som ökar AUC cirka fem gånger eller mer) är oundviklig, ska INEGY-behandlingen avbrytas (och användningen av ett annat statin bör övervägas) under behandlingens gång Försiktighet bör iakttas vid kombination av INEGY med några andra mindre potenta CYP3A4 -hämmare: flukonazol, verapamil eller diltiazem (se avsnitt 4.2 och 4.4).
Flukonazol: Sällsynta fall av rabdomyolys i samband med samtidig administrering av simvastatin och flukonazol har rapporterats. (se avsnitt 4.4).
Cyklosporin: risken för myopati / rabdomyolys ökar vid samtidig administrering av ciklosporin med INEGY; därför är användning med cyklosporin kontraindicerad (se avsnitt 4.3 och 4.4). Även om mekanismen inte är helt klarlagd har cyklosporin visat sig öka AUC för HMG-CoA-reduktashämmare. av simvastatinsyra beror förmodligen delvis på hämning av CYP3A4 och / eller OATP1B1.
Danazol: risken för myopati och rabdomyolys ökar vid samtidig administrering av danazol och INEGY; Därför är användning med danazol kontraindicerad (se avsnitt 4.3 och 4.4).
Gemfibrozil: gemfibrozil ökar AUC för surmetaboliten för simvastatin med 1,9 gånger, möjligen på grund av hämning av glukuronidering och / eller OATP1B1 (se avsnitt 4.3 och 4.4). Samtidig administrering med gemfibrozil är kontraindicerat.
Fusidinsyra: risken för myopati inklusive rabdomyolys kan ökas genom samtidig administrering av systemisk fusidinsyra och statiner. Samtidig administrering av denna kombination kan orsaka ökade plasmakoncentrationer av båda medlen. Mekanismen för denna interaktion (oavsett om den är farmakodynamisk eller farmakokinetisk eller båda) är fortfarande okänd. Det har rapporterats om rabdomyolys (inklusive vissa dödsfall) hos patienter som får denna kombination. Om behandling med fusidinsyra krävs, ska behandlingen med INEGY avbrytas under behandlingen med fusidinsyra (se avsnitt 4.4).
Amiodaron: risken för myopati och rabdomyolys ökar vid samtidig administrering av amiodaron och simvastatin (se avsnitt 4.4). I en klinisk studie rapporterades myopati hos 6% av patienterna som behandlades med simvastatin 80 mg och amiodaron. Därför bör INEGY -dosen inte överstiga 10 mg / 20 mg per dag hos patienter som samtidigt får behandling med amiodaron.
Kalciumkanalblockerare
•Verapamil: risken för myopati och rabdomyolys ökar vid samtidig administrering av verapamil och simvastatin 40 mg eller 80 mg (se avsnitt 4.4).
I en farmakokinetisk studie resulterade samtidig administrering av simvastatin med verapamil i en 2,3-faldig ökning av simvastatinsyraexponering förmodligen delvis på grund av hämning av CYP3A4. Dosen INEGY bör därför inte överstiga 10 mg / 20 mg per dag hos patienter som får samtidig behandling med verapamil.
• Diltiazem: risken för myopati och rabdomyolys ökar vid samtidig administrering av diltiazem och 80 mg simvastatin (se avsnitt 4.4). I en farmakokinetisk studie orsakade samtidig administrering av diltiazem och simvastatin en 2,7-faldig ökning av simvastatinsyraexponering, möjligen på grund av hämning av CYP3A4. Dosen INEGY bör därför inte överstiga 10 mg / 20 mg per dag hos patienter som får samtidig behandling med diltiazem.
• Amlodipin: patienter som samtidigt behandlas med amlodipin och simvastatin har en ökad risk för myopati. I en farmakokinetisk studie orsakade samtidig administrering av amlodipin en 1,6-faldig exponering av simvastatinsyra.Dosen INEGY bör därför inte överstiga 10 mg / 20 mg dagligen hos patienter som får amlodipin samtidigt.
Lomitapide: risken för myopati och rabdomyolys kan ökas genom samtidig administrering av lomitapid och simvastatin (se avsnitt 4.3 och 4.4). Därför, hos patienter med homozygot IF, bör INEGY -dosen inte överstiga 10 mg / 40 mg per dag hos patienter som får samtidig behandling med lomitapid.
Måttliga CYP3A4 -hämmare: Patienter som tar andra läkemedel som är kända för att ha en måttlig hämmande effekt på CYP3A4 när de används samtidigt med INEGY, särskilt med högre doser INEGY, kan ha en ökad risk för myopati (se avsnitt 4.4).
Hämmare av transportproteinet OATP1B1: simvastatinsyra är ett substrat för transportproteinet OATP1B1. Samtidig administrering av läkemedel som är hämmare av transportproteinet OATP1B1 kan leda till ökade plasmakoncentrationer av simvastatinsyra och ökad risk för myopati (se avsnitt 4.3 och 4.4).
Grapefruktjuice: grapefruktjuice hämmar cytokrom P450 3A4. Samtidigt intag av simvastatin och stora mängder (mer än en liter per dag) grapefruktjuice resulterade i en 7-faldig ökning av exponeringen av simvastatinsyra. Intag av 240 ml grapefruktjuice på morgonen och simvastatin på kvällen resulterade också i en 1,9-faldig ökning. Intag av grapefruktjuice under behandling med INEGY bör därför undvikas.
Kolkicin: Det har rapporterats om myopati och rabdomyolys vid samtidig administrering av kolchicin och simvastatin hos patienter med nedsatt njurfunktion. Noggrann klinisk övervakning av sådana patienter som tar denna kombination rekommenderas.
Rifampicin: eftersom rifampicin är en kraftig inducerare av CYP3A4 kan patienter som genomgår långvarig behandling med rifampicin (t.ex. behandling av tuberkulos) uppleva förlust av effektiviteten av simvastatin. I en farmakokinetisk studie på friska frivilliga minskade området under plasmakoncentrationskurvan (AUC) för simvastatinsyra med 93% vid samtidig administrering av rifampicin.
Niacin: Fall av myopati / rabdomyolys har observerats med simvastatin administrerat samtidigt med lipidmodifierande doser av niacin (≥ 1 g / dag) (se avsnitt 4.4).
Inegys effekter på andra läkemedels farmakokinetik
Ezetimibe
I prekliniska studier har det visat sig att ezetimibe inte inducerar cytokrom P450-enzymer som är inblandade i läkemedelsmetabolism. Inga kliniskt signifikanta farmakokinetiska interaktioner har observerats mellan ezetimib och läkemedel som är föremål för metabolism av cytokrom P450 1A2, 2D6. 2C8, 2C9 och 3A4 eller N- acetyltransferas.
Antikoagulantia: i en studie på tolv friska vuxna män hade samtidig administrering av ezetimib (10 mg en gång dagligen) ingen signifikant effekt på warfarins biotillgänglighet och protrombintid. Det har dock rapporterats efter marknadsföring om ökningar av det internationella normaliserade förhållandet hos patienter som hade tillsatt ezetimib till warfarin eller fluindion. Om INEGY tillsätts till warfarin eller ett annat kumarinantikoagulantia, eller till fluindion, bör INR övervakas tillräckligt ( se avsnitt 4.4).
Simvastatin: simvastatin har ingen hämmande effekt på cytokrom P450 3A4. Därför förväntas ingen verkan av simvastatin på plasmakoncentrationer av ämnen som metaboliseras via cytokrom P450 3A4.
Orala antikoagulantia: i två kliniska studier, en hos normala frivilliga och den andra hos hyperkolesterolemiska patienter, förstärkte simvastatin 20-40 mg / dag måttligt effekten av kumarinantikoagulantia; protrombintiden som rapporterats som International Normalized Ratio (INR) ökade från en baseline på 1,7 till 1,8 och från en baseline på 2,6 till 3,4 hos frivilliga respektive studiepatienter. Mycket sällsynta fall av hög INR har rapporterats. Hos patienter som behandlas med kumarinantikoagulantia bör protrombintid bestämmas innan behandling med INEGY påbörjas och tillräckligt ofta under de tidiga stadierna av behandlingen för att säkerställa att ingen signifikant förändring av protrombintiden inträffar. När en stabil protrombintid har dokumenterats kan protrombintiderna övervakas med de intervall som rutinmässigt rekommenderas för patienter på kumarinantikoagulantia. Om dosen INEGY ändras eller administreringen avbryts måste samma procedur upprepas. Simvastatinbehandling har inte associerats med blödning eller förändringar i protrombintid hos patienter som inte behandlas med antikoagulantia.
Pediatrisk population
Interaktionsstudier har endast utförts på vuxna.
04.6 Graviditet och amning
Graviditet
Åderförkalkning är en kronisk process och rutinmässigt avbrytande av lipidsänkande läkemedel under graviditeten måste ha en försumbar inverkan på den långsiktiga risken med primär hyperkolesterolemi.
INEGY
INEGY är kontraindicerat under graviditet. Inga kliniska data finns tillgängliga om användning av INEGY under graviditet. Djurstudier i kombinationsterapi har visat reproduktionstoxicitet (se avsnitt 5.3).
Simvastatin
Säkerheten för simvastatin hos gravida kvinnor har inte fastställts. Inga kontrollerade kliniska studier har utförts med simvastatin hos gravida kvinnor. Det har förekommit sällsynta rapporter om medfödda abnormiteter efter intrauterin exponering för HMG-CoA-reduktashämmare. I en prospektiv analys av cirka 200 graviditeter som under första trimestern exponerades för simvastatin eller en annan närbesläktad HMG-CoA-reduktashämmare var förekomsten av medfödda avvikelser jämförbar med den som observerades i den allmänna befolkningen. Detta antal graviditeter var statistiskt tillräckligt för att utesluta en ökning av medfödda anomalier med 2,5 gånger eller högre än baslinjeincidensen.
Även om det inte finns några tecken på att förekomsten av medfödda abnormiteter hos avkomman hos patienter som behandlats med simvastatin eller andra närbesläktade HMG-CoA-reduktashämmare skiljer sig från vad som ses i den allmänna befolkningen, kan behandling av mödrar med simvastatin minska fosternivåer av mevalonat, en föregångare till kolesterolbiosyntes. Av denna anledning ska INEGY inte användas till kvinnor som är gravida, som vill bli gravida eller misstänker att de är gravida. Behandling med INEGY bör avbrytas under graviditetens längd eller tills det inte har fastställts att kvinnan inte är gravid (se avsnitt 4.3).
Ezetimibe
Det finns inga kliniska prövningsdata om användning av ezetimib under graviditet.
Matdags
INEGY är kontraindicerat under amning. Studier på råttor har visat att ezetimib utsöndras i mjölk. Det är inte känt om de aktiva komponenterna i INEGY utsöndras i bröstmjölk (se avsnitt 4.3).
Fertilitet
Ezetimibe
Det finns inga data från kliniska studier om effekterna av ezetimib på människans fertilitet Ezetimibe hade ingen effekt på fertiliteten hos han- eller honråttor (se avsnitt 5.3).
Simvastatin
Inga kliniska studiedata om effekterna av simvastatin på människans fertilitet finns tillgängliga Simvastatin hade ingen effekt i fertilitetsstudier på råttor (se avsnitt 5.3).
04.7 Effekter på förmågan att framföra fordon och använda maskiner
Inga studier har utförts på förmågan att framföra fordon och använda maskiner, men vid körning eller användning av maskiner bör man komma ihåg att yrsel har rapporterats.
04.8 Biverkningar
Tabell över biverkningar (kliniska studier)
Säkerheten för INEGY (eller för samtidig administrering av ezetimib och simvastatin motsvarande INEGY) har utvärderats hos cirka 12 000 patienter i kliniska studier.
Frekvensen av biverkningar klassificeras enligt följande: mycket vanliga (≥ 1/10), vanliga (≥ 1/100,
Följande biverkningar observerades hos patienter behandlade med INEGY (N = 2.404) och med högre incidens än placebo (N = 1.340).
Följande biverkningar observerades hos patienter behandlade med INEGY (N = 9595) och med en högre förekomst än statiner en gång administrerade (N = 8 883).
Pediatrisk population
I en studie utförd på ungdomspatienter (10 till 17 år) med heterozygot familjär hyperkolesterolemi (n = 248) observerades förhöjningar av ALAT och / eller ASAT (≥ 3 X ULN, i följd) hos 3% (4 patienter) av patienter i gruppen ezetimibe / simvastatin mot 2% (2 patienter) av patienterna i gruppen simvastatin som monoterapi; procentsatserna för höjningar av CPK -värden (≥10 X ULN) var 2% (2 patienter) respektive 0%. Inga fall av myopati har rapporterats.
Denna studie var inte lämplig för att jämföra sällsynta läkemedelsbiverkningar.
Patienter med kronisk njursjukdom
I studien av hjärt- och njurskydd (SHARP) (se avsnitt 5.1), som involverade över 9000 patienter som behandlats med INEGY 10 mg / 20 mg dagligen (n = 4650) eller placebo (n = 4620), var de säkerhetsprofiler de jämförbara över en median uppföljningstid på 4,9 år. I denna studie registrerades endast allvarliga biverkningar och avbrott på grund av eventuella biverkningar. Avbrottsfrekvensen på grund av biverkningar var jämförbar (10,4% hos patienter som behandlades med INEGY, 9,8% hos patienter som behandlades med placebo). Förekomsten av myopati / rabdomyolys var 0,2% hos patienter som behandlades med INEGY och 0,1% hos patienter som behandlades med placebo.Konsekventa förhöjningar av transaminaser (> 3x ULN) inträffade hos 0,7% av patienterna. Behandlade med INEGY jämfört med 0,6% av patienterna som behandlades med I denna studie fanns det ingen statistiskt signifikant ökning av förekomsten av förspecificerade biverkningar, inklusive cancer (9,4% för INEGY, 9,5% för placebo), hepatit, kolecystektomi eller komplikationer av gallsten eller pankreatit.
Laboratoriets värden
I kombinationsdoseringsstudier var incidensen av kliniskt viktiga förhöjningar av serumtransaminaser (ALAT och / eller ASAT ≥ 3 X ULN, på varandra följande värden) 1,7% hos patienter som behandlats med INEGY. Dessa förhöjningar var i allmänhet asymptomatiska. Inte associerade med kolestas och återkom baslinjen efter avslutad behandling eller under behandlingens gång (se avsnitt 4.4).
Kliniskt relevanta ökningar av CK (≥10 X ULN) observerades hos 0,2% av patienterna som behandlades med INEGY.
Erfarenhet efter marknadsföring
Följande ytterligare biverkningar har rapporterats vid användning efter marknadsföring med INEGY eller i kliniska prövningar eller vid användning efter marknadsföring med en av de enskilda komponenterna.
Störningar i blodet och lymfsystemet: trombocytopeni; anemi
Nervsystemet: perifer neuropati; minnesskada
Andningsvägar, bröstkorg och mediastinum: hosta; dyspné; interstitiell lungsjukdom (se avsnitt 4.4)
Gastrointestinala störningar: förstoppning; pankreatit; gastrit
Hud och subkutan vävnad: alopeci; erythema multiforme; överkänslighetsreaktioner, inklusive utslag, urtikaria, anafylaksi, angioödem
Muskuloskeletala systemet och bindväv: muskelkramp; myopati * (inklusive myosit); rabdomyolys med eller utan akut njursvikt (se avsnitt 4.4); tendinopati, ibland komplicerad av bristning; immunförmedlad nekrotiserande myopati (IMNM) (frekvens ej känd) **
* I en klinisk studie förekom myopati vanligt hos patienter som behandlades med simvastatin 80 mg / dag jämfört med patienter som behandlades med 20 mg / dag (1,0% respektive 0,02%) (se avsnitt 4.4 och 4.5).
** Det har förekommit mycket sällsynta rapporter om immunförmedlad nekrotiserande myopati (IMNM), en autoimmun myopati, under eller efter behandling med vissa statiner. IMNM kännetecknas av: ihållande proximal muskelsvaghet och förhöjt serumkreatinkinas, som kvarstår trots avbrott av statinbehandling, muskelbiopsi som visar nekrotiserande myopati utan signifikant inflammation, förbättring med immunsuppressiva medel (se avsnitt 4.4).
Metabolism och näringsstörningar: minskad aptit
Kärlsjukdomar: värmevallningar; högt blodtryck
Allmänna symtom och / eller symtom vid administreringsstället: värk
Lever- och gallvägar: hepatit / gulsot; dödlig och icke-dödlig leversvikt; kolelithiasis; cholecystit
Reproduktionssystemet och bröstsjukdomar: erektil dysfunktion
Psykiatriska störningar: depression, sömnlöshet
Tydligen överkänslighetssyndrom har rapporterats sällan, inklusive några av följande: angioödem, lupusliknande syndrom, polymyalgia rheumatica, dermatomyosit, vaskulit, trombocytopeni, eosinofili, ökad erytrocytsedimenteringshastighet, artrit och artralgi, urtikaria, ljuskänslighet, feber, väsande andning.
Laboratoriets värden: förhöjt alkaliskt fosfatas; leverfunktionstest onormalt.
Ökningar av HbA1c och fastande serumglukosnivåer har rapporterats med statiner, inklusive simvastatin.
Det har förekommit sällsynta rapporter efter marknadsföring om kognitiv försämring (t.ex. minnesförlust, glömska, amnesi, minnesstörning, förvirring) i samband med statinanvändning, inklusive simvastatin. Rapporterna var i allmänhet icke-allvarliga. med varierande tider för symptomdebut (1 dag till år) och symptomupplösning (median 3 veckor).
Följande ytterligare biverkningar har rapporterats med vissa statiner:
• Sömnstörningar, inklusive mardrömmar
• Sexuell dysfunktion
• Diabetes mellitus: frekvensen beror på närvaron eller frånvaron av riskfaktorer (fastande blodsocker ≥ 5,6 mmol / L, BMI> 30 kg / m2, förhöjda triglyceridnivåer, hypertoni historia).
Rapportering av misstänkta biverkningar
Rapportering av misstänkta biverkningar som inträffar efter godkännande av läkemedlet är viktigt eftersom det möjliggör kontinuerlig övervakning av nytta / riskbalansen för läkemedlet. Vårdpersonal uppmanas att rapportera alla misstänkta biverkningar via det nationella rapporteringssystemet. "Adress: www .agenziafarmaco.gov.it/it/responsabili.
04.9 Överdosering
INEGY
Vid överdosering bör symtomatiska och stödjande åtgärder vidtas. Samtidig administrering av ezetimib (1 000 mg / kg) och simvastatin (1 000 mg / kg) tolererades väl i studier av akut oral toxicitet på möss och råttor. Inga kliniska tecken på toxicitet observerades hos dessa djur. Den orala LD50 -uppskattningen för båda arterna var ezetimibe ≥ 1000 mg / kg / simvastatin ≥ 1000 mg / kg.
Ezetimibe
I kliniska studier tolererades generellt väl administrering av ezetimib, 50 mg / dag till 15 friska försökspersoner i upp till 14 dagar, eller 40 mg / dag till 18 patienter med primär hyperkolesterolemi i upp till 56 dagar. Få fall av överdosering har rapporterats; de flesta av dem var inte associerade med biverkningar. De rapporterade biverkningarna var inte allvarliga. Hos djur observerades ingen toxicitet efter enstaka orala doser av 5.000 mg / kg ezetimib hos råttor och möss och 3000 mg / kg hos hundar.
Simvastatin
Få fall av överdosering har rapporterats; den maximala dosen som togs var 3,6 g. Alla patienter återhämtade sig utan följdsjukdomar.
05.0 FARMAKOLOGISKA EGENSKAPER
05.1 Farmakodynamiska egenskaper
Farmakoterapeutisk grupp: HMG-CoA-reduktashämmare i kombination med andra farmakologiska medel som modifierar lipidprofilen, ATC-kod: C10BA02
INEGY (ezetimibe / simvastatin) är en lipidsänkande produkt som selektivt hämmar tarmabsorberingen av kolesterol och relaterade växtsteroler och hämmar den endogena syntesen av kolesterol.
Handlingsmekanism
INEGY
Plasmakolesterol kommer från tarmabsorption och endogen syntes. INEGY innehåller ezetimibe och simvastatin, två lipidsänkande föreningar med komplementära verkningsmekanismer. INEGY minskar förhöjda nivåer av totalt kolesterol (total-C), LDL-C, apolipoprotein B (Apo B), triglycerider (TG), icke-högdensitetslipoprotein (C-icke-HDL) kolesterol och ökar kolesterolet för högt densitet lipoprotein (HDL-C) genom dubbel hämning av absorption och syntes av kolesterol.
Ezetimibe
Ezetimibe hämmar tarmabsorberingen av kolesterol. Ezetimibe är oralt aktivt och har en verkningsmekanism som skiljer sig från andra klasser av kolesterolsänkande ämnen (t.ex. statiner, gallsyrasekvestranter [hartser], fibrinsyraderivat och växtstanoler). Molekylmålet för ezetimib är steroltransportören , Niemann-Pick C1-Like 1 (NPC1L1), ansvarig för tarmupptagningen av kolesterol och fytosteroler.
Ezetimibe är lokaliserat på nivån av tunntarmens borstgräns och hämmar absorptionen av kolesterol, vilket orsakar en minskning av passage av tarmkolesterol till levern; statiner minskar syntesen av kolesterol i levern och dessa två distinkta mekanismer ger en komplementär minskning av kolesterol. I en 2-veckors klinisk studie av 18 hyperkolesterolemiska patienter hämmade ezetimibe tarmabsorberingen av kolesterol med 54% jämfört med placebo.
En rad prekliniska studier utfördes för att bestämma selektiviteten av ezetimib för att hämma absorptionen av kolesterol. Ezetimibe hämmade absorptionen av [14C] -kolesterol utan påverkan på absorptionen av triglycerider, fettsyror, gallsyror, progesteron, etinylöstradiol, eller fettlösliga vitamin A och D.
Simvastatin
Efter oralt intag hydrolyseras simvastatin, som är en inaktiv lakton, i levern till motsvarande aktiv beta-hydroxisyraform som har kraftig hämmande aktivitet på HMG-CoA-reduktas (3-hydroxi-3metylglutaryl CoA-reduktas). Detta enzym katalyserar omvandlingen av HMG-CoA till mevalonat, ett tidigt och begränsande steg i kolesterolbiosyntesen.
Simvastatin har visat sig minska både normala och förhöjda LDL-C-koncentrationer. LDL bildas av lipoprotein med mycket låg densitet (VLDL) och kataboliseras huvudsakligen av LDL-receptorn med hög affinitet. C-VLDL) och induktion av LDL-receptorn, vilket leder till en minskning av produktionen och en ökning av LDL-C katabolism. Apolipoprotein B minskar också väsentligt under behandling med simvastatin. Simvastatin ökar också måttligt HDL-C och minskar plasma-TG. Som ett resultat av dessa förändringar minskar förhållandet mellan totalt kolesterol / HDL-C och LDL-C / C-HDL.
Klinisk effekt och säkerhet
I kontrollerade kliniska prövningar minskade INEGY signifikant total-C, LDL-C, Apo B, TG och icke-HDL-C och ökade HDL-C hos patienter med hyperkolesterolemi.
Primär hyperkolesterolemi
I en 8-veckors, dubbelblind, placebokontrollerad studie, 240 patienter med hyperkolesterolemi redan på simvastatin monoterapi och som inte lyckades uppnå LDL-C-mål enligt National Cholesterol Education Program (NCEP) (från 2, 6 till 4,1 mmol) / l [100 till 160 mg / dl beroende på baslinjeegenskaper) randomiserades för att få ezetimibe 10 mg eller placebo utöver deras redan existerande simvastatinbehandling. hade inte nått baslinjen LDL-C-mål (~ 80%), signifikant mer patienter randomiserade till ezetimibe ges med simvastatin uppnådde LDL-C-målet vid studiens slutpunkt jämfört med patienter randomiserade till placebo administrerade samtidigt med simvastatin, 76% respektive 21,5%.
Motsvarande minskning av LDL-C för ezetimib eller placebo administrerat samtidigt med simvastatin var signifikant olika (27% respektive 3%).
Dessutom minskade ezetimibe, administrerat samtidigt med simvastatinbehandling, signifikant total-C, Apo B, TG jämfört med placebo administrerat samtidigt med simvastatin.
I en 24-veckors dubbelblind multicenterstudie behandlade 214 patienter med typ 2-diabetes mellitus behandlade med tiazolidindioner (rosiglitazon och pioglitazon) i minst 3 månader och simvastatin 20 mg i minst 6 veckor med en genomsnittlig LDL-C på 2,4 mmol / l (93 mg / dl) randomiserades till antingen 40 mg simvastatin eller samtidig administrering av aktiva substanser motsvarande INEGY 10 mg / 20 mg. INEGY 10 mg / 20 mg var signifikant effektivare än att fördubbla simvastatindosen till 40 mg för att ytterligare minska LDL-C (-21% respektive 0%), total-C (-14% respektive -1%), ApoB (-14% respektive -2%) och C-icke-HDL (-20% respektive -2%) över de minskningar som observerades med simvastatin 20 mg. Resultaten för HDL-C och TG mellan de två behandlingsgrupperna var inte signifikant olika och resultaten påverkades inte av typen av behandling med tiazolidindioner.
Effekten av de olika doserna INEGY (10 mg / 10 mg till 10 mg / 80 mg / dag) visades i en 12-veckors dubbelblind, placebokontrollerad, multicenterstudie som inkluderade alla doser tillgängliga av INEGY och alla relaterade simvastatin styrkor.
Vid jämförelse av patienter som behandlats med alla doser INEGY med patienter som behandlats med alla doser av simvastatin reducerade INEGY signifikant total-C, LDL-C och TG (se tabell 1) och även Apo B (-42% respektive -29%) , icke-HDL-C (-49% respektive -34%) och C-reaktivt protein (-33% respektive -9%). Effekterna av INEGY på HDL-C var liknande effekterna som observerades med simvastatin. Ytterligare analys visade att INEGY signifikant ökade HDL-C jämfört med placebo.
bord 1
Svar på INEGY hos patienter med primär hyperkolesterolemi (genomsnittlig förändring% från baslinjen i frånvaro av behandling b)
a För triglycerider, median% avvikelse från baslinjen
b Basal - inte vid lipidsänkande läkemedelsbehandling
c Kombinerade doser av INEGY (10 / 10-10 / 80) minskade signifikant total-C, LDL-C och TG, jämfört med simvastatin, och signifikant ökade HDL-C jämfört med placebo.
I en liknande utformad studie var resultaten för alla lipidparametrar generellt överensstämmande. I en kombinerad analys av dessa två studier var lipidsvaret på INEGY liknande hos patienter med TG -nivåer större än eller mindre än 200 mg / dL.
I en multicenter, dubbelblind, kontrollerad klinisk studie (ENHANCE) randomiserades 720 patienter med heterozygot familjär hyperkolesterolemi till att få ezetimibe 10 mg i kombination med simvastatin 80 mg (n = 357) eller simvastatin 80 mg (n = 363) för 2 år. Studiens primära mål var att undersöka effekten av kombinationsbehandlingen ezetimibe / simvastatin på tjockleken på tunica intima och media (IMT) hos halspulsådern jämfört med simvastatin ensam. Effekten av denna markör är ännu inte påvisad. Surrogat för kardiovaskulär sjuklighet och dödlighet.
Den primära slutpunkten, den genomsnittliga IMT-förändringen för alla sex halspulssegmenten, var inte signifikant olika (p = 0,29) mellan de två behandlingsgrupperna baserat på ultraljudsmätningar i B-läge. Med ezetimibe 10 mg i kombination med simvastatin 80 mg eller simvastatin 80 mg ensamt ökade tjockleken på intima och medial tunika med 0,0111 mm respektive 0,0058 mm under den 2-åriga studietiden (vid baslinjen var medelvärdet av IMT-mätning i halspulsådern 0,68 mm respektive 0,69 mm).
Ezetimibe 10 mg i kombination med simvastatin 80 mg minskade LDL-C, total-C, Apo B och TG betydligt mer än simvastatin 80 mg. För de två behandlingsgrupperna var procentuell ökning av C -HDL liknande. Biverkningar som rapporterats med ezetimibe 10 mg i kombination med simvastatin 80 mg överensstämde med dess kända säkerhetsprofil.
INEGY innehåller simvastatin. I två stora placebokontrollerade kliniska prövningar, Scandinavian Simvastatin Survival Study (20-40 mg n = 4444 patienter) e Hjärtskyddsstudie (40 mg; N = 20 536 patienter) utvärderades effekten av simvastatinbehandling hos patienter med hög risk för kranskärlssjukdomar på grund av pågående kranskärlssjukdom, diabetes, perifer kärlsjukdom, stroke eller annan cerebrovaskulär sjukdom. Behandling med simvastatin har har visat sig minska: risken för total dödlighet genom minskning av dödsfall på grund av CHD, risken för icke-dödligt hjärtinfarkt och stroke; och behovet av kirurgi med koronar och icke-koronar revaskularisering.
Studien av effektiviteten av ytterligare minskningar av kolesterol och homocystein (SÖK) utvärderade effekten av behandling med simvastatin 80 mg mot 20 mg (medianuppföljning av 6,7 år) på större kärlhändelser (MVE; definieras som dödligt ischemiskt hjärta sjukdom, icke-dödligt hjärtinfarkt, koronarrevaskulariseringsprocedur, icke-dödlig eller dödlig stroke eller perifer revaskulariseringsprocedur) hos 12 064 patienter med hjärtinfarkt i historia. Det fanns ingen signifikant skillnad i förekomsten av MVE mellan 2 grupper; simvastatin 20 mg (n = 1 553; 25,7%) mot simvastatin 80 mg (n = 1 477; 24,5%); RR 0,94, 95%CI: 0,88 till 1, 01. Den absoluta skillnaden i LDL-C-nivå mellan de två grupperna över studiens gång var 0,35 ± 0,01 mmol / L. Säkerhetsprofilerna var likartade mellan de två behandlingsgrupperna förutom "förekomst av myopati som var cirka 1,0% för patienter som behandlats med simvastatin 80 mg jämfört med 0,02% för patienter behandlade med 20 mg. Ungefär hälften av dessa myopatifall inträffade under det första behandlingsåret. Förekomsten av myopati under varje påföljande behandlingsår var cirka 0,1%.
INEGY har visat sig minska stora kardiovaskulära händelser hos patienter med kronisk njursjukdom; en ökning av fördelarna med INEGY för kardiovaskulär morbiditet och dödlighet jämfört med den som visats för simvastatin har dock inte fastställts definitivt.
Pediatrisk population
I en multicenter, dubbelblind, kontrollerad studie, 142 pojkar (Tanner stadium II och högre) och 106 postmenarche tjejer, 10 till 17 år (medelålder 14,2 år) med heterozygot familjär hyperkolesterolemi (IF heterozygot) med baslinje LDL-C värden från 4,1 till 10,4 mmol / l randomiserades till ezetimibe 10 mg samtidigt administrerat med simvastatin (10, 20 eller 40 mg) eller simvastatin (10, 20 eller 40 mg) ensamt i 6 veckor, ezetimibe och simvastatin 40 mg samtidigt administrerat eller simvastatin 40 mg ensamt under de kommande 27 veckorna, och sedan ezetimibe och simvastatin (10 mg, 20 mg eller 40 mg) samtidigt administrerat öppen etikett i 20 veckor.
Vid vecka 6 minskade ezetimibe samtidigt med simvastatin (alla doser) signifikant total-C (38% mot 26%), LDL-C (49% mot 34%), Apo B (39% mot 27%) och icke- HDL-C (47% vs 33%) jämfört med simvastatin enbart (alla doser). Resultaten var liknande mellan de två behandlingsgrupperna för TG och HDL-C (-17% vs -12% respektive +7% vs +6% Vid vecka 33 överensstämde resultaten med resultaten från vecka 6 och betydligt fler patienter på ezetimibe och simvastatin 40 mg (62%) uppnådde "idealiskt terapeutiskt mål enligt NCEP AAP (
Säkerhet och effekt för ezetimib som ges samtidigt med simvastatindoser över 40 mg dagligen har inte studerats hos barn 10 till 17 år. Effekt har inte studerats hos patienter under 17 år. Långtidsbehandling med ezetimib för att minska sjuklighet och dödlighet i vuxen ålder.
Europeiska läkemedelsmyndigheten har avstått från skyldigheten att lämna in resultat från studier med INEGY i alla undergrupper av den pediatriska populationen för hyperkolesterolemi (se avsnitt 4.2 för information om pediatrisk användning).
Homozygot familjär hyperkolesterolemi (homozygot IF)
En 12-veckors, dubbelblind, randomiserad studie utfördes på patienter med en klinisk och / eller genotypisk diagnos av homozygot IF. Data från en undergrupp av patienter (n = 14) som behandlades med simvastatin 40 mg vid baslinjen analyserades. Ökning av simvastatindosen från 40 till 80 mg (n = 5) resulterade i en minskning av LDL-C från baslinjen med 13% jämfört med 40 mg simvastatin. Samtidig administrering av ezetimib och simvastatin motsvarande INEGY (10 mg / 40 mg och 10 mg / 80 mg kombinerat, n = 9) resulterade i en 23% minskning av LDL-C från baslinjen jämfört med simvastatin 40 mg. Hos patienter som administreras samtidigt med ezetimibe och simvastatin motsvarande INEGY (10 mg / 80 mg mg, n = 5 ), en LDL-C-minskning med 29% från baslinjen producerades jämfört med simvastatin 40 mg.
Förebyggande av större kärlhändelser vid kronisk njursjukdom (CKD)
Studien av hjärt- och njurskydd (SHARP) var en multinationell, randomiserad, placebokontrollerad, dubbelblind studie av 9438 patienter med kronisk njursjukdom, varav en tredjedel var i dialys vid baslinjen. Totalt 4 650 patienter tilldelades INEGY 10/20 och 4 620 till placebo och följde i en median på 4,9 år. Patienterna hade en medelålder på 62 år och 63% var män, 72% kaukasiska, 23% diabetiker och för dem som inte var i dialys var den genomsnittliga uppskattade glomerulära filtreringshastigheten (eGFR) 26,5 ml / min. / 1,73 m2. inget lipidbaserat inkluderingskriterium för studien. Genomsnittlig LDL-C vid baslinjen var 108 mg / dL. Efter ett år, inklusive patienter som inte längre tog studieläkemedel, minskades LDL-C med 26% jämfört med placebo med simvastatin 20 mg enbart och med 38 % med INEGY 10 mg / 20 mg.
Den primära jämförelsen som anges i SHARP-protokollet var en "intention-to-treat-analys av" större kärlhändelser "(MVE; definierat som icke-dödligt hjärtinfarkt eller hjärtdöd, stroke eller någon revaskulariseringsprocedur) endast hos de patienter som initialt randomiserades till INEGY (n = 4 193) eller placebo (n = 4 191) grupper. Sekundära analyser inkluderade samma sammansatta analyserad för hela den randomiserade kohorten (studiens baslinje eller 1 år) till INEGY (n = 4 650) eller placebo (n = 4 620) som samt komponenterna i denna komposit.
Den primära slutpunktsanalysen visade att INEGY signifikant minskade risken för större vaskulära händelser (749 patienter med händelser i placebogruppen kontra 639 i INEGY -gruppen) med en relativ riskminskning på 16% (p = 0,001).
Utformningen av denna studie tillät emellertid inte ett separat bidrag från monokomponenten ezetimib till effekt för att avsevärt minska risken för större kärlhändelser hos patienter med CKD.
De enskilda komponenterna i MVE hos alla randomiserade patienter visas i tabell 2. INEGY minskade signifikant risken för stroke och eventuell revaskularisering, utan några signifikanta numeriska skillnader som gynnade INEGY för icke-dödligt hjärtinfarkt och hjärtdöd.
Tabell 2
Större kärlhändelser efter behandlingsgrupp hos alla randomiserade patienter i SHARPa
a Analys av avsikt att behandla alla SHARP -patienter randomiserade till INEGY eller placebo vid baslinjen eller vid 1 år
b MAE; definieras som sammansättningen av icke-dödligt hjärtinfarkt, koronardöd, icke-hemorragisk stroke eller någon revaskularisering
Den absoluta minskningen av LDL-kolesterol som uppnåddes med INEGY var lägre bland patienter med en lägre LDL-C (
Aortastenos
Simvastatin och Ezetimibe för behandling av aortastenos (SEAS) var en multicenter, dubbelblind, placebokontrollerad studie med en genomsnittlig varaktighet på 4,4 år hos 1 873 patienter med asymptomatisk aortastenos (AS), dokumenterat med hastighetstopp aortaflödet mätt med Doppler mellan 2,5 och 4,0 m / s. Endast patienter registrerades för vilka statinbehandling inte ansågs nödvändigt för att minska risken för aterosklerotisk kardiovaskulär sjukdom. Patienter randomiserades i förhållandet 1: 1 för att få placebo eller ezetimibe 10 mg och simvastatin 40 mg dagligen vid samtidig administrering.
Det primära effektmåttet var sammansättningen av stora kardiovaskulära händelser (MCE) bestående av kardiovaskulär död, kirurgisk aortaklaffersättning (AVR), hjärtsvikt (CHF) till följd av progression av AS, icke-dödligt hjärtinfarkt, koronar bypass bypass (CABG) )), perkutan koronar intervention (PCI), sjukhusvistelse för instabil angina och icke-hemorragisk stroke De viktigaste sekundära slutpunkterna var sammansatta delmängder av händelsekategorierna för den primära slutpunkten.
Jämfört med placebo minskade inte ezetimibe / simvastatin 10 mg / 40 mg signifikant risken för MCE. Det primära utfallet inträffade hos 333 patienter (35,3%) i gruppen ezetimibe / simvastatin och hos 355 patienter (38,2%) i placebogruppen (riskförhållande i gruppen ezetimibe / simvastatin, 0,96; konfidensintervall 95%, 0,83 till 1,12; p = 0,59) Aortaklaffsbyte utfördes hos 267 patienter (28,3%) i gruppen ezetimibe / simvastatin och hos 278 patienter (29,9%) i placebogruppen (riskförhållande 1,00; 95%KI, 0,84 till 1,18; p = 0,97) Färre patienter hade ischemiska kardiovaskulära händelser i gruppen ezetimibe / simvastatin (n = 148) jämfört med placebogruppen (n = 187) (riskförhållande, 0,78; 95% KI, 0,63 till 0,97; p = 0,02), främst beroende på till det mindre antalet patienter de hade genomgått koronar bypass -ympning.
Cancer förekom oftare i gruppen ezetimibe / simvastatin (105 mot 70, p = 0,01). Den kliniska relevansen av denna observation är osäker, eftersom i den större SHARP -studien var det totala antalet patienter med någon typ av incidentcancer (438 i gruppen ezetimibe / simvastatin mot 439 i placebogruppen) inte annorlunda och därför var resultatet av SEAS studie kunde det inte bekräftas av SHARP.
05.2 Farmakokinetiska egenskaper
Inga signifikanta farmakokinetiska interaktioner observerades vid samtidig administrering av ezetimib och simvastatin.
Absorption
INEGY
INEGY är bioekvivalent med samtidig administrering av ezetimib och simvastatin.
Ezetimibe
Efter oral administrering absorberas ezetimibe snabbt och omfattande konjugerat till den farmakologiskt aktiva fenoliska glukuroniden (ezetimib-glukuronid). Medeltaxala plasmakoncentrationer (Cmax) observeras inom 1-2 timmar för ezetimibe-glukuronid och 4-12 timmar för ezetimibe. Absolut biotillgänglighet för ezetimib kan inte bestämmas eftersom föreningen är praktiskt taget olöslig i ett vattenhaltigt medium som är lämpligt för en injektion.
Samtidig administrering av mat (fettrika eller feta måltider) hade ingen effekt på den orala biotillgängligheten av ezetimib som 10 mg tabletter.
Simvastatin
Tillgängligheten av den aktiva β-hydroxisyran till systemcirkulationen efter en oral dos av simvastatin befanns vara mindre än 5% av dosen, i överensstämmelse med omfattande extraktion av första pass i levern. De viktigaste metaboliterna av simvastatin som finns i humant plasma är β-hydroxisyra och fyra andra aktiva metaboliter.
Plasmaprofilerna för både totala och aktiva hämmare ändrades inte genom administrering av simvastatin omedelbart före en standardmåltid jämfört med fasta.
Distribution
Ezetimibe
Ezetimibe och ezetimibe-glukuronid är 99,7% respektive 88-92% bundna till humana plasmaproteiner.
Simvastatin
Både simvastatin och β-hydroxisyra är bundna till humana plasmaproteiner (95%).
Simvastatins farmakokinetik i en och flera doser visade ingen läkemedelsackumulering efter flera doser. I alla ovanstående farmakokinetiska studier inträffade den maximala koncentrationen av hämmare 1,3 till 2,4 timmar efter dos.
Biotransformation
Ezetimibe
Ezetimibe metaboliseras främst i tunntarmen och levern via glukuronidkonjugering (en fas II -reaktion) med efterföljande biliär utsöndring. Minimal oxidativ metabolism (en fas I -reaktion) observerades hos alla utvärderade arter. Ezetimibe och ezetimibglukuronid är de huvudsakliga läkemedelshärledda föreningarna som finns i plasma och står för cirka 10-20% respektive 80-90% av det totala läkemedlet som finns i plasma. Både ezetimib och ezetimib-glukuronid elimineras långsamt från plasma med bevis av signifikant enterohepatisk cykel. Halveringstiden för ezetimib och ezetimib-glukuronid är cirka 22 timmar.
Simvastatin
Simvastatin är en inaktiv lakton som snabbt hydrolyseras in vivo i motsvarande β-hydroxisyra, en potent hämmare av HMG-CoA-reduktas Hydrolys sker huvudsakligen i levern; hydrolyshastigheten i mänsklig plasma är mycket långsam.
Hos människor absorberas simvastatin väl och genomgår snabb extraktion i levern. Extraktion i levern är beroende av leverblodflöde. Levern är dess främsta verkningsställe, med efterföljande utsöndring av likvärdiga ämnen i gallan. Tillgängligheten för det aktiva läkemedlet i systemcirkulationen är därför låg.
Efter intravenös administrering av β-hydroxisyrametaboliten var dess genomsnittliga halveringstid 1,9 timmar.
Eliminering
Ezetimibe
Efter oral administrering av 14C ezetimibe (20 mg) till människor stod totalt ezetimibe för cirka 93% av den totala plasmoradioaktiviteten. Cirka 78% och 11% av den administrerade radioaktiviteten återfanns i avföringen respektive urinen under en provtagningsperiod på 10 dagar. Efter 48 timmar fanns inga påvisbara nivåer av radioaktivitet i plasma.
Simvastatin
Simvastatinsyra transporteras aktivt till hepatocyter via bäraren OATP1B1.
Efter administrering av en oral dos simvastatin till människor utsöndrades 13% av radioaktiviteten i urinen och 60% i avföringen inom 96 timmar. Mängden som finns i avföringen representerar ekvivalenta ämnen som utsöndras i gallan såväl som det icke -absorberade läkemedlet. Efter intravenös administrering av β-hydroxisyrametaboliten utsöndrades endast i genomsnitt 0,3% av den intravenösa dosen i urinen som hämmare.
Särskilda populationer
Pediatrisk population
Absorption och metabolism av ezetimib är liknande hos barn och ungdomar (10 till 18 år) och vuxna. Det finns inga farmakokinetiska skillnader mellan ungdomar och vuxna baserat på totalt ezetimib.Farmakokinetiska data för den pediatriska populationen sitosterolemi (se avsnitt 4.2).
Pensionärer
Plasmakoncentrationerna av totalt ezetimib är ungefär dubbelt så höga hos äldre (≥ 65 år) som hos unga (18-45 år). LDL-C-minskning och säkerhetsprofil är jämförbara mellan äldre och yngre personer som behandlats med ezetimib (se avsnitt 4.2 ).
Nedsatt leverfunktion
Efter administrering av en enstaka dos på 10 mg ezetimib ökade medelområdet under kurvan (AUC) för totalt ezetimib cirka 1,7-faldigt hos patienter med lätt nedsatt leverfunktion (Child Pugh-poäng 5 eller 6), jämfört med friska försökspersoner. I en 14-dagars multipeldos (10 mg / dag) -studie på patienter med måttligt nedsatt leverfunktion (Child Pugh-poäng 7 till 9) ökade genomsnittlig AUC för totalt ezetimib cirka 4 gånger per dag 1 och dag 14 jämfört med friska försökspersoner. Ingen dosjustering är nödvändig hos patienter med lätt nedsatt leverfunktion. På grund av de okända effekterna av den ökade exponeringen för ezetimib hos patienter med måttligt eller allvarligt nedsatt leverfunktion (Child Pugh -poäng> 9) rekommenderas inte ezetimib till dessa patienter (se avsnitt 4.2. Och 4.4).
Njurskador
Ezetimibe
Efter en engångsdos på 10 mg ezetimib till patienter med allvarligt nedsatt njurfunktion (n = 8; medelvärde CrCl ≤ 30 ml / min), ökade den genomsnittliga AUC för totalt ezetimib cirka 1,5 gånger jämfört med friska försökspersoner. (N = 9), (se avsnitt 4.2).
Ytterligare en patient i denna studie (efter njurtransplantation och behandlad med multipel läkemedelsbehandling inklusive cyklosporin) hade en 12-faldig "exponering för" totalt ezetimib.
Simvastatin
I en studie med patienter med gravt nedsatt njurfunktion (kreatininclearance
Sex
Plasmakoncentrationer av totalt ezetimib är något högre (cirka 20%) hos kvinnor än hos män LDL-C-minskning och säkerhetsprofil är jämförbara mellan män och kvinnor som behandlas med ezetimib.
SLCO1B1 polymorfism
Bärare av c.521T> C -allelen i SLCO1B1 -genen har reducerat OATP1B1 -aktivitet Den genomsnittliga exponeringen (AUC) för den huvudsakliga aktiva metaboliten, simvastatinsyra, är 120% i heterozygota bärare av C -allelen (CT) och 221% i homozygoter (CC) jämfört med patienter med den vanligaste genotypen (TT) .C -allelen har en frekvens på 18% i den europeiska befolkningen. Det finns en risk för ökad exponering för simvastatinsyra hos patienter med SLCO1B1 -polymorfism, vilket kan leda till en ökad risk för rabdomyolys (se avsnitt 4.4).
05.3 Prekliniska säkerhetsdata
INEGY
I samtidiga administreringsstudier med ezetimibe och simvastatin var de toxiska effekterna som observerades i huvudsak de som vanligtvis associerades med statiner. Några av de toxiska effekterna var mer uttalade än de som ses med statinbehandling ensam. Detta tillskrivs farmakokinetiska och / eller farmakodynamiska interaktioner vid samtidig administrering. Interaktioner av detta slag förekom inte i kliniska studier. Episoder av myopati inträffade hos råttor endast efter exponering för doser som var flera gånger högre än den terapeutiska dosen hos människor (cirka 20 gånger AUC -nivån för simvastatin och 1800 gånger AUC -nivån för den aktiva metaboliten). Det fanns inga tecken på att samtidig administrering av ezetimib hade någon effekt på den myotoxiska potentialen för simvastatin.
Hos hundar som administreras samtidigt med ezetimib och statiner, vid låg exponering (gallgångshyperplasi, pigmentackumulering, mononukleär cellinfiltration och små hepatocyter). Dessa förändringar utvecklades inte med exponering för förlängda doser upp till 14 månader. En total återhämtning av levertestresultaten observerades efter utsättande av exponeringen. Dessa data överensstämmer med de som beskrivs med HMG-CoA-hämmare eller hänför sig till de mycket låga kolesterolnivåerna som uppnås hos de undersökta hundarna.
Samtidig administrering av ezetimib och simvastatin var inte teratogent hos råttor. Ett begränsat antal skelettdeformiteter (sammansmältning av stjärtkotorna, minskat antal halskotor) har observerats hos gravida kaninhonor.
I en uppsats in vivo Och in vitro Ezetimibe, administrerat ensamt eller samtidigt administrerat med simvastatin, visade inte genotoxisk potential.
Ezetimibe
Djurstudier med kronisk toxicitet med ezetimibe identifierade inte målorgan för toxiska effekter. Hos hundar som behandlats i 4 veckor med ezetimibe (≥ 0,03 mg / kg / dag) ökade kolesterolkoncentrationen i gallan med en faktor 2,5 till 3,5. Ingen ökad förekomst av kolelithiasis eller andra hepatobiliära effekter observerades dock i en ettårig hundstudie behandlad med doser upp till 300 mg / kg / dag. Det kliniska värdet av dessa data för människor är okänt.Risk för litogenes i samband med terapeutisk användning av ezetimib kan inte uteslutas.
Långsiktiga cancerframkallande tester på ezetimib var negativa.
Ezetimibe hade ingen effekt på fertiliteten hos båda könen hos råttor, ingen teratogenicitet detekterades hos råttor eller kaniner, inte heller förändrades utvecklingen före eller efter födseln. Ezetimibe passerade placentabarriären hos honråttor. kg / dag.
Simvastatin
Baserat på konventionella djurstudier av farmakodynamik, toxicitet vid upprepade doser, gentoxicitet och cancerframkallande, finns det inga andra risker för patienten än de som förväntas utifrån den farmakologiska mekanismen. Vid maximalt tolererade doser hos både råttor och kaniner resulterade simvastatin inte i fostermissbildningar och hade inga effekter på fertilitet, reproduktiv funktion eller neonatal utveckling.
06.0 LÄKEMEDELSINFORMATION
06.1 Hjälpämnen
Butylhydroxianisol
Citronsyra monohydrat
Kroskarmellosnatrium
Hypromellos
Laktosmonohydrat
Magnesiumstearat
Mikrokristallin cellulosa
Propylgallat
06.2 Oförenlighet
Inte relevant.
06.3 Giltighetstid
2 år.
06.4 Särskilda förvaringsanvisningar
Förvaras vid högst 30 ° C.
Blister: Förvaras i originalförpackningen för att skydda läkemedlet från ljus och fukt.
Flaskor: Håll flaskan tätt stängd för att skydda läkemedlet från ljus och fukt.
06.5 Förpackningens innehåll och förpackningens innehåll
INEGY 10 mg / 10 mg, 10 mg / 20 mg och 10 mg / 40 mg
Vit flaska med hög densitet polyeten (HDPE) med barnsäker polypropylenförslutning och torkmedel kiselgel, förseglad med en speciell flik, innehållande 100 tabletter.
INEGY 10 mg / 10 mg
Blister av PVC / aluminiumpolyamid svetsad på aluminiumfolie med vinylharts. Tabletterna kan extraheras genom att trycka på plastfickan. Förpackningar med 7, 10, 14, 28, 30, 50, 56, 84, 98, multipack innehållande 98 (2 kartonger med 49), 100 eller 300 tabletter.
Endosblister i PVC / aluminiumpolyamid svetsad på en aluminiumfolie med vinylharts. Tabletterna kan extraheras genom tryck på plastfickan. Förpackningar om 30, 50, 100 eller 300 tabletter.
INEGY 10 mg / 20 mg, 10 mg / 40 mg
Opak polychlorotrifluoretylen / PVC -blister förseglad till aluminiumfolie med vinylharts. Tabletterna kan extraheras genom att trycka på plastfickan. Förpackning med 90 tabletter.
INEGY 10 mg / 20 mg, 10 mg / 40 mg och 10 mg / 80 mg
Opak polychlorotrifluoretylen / PVC -blister förseglad till aluminiumfolie med vinylharts. Tabletterna kan extraheras genom att trycka på plastfickan. Förpackningar med 7, 10, 14, 28, 30, 50, 56, 84, 98, 100 eller 300 tabletter.
En-dos polyklorotrifluoretylen / PVC-blister förseglad till aluminiumfolie med vinylharts. Tabletterna kan extraheras genom tryck på plastfickan. Förpackningar om 30, 50, 100 eller 300 tabletter.
INEGY 10 mg / 40 mg och 10 mg / 80 mg
Opak polychlorotrifluoretylen / PVC -blister förseglad till aluminiumfolie med vinylharts. Tabletterna kan extraheras genom att trycka på plastfickan. Förpackningar med 7, 10, 14, 28, 30, 50, 56, 84, 98, multipack innehållande 98 (2 kartonger med 49), 100 eller 300 tabletter.
En-dos polyklorotrifluoretylen / PVC-blister förseglad till aluminiumfolie med vinylharts. Tabletterna kan extraheras genom tryck på plastfickan. Förpackningar om 30, 50, 100 eller 300 tabletter.
Alla förpackningsstorlekar kanske inte marknadsförs.
06.6 Anvisningar för användning och hantering
Inga speciella instruktioner.
07.0 INNEHAVARE AV GODKÄNNANDE FÖR FÖRSÄLJNING
Merck Sharp & Dohme Limited
Hertford Road,
Hoddesdon, Hertfordshire
EN11 9BU Storbritannien
08.0 NUMMER FÖR FÖRSÄLJNINGSTILLSTÅND
100 tabletter i flaska med 10 mg / 10 mg AIC n. 036679013
7 tabletter i blisterförpackningar med 10 mg / 10 mg AIC n. 036679025
10 tabletter i blisterförpackningar med 10 mg / 10 mg AIC n. 036679037
14 tabletter i blisterförpackningar med 10 mg / 10 mg AIC n. 036679049
28 tabletter i blister om 10 mg / 10 mg AIC n. 036679052
30 tabletter i blisterförpackningar med 10 mg / 10 mg AIC n. 036679064
50 tabletter i blister om 10 mg / 10 mg AIC n. 036679076
56 tabletter i blisterförpackningar med 10 mg / 10 mg AIC n. 036679088
84 tabletter i blisterförpackningar med 10 mg / 10 mg AIC n. 036679607
98 tabletter i blisterförpackningar med 10 mg / 10 mg AIC n. 036679090
2 x 49 tabletter i 10 mg / 10 mg AIC -blister. n. 036679645
100 tabletter i blister om 10 mg / 10 mg AIC n. 036679102
300 tabletter i blisterförpackningar med 10 mg / 10 mg AIC n. 036679114
30 tabletter i 10 mg / 10 mg endosblister AIC n. 036679126
50 tabletter i 10 mg / 10 mg endosblister AIC n. 036679138 100 tabletter i 10 mg / 10 mg endosblister AIC n. 036679140
300 tabletter i 10 mg / 10 mg endosblister AIC n. 036679153
100 tabletter i flaska med 10 mg / 20 mg AIC n. 036679165
7 tabletter i blisterförpackningar med 10 mg / 20 mg AIC n. 036679177
10 tabletter i blisterförpackningar med 10 mg / 20 mg AIC n. 036679189
14 tabletter i blisterförpackningar med 10 mg / 20 mg AIC n. 036679191
28 tabletter i blisterförpackningar med 10 mg / 20 mg AIC n. 036679203
30 tabletter i blisterförpackningar med 10 mg / 20 mg AIC n. 036679215
50 tabletter i blisterförpackningar med 10 mg / 20 mg AIC n. 036679227
56 tabletter i blisterförpackningar med 10 mg / 20 mg AIC n. 036679239
84 tabletter i blisterförpackningar med 10 mg / 20 mg AIC n. 036679619
98 tabletter i blisterförpackningar med 10 mg / 20 mg AIC n. 036679241
100 tabletter i blisterförpackningar med 10 mg / 20 mg AIC n. 036679254
300 tabletter i blisterförpackningar med 10 mg / 20 mg AIC n. 036679266
30 tabletter i 10 mg / 20 mg endosblister AIC n. 036679278
50 tabletter i 10 mg / 20 mg endosblister AIC n. 036679280
100 tabletter i 10 mg / 20 mg endosblister AIC n. 036679292
300 tabletter i 10 mg / 20 mg endosblister AIC n. 036679304
100 tabletter i flaska med 10 mg / 40 mg AIC n. 036679316
7 tabletter i blisterförpackningar med 10 mg / 40 mg AIC n. 036679328
10 tabletter i blisterförpackningar med 10 mg / 40 mg AIC n. 036679330
14 tabletter i blisterförpackningar med 10 mg / 40 mg AIC n. 036679342
28 tabletter i blisterförpackningar med 10 mg / 40 mg AIC n. 036679355
30 tabletter i blisterförpackningar med 10 mg / 40 mg AIC n. 036679367
50 tabletter i blisterförpackningar med 10 mg / 40 mg AIC n. 036679379
56 tabletter i blisterförpackningar med 10 mg / 40 mg AIC n. 036679381
84 tabletter i blisterförpackningar med 10 mg / 40 mg AIC n. 036679621
98 tabletter i blisterförpackningar med 10 mg / 40 mg AIC n. 036679658
2x49 tabletter i 10 mg / 40 mg AIC -blister. n. 036679393
100 tabletter i blister om 10 mg / 40 mg AIC n. 036679405
300 tabletter i blisterförpackningar med 10 mg / 40 mg AIC n. 036679417
30 tabletter i 10 mg / 40 mg endosblister AIC n. 036679429
50 tabletter i 10 mg / 40 mg endosblister AIC n. 036679431
100 tabletter i 10 mg / 40 mg endosblister AIC n. 036679443
300 tabletter i 10 mg / 40 mg endosblister AIC n. 036679456
7 tabletter i blisterförpackningar med 10 mg / 80 mg AIC n. 036679468
10 tabletter i blisterförpackningar med 10 mg / 80 mg AIC n. 036679470
14 tabletter i blisterförpackningar med 10 mg / 80 mg AIC n. 036679482
28 tabletter i blister om 10 mg / 80 mg AIC n. 036679494
30 tabletter i blister om 10 mg / 80 mg AIC n. 036679506
50 tabletter i blister om 10 mg / 80 mg AIC n. 036679518
56 tabletter i blisterförpackningar med 10 mg / 80 mg AIC n. 036679520
84 tabletter i blisterförpackningar med 10 mg / 80 mg AIC n. 036679633
98 tabletter i blisterförpackningar med 10 mg / 80 mg AIC n. 036679660
2 x 49 tabletter i 10 mg / 80 mg AIC -blister. n. 036679532
100 tabletter i blister om 10 mg / 80 mg AIC n. 036679544
300 tabletter i blister om 10 mg / 80 mg AIC n. 036679557
30 tabletter i 10 mg / 80 mg endosblister AIC n. 036679569
50 tabletter i 10 mg / 80 mg endosblister AIC n. 036679571
100 tabletter i 10 mg / 80 mg endosblister AIC n. 036679583
300 tabletter i 10 mg / 80 mg endosblister AIC n. 036679595
09.0 DATUM FÖR FÖRSTA GODKÄNNANDE ELLER FÖRNYELSE AV GODKÄNNANDET
Datum för första godkännandet: augusti 2005
Sista förnyelsedatum: februari 2010
10.0 DATUM FÖR ÖVERSYN AV TEXTEN
December 2015